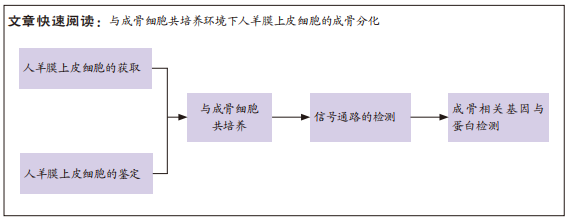
1.1 设计 体外细胞学随机对照实验,所有数据资料采用Student’s t检验和单因素方差分析。
1.2 时间及地点 实验于2021年9月至2022年4月在锦州医科大学附属第一医院骨外科学研究所完成。
1.3 材料
1.3.1 细胞和羊膜 成骨细胞购买于普诺赛公司。羊膜样本由锦州医科大学第一医院妇产科提供,取样前排除胎儿畸形、产妇先天性遗传病及甲肝、乙肝、HIV、梅毒等传染病史,产妇术前签署了知情同意书,经锦州医科大学第一附属医院伦理委员会批准(伦理编号:202241)。
1.3.2 实验试剂与仪器 组织固定液、0.1%TritonX-100、山羊血清、即用型DAPI、抗荧光淬灭封固液、二甲基亚砜、20X TBST(索莱宝,中国);胎牛血清、α-MEM培养基、DMEM/F12
培养基(Hyclone,美国);表皮生长因子(Peprotech,美国);CD45、HlA-DR、CD90、E-Cadherin抗体(博奥森,中国);CK19抗体、波形蛋白抗体(Abcam,美国);GAPDH (Earthox,美国);YAP抗体(CST,美国);ALP、RUNX2、OCN、COL1A1抗体(ABclonal,中国);SDS-PAGE凝胶(碧云天,中国);YAP1-inhibitor(Ribobio,中国);xCELLigence RTCA S16细胞动态监测仪(ACEA Biosciences Inc,美国);荧光显微镜(徕卡,德国)。
1.4 实验方法
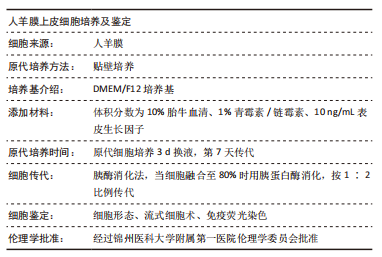
1.4.1 人羊膜上皮细胞的分离和培养 用手术镊和无刀片手术刀将新鲜羊膜与胎盘钝性分离,使用预冷PBS洗净羊膜,去除表面凝血和基质成分,然后使用含1%青霉素的生理盐水洗涤羊膜组织3次,使用无菌纱布吸干羊膜多余水分,置于无菌100 mm培养皿,使用眼科剪将羊膜组织剪成1 cm×1 cm小块,分装于50 mL离心管,每个离心管加入0.25%胰酶15 mL,转移至37 ℃培养箱,消化15 min。使用200目筛网将消化后的羊膜与细胞悬液过滤,得到首次消化细胞悬液,将过滤后的羊膜置于37 ℃培养箱30 min再次消化,收集得到二次消化细胞悬液,混合2次细胞悬液,加入5 mL胎牛血清终止消化。所得细胞悬液以1 200 r/min离心3 min,收获人羊膜上皮细胞,加入低张力液溶解血细胞,得到无血细胞污染人羊膜上皮细胞。使用DMEM/F12完全培养基(含体积分数为10%胎牛血清、10 ng/mL表皮生长因子、1%青霉素/链霉素)将细胞重悬,以1×105/cm2接种到T75培养瓶,37 ℃下CO2培养箱静置培养24 h后进行半换液,72 h首次换液,待细胞生长达80%-90%融合时进行传代。
1.4.2 成骨细胞的准备 将成骨细胞在含体积分数为10%胎牛血清的α-MEM培养基中培养,挑选生长状态良好的细胞进行体外实验。
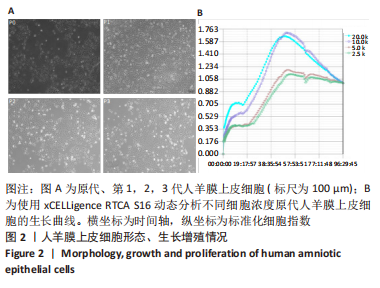
1.4.3 细胞形态学观察 倒置相差显微镜下观察人羊膜上皮细胞形态,记录并采集图片。
1.4.4 人羊膜上皮细胞增殖情况 使用实时细胞分析(RTCA) S16仪器进行实验[16-17],将其置于37 ℃的CO2培养箱中,使用嵌入16孔板的金微电极(E-plate 16 PET)进行细胞增殖实验。用0.25%胰酶将第1代人羊膜上皮细胞进行消化,离心后去上清液,重悬配置成细胞悬液,将细胞悬液稀释调整浓度为2×108 L-1,1×108 L-1,5×107 L-1,2.5×107 L-1备用。在E-Plate 16板的孔中加入50 µL DMEM/F12培养基测定基线,然后每孔加入0.1 mL的细胞悬液(20×103,10×103,5×103,2.5×103个/孔)。每隔15 min记录1次,记录96 h内细胞增殖曲线。
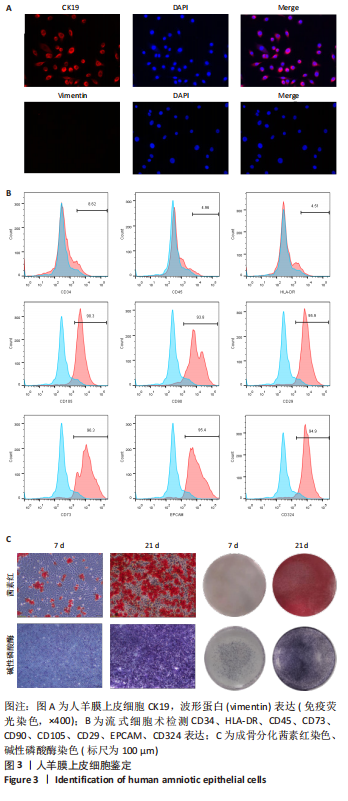
1.4.5 流式细胞仪鉴定细胞蛋白表型 取出生长状态良好的第3代人羊膜上皮细胞,使用0.25%胰蛋白酶消化10 min,将全部细胞消化至脱落,加入等体积DMEM/F12培养基中止消化,离心收集细胞,PBS洗涤1次,再次离心收集细胞;将细胞重悬在1 mL PBS中,加入预冷的等体积甲醛溶液,室温固定10 min,向各管待测样本中加入2 mL PBS,充分洗涤,并以200×g离心5 min,回收细胞;重复洗涤操作1次,并回收细胞;加入100 μL抗体标记液重悬细胞静置5 min,然后加入100 μL体积分数为10%山羊血清于抗体标记液,室温封闭15 min;向每支样品管中加入相应经抗体稀释液按合适比例稀释后的无荧光一抗(CD34、HLA-DR、CD45、CD73、CD90、CD105、CD29、EPCAM、CD324一抗),室温孵育30 min;加入2 mL抗体标记液,200×g离心5 min,离心回收细胞,重复1次;加入一定比例稀释的荧光素二抗,室温孵育40 min;将细胞重悬在10 g/L多聚甲醛溶液中,上流式细胞仪检测。获取数据,使用flowjo软件(V10版)分析结果。
1.4.6 免疫细胞化学鉴定 生长融合达到80%左右的第1代人羊膜上皮细胞进行免疫荧光染色。在37 ℃恒温培养条件下,使用胰蛋白酶消化5-10 min,至细胞游离悬浮,离心回收细胞。使用DMEM/F12完全培养基将细胞浓度调整为2×107 L-1,取1 mL细胞悬液,接种于培养皿中培养。将贴附2 d的细胞取出,使用40 g/L多聚甲醛固定后PBS漂洗3次,每次5 min,用TritonX-100通透液处理细胞20 min,使用预冷PBS漂洗后加入封闭液封闭30 min;丢弃封闭液,滴加CK19一抗(1∶1 000)或波形蛋白一抗(1∶1 000),4 ℃孵育过夜。次日冲洗3次,然后加入带荧光的二抗,孵育1.5 h,冲洗后滴加DAPI避光孵育5 min,PBS冲洗3次,滴加抗荧光淬灭封固液,镜下拍照记录。
1.4.7 人羊膜上皮细胞成骨分化能力鉴定 第3代人羊膜上皮细胞生长融合达80%时进行成骨分化诱导,配制人羊膜上皮细胞成骨分化诱导培养基(含有100 nmol/L地塞米松、50 mg/L
抗坏血酸和5 mmol/L β-甘油磷酸盐的α-MEM培养基),将第3代生长状态良好的人羊膜上皮细胞均匀接种于6孔板,使用DMEM/F12完全培养基培养;待细胞生长至基本融合,更换为成骨分化诱导培养基,每3 d换液1次,于7,21 d结束诱导进行碱性磷酸酶、茜素红染色。
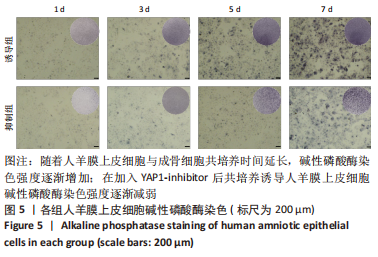
1.4.8 碱性磷酸酶染色 将诱导分化7,21 d的细胞用PBS洗涤,在室温下用40 g/L多聚甲醛固定30 min,去离子水冲洗2次,加入碱性磷酸酶染液覆盖细胞,避光孵育60 min后去离子水洗涤4次,在倒置显微镜下观察染色情况。
1.4.9 茜素红染色 将诱导分化7,21 d的细胞用PBS洗涤,在室温下用40 g/L多聚甲醛固定30 min,去离子水冲洗2次,加入40 mmol/L茜素红S,室温下放置 45 min,然后用去离子水洗涤4次以去除非特异性结合的污渍,干燥后在倒置显微镜下观察染色情况。
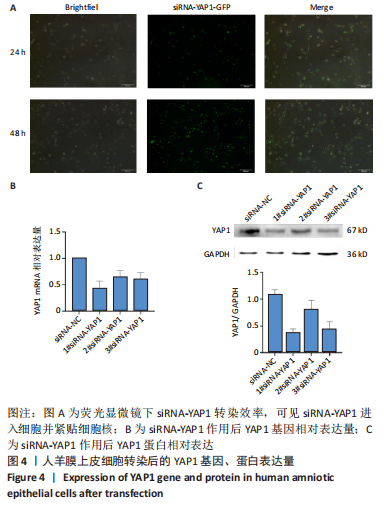
1.4.10 siRNA沉默YAP基因的表达 在人羊膜上皮细胞生长融合度达80%的6孔板中加入6% 1×riboFECT™ CP Buffer、0.6% 1×riboFECT™ CP Reagent、50 nmol/L siRNA-NC或1#siRNA-YAP1
或2#siRNA-YAP1或3#siRNA-YAP1,于第3天行PCR检测YAP1的基因相对表达量,第7天检测YAP1蛋白相对表达量,以筛选效果最好的siRNA-YAP1。使用荧光显微镜观察siRNA转染情况,并检测7 d内碱性磷酸酶活性。
1.4.11 成骨细胞与人羊膜上皮细胞共培养诱导体系的构建[18-20] 取生长状态良好的成骨细胞和生长融合至80%-90%的第3代人羊膜上皮细胞,PBS 清洗3次,胰酶消化,使用α-MEM完全培养液重悬备用。实验分为4组,分别为:①空白组:人羊膜上皮细胞接种于6孔板,细胞浓度为 5×107 L-1,每孔1 mL,α-MEM完全培养基培养21 d;②对照组:人羊膜上皮细胞接种于6孔板,细胞浓度为 5×107 L-1,每孔1 mL,α-MEM完全培养基培养,待细胞完成贴壁,融合至90%时加入siRNA-YAP1,每3 d更换1次培养基,并重新加入siRNA-YAP1,直至21 d培养结束;③诱导组:将成骨细胞与人羊膜上皮细胞体外共培养,人羊膜上皮细胞接种于6孔板,细胞浓度为 5×107 L-1,每孔1 mL,α-MEM完全培养基培养,在transwell 上室中接种成骨细胞,细胞浓度为 1×108 L-1,每孔1 mL,α-MEM完全培养基培养,共培养21 d;④抑制组:人羊膜上皮细胞接种于6孔板,细胞浓度为 5×107 L-1,每孔1 mL,α-MEM完全培养基培养,并在transwell上室中接种成骨细胞,细胞浓度为1×108 L-1,每孔1 mL,α-MEM完全培养基培养,待细胞完成贴壁,融合至90%时加入siRNA-YAP1,每3 d更换1次培养基,并重新加入siRNA-YAP1,直至21 d培养结束。各组细胞培养模式见图1。
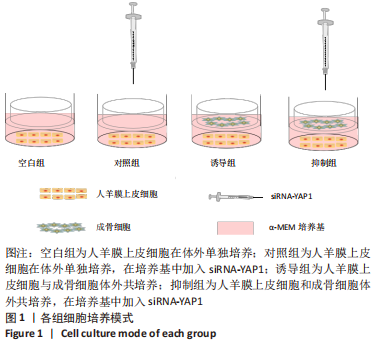
1.5 主要观察指标
1.5.1 碱性磷酸酶染色 按上述分组干预21 d后的细胞,使用碱性磷酸酯酶显色试剂盒进行显色,在倒置显微镜下观察记录。
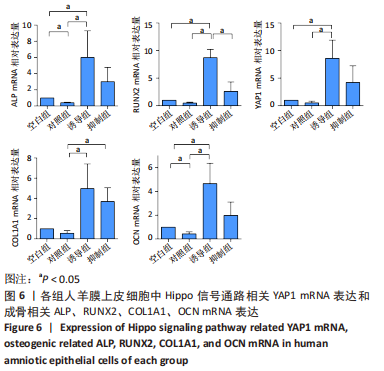
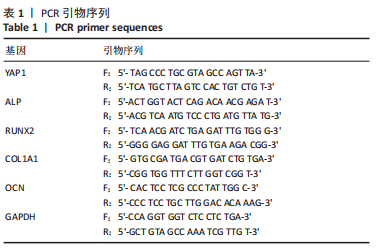
1.5.2 RT-qPCR 检测人羊膜上皮细胞相关基因表达 各组人羊膜上皮细胞培养21 d后,弃去培养基,用4 ℃预冷的PBS漂洗3次,用离心柱提取RNA,向细胞样品依次加入裂解液、结合液,离心后分别加入洗涤液洗去杂质,加入提取液得到RNA样品,提取总 RNA,使用分光光度计测量其纯度和浓度。按照42 ℃ 15 min,85℃ 5 s,4 ℃维持的方式进行反转录。按照95 ℃预变性30 s,95 ℃,5 s→60 ℃,34 s 循环40次,60 ℃ →95 ℃,每15 s升温 0.5 ℃测量熔解曲线的方式进行扩增。采用 2-ΔΔCT法计算 mRNA的相对表达量。PCR引物序列见表1。
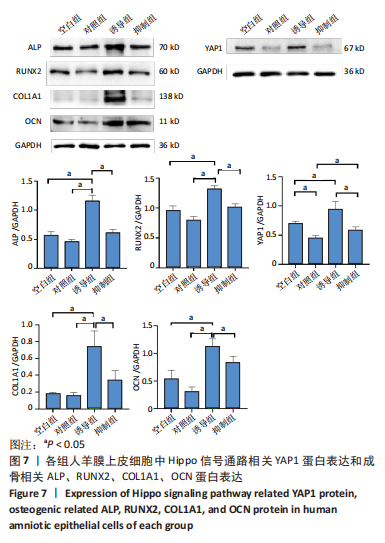
1.5.3 Western blot 检测人羊膜上皮细胞相关蛋白表达 各组人羊膜上皮细胞诱导培养21 d,将培养皿置于冰上,使用RIPA裂解,通过SAS-PAGE 凝胶分离蛋白裂解物转移到聚偏二氟乙烯膜上,用 5% BSA封闭膜并在4 ℃环境下孵育以下一抗:YAP(1∶1 000)、ALP(1∶1 000)、RUNX2(1∶1 000)、OCN(1∶1 000)、COL1A1(1∶1 000)、GAPDH(1∶5 000),使用山羊抗兔二抗标记,用化学发光液试剂盒进行发光显影,采用ImageJ软件分析蛋白条带灰度。
1.6 统计学分析 所有实验至少重复3次,数值以均数±标准误表示。使用ImageJ和GraphPad Prism 8.0软件(GraphPadSoftware,la Jolla,CA),采用Student’s t检验和单因素方差分析,P < 0.05为差异有显著性意义。文章统计学方法已经通过锦州医科大学附属第一医院生物统计学专家审核。