中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (33): 5283-5291.doi: 10.12307/2023.713
• 牙髓及牙周膜干细胞 Dental pulp and periodontal ligament stem cells • 上一篇 下一篇
RNA结合蛋白Lin28A差异表达可调控牙周膜干细胞的成骨分化
何 琴1,2,3,卜 艳1,2,林光磊1,2,罗 晶1,2,雍 敏1,3,黄永清1,4
- 1宁夏医科大学口腔医学院正畸学系,宁夏回族自治区银川市 750004;2宁夏回族自治区干细胞与再生医学重点实验室,宁夏回族自治区银川市 750004;3宁夏医科大学总医院口腔正畸科,宁夏回族自治区银川市 750004;4宁夏医科大学口腔医学院口腔颌面外科学系,宁夏回族自治区银川市 750004
Differential expression of RNA binding protein Lin28A regulates osteoblastic differentiation of periodontal ligament stem cells
He Qin1, 2, 3, Bu Yan1, 2, Lin Guanglei1, 2, Luo Jing1, 2, Yong Min1, 3, Huang Yongqing1, 4
- 1Department of Orthodontics, School of Stomatology, Ningxia Medical University, Yinchuan 750004, Ningxia Hui Autonomous Region, China; 2Key Laboratory of Stem Cell and Regenerative Medicine of Ningxia Hui Autonomous Region, Yinchuan 750004, Ningxia Hui Autonomous Region, China; 3Department of Orthodontics, General Hospital of Ningxia Medical University, Yinchuan 750004, Ningxia Hui Autonomous Region, China; 4Department of Oral and Maxillofacial Surgery, School of Stomatology, Ningxia Medical University, Yinchuan 750004, Ningxia Hui Autonomous Region, China
摘要:
文题释义:
牙周膜干细胞:是牙周膜来源的间充质干细胞群体,具有多向分化、自我更新及迁移等能力,从而实现牙周骨组织修复。其中,牙周膜干细胞成骨分化是骨组织修复和再生的生物学基础,揭示其具体的调控功能,可引导干细胞发挥其潜能,有利于牙周组织的维持和生物再生。Lin28A:是一种高度保守的RNA结合蛋白,首次从秀丽隐杆线虫中发现,被认为是调控机体发育特征、细胞代谢和维持干细胞处于胚胎状态的重要重编程因子。过去的研究显示,该蛋白可通过与靶标RNA直接作用和间接作用,实现调控细胞的生长和分化;Lin28A的表达差异能调节胚胎干细胞的发育时间和自我更新能力,是细胞活动的主要调节因子。
背景:Lin28A能影响细胞活动的多个方面,包括胚胎干细胞的自我更新、体细胞的重编程、个体的生长发育、组织代谢及致癌作用等,而它对牙周膜干细胞成骨分化的影响国内外均没有深入研究,其影响机制更未见报道。
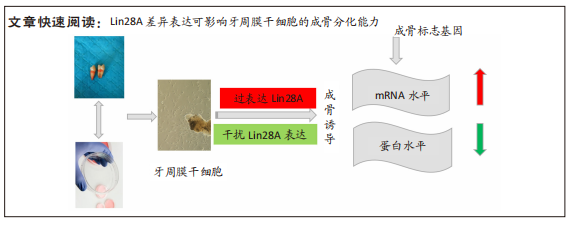
目的:探索Lin28A对牙周膜干细胞成骨分化能力的影响。
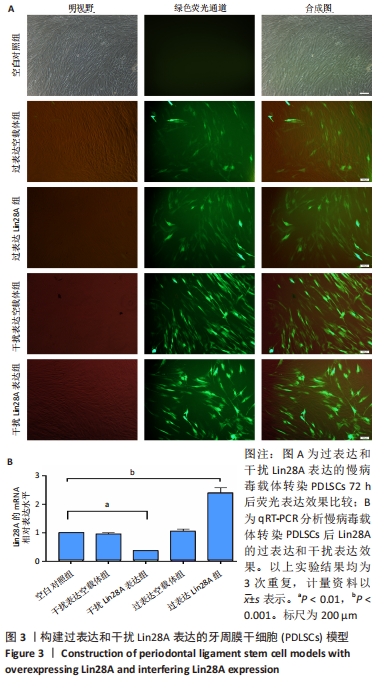
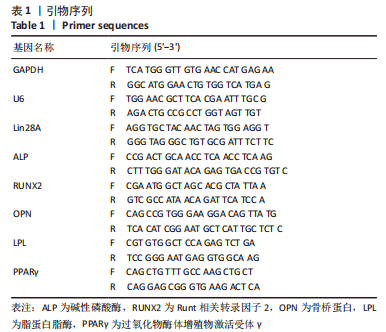
方法:经典酶消化法分离、培养人牙周膜干细胞,qRT-PCR检测 Lin28A 在该类细胞中的分布情况及其在成骨诱导不同时间的差异性表达;构建Lin28A过表达及干扰表达的慢病毒载体转染至牙周膜干细胞,荧光显微镜观察转染效果;qRT-PCR验证慢病毒转染后Lin28A的表达差异,并进一步从正反两个方面检测成骨诱导培养过程中成骨基因碱性磷酸酶、Runt相关转录因子2和骨桥蛋白的表达量以及碱性磷酸酶染色和茜素红染色,Western blot检测Runt相关转录因子2的蛋白表达水平;应用生物信息学技术预测和双荧光素酶结合实验验证与Lin28A有关的let-7家族成员之间的相关关系,并通过成骨诱导培养差异表达Lin28A的牙周膜干细胞,测定细胞成骨分化过程中表达变化最明显的miRNA。
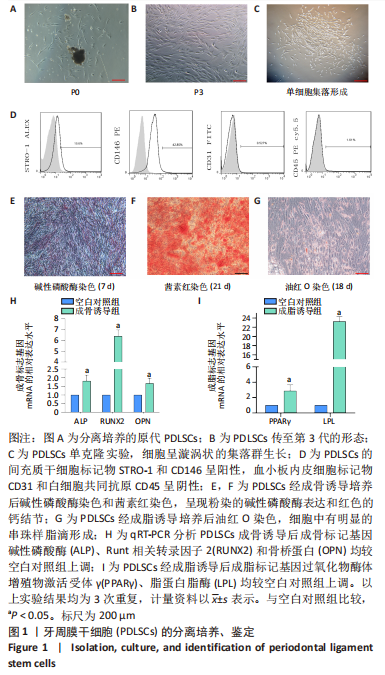
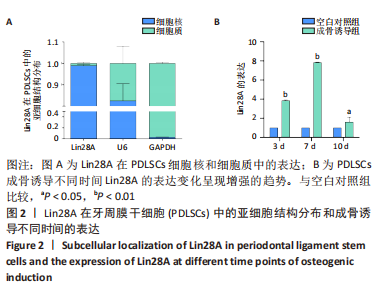
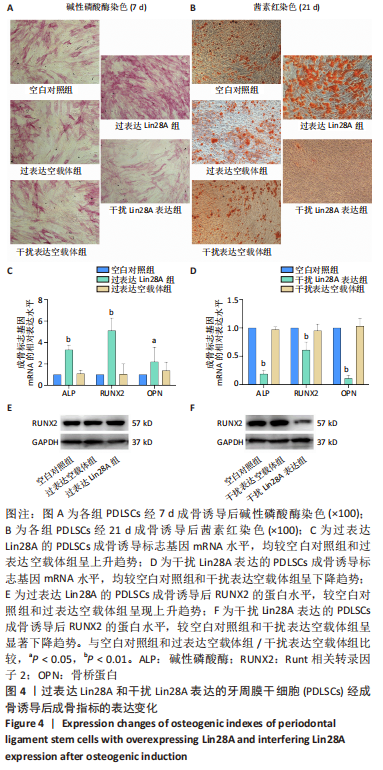
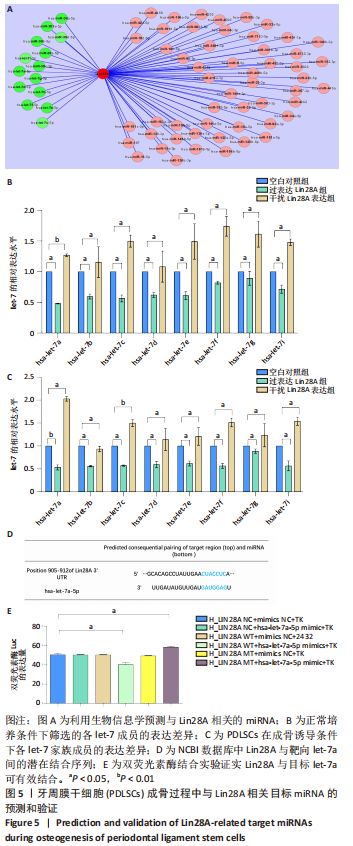
结果与结论:①Lin28A 富集在牙周膜干细胞的细胞核中,且在成骨诱导不同时间后呈表达上升的趋势;②与空白对照组比较,在过表达Lin28A的牙周膜干细胞模型中,碱性磷酸酶染色和茜素红染色相较空白对照组明显深染,成骨基因碱性磷酸酶、Runt相关转录因子2及骨桥蛋白的表达量分别增加3.3倍、5.1倍及2.2倍(P < 0.01);干扰Lin28A表达的细胞模型中,碱性磷酸酶染色和茜素红染色相较对照组染色减少,成骨基因碱性磷酸酶、Runt相关转录因子2及骨桥蛋白的表达量分别下降19%,61%及10%(P < 0.01);③成骨相关转录因子Runt相关转录因子2的蛋白表达水平与mRNA的差异趋势一致,过表达组呈上升趋势,干扰组呈下降趋势;④生物信息学预测出与Lin28A相关的let-7家族成员有8个,分别为let-7a、let-7b、let-7c、let-7d、let-7e、let-7f、let-7g和let-7i,经正常培养和成骨诱导培养筛选发现let-7a和let-7c随Lin28A的表达差异而发生明显的变化,以let-7a的表达趋势最显著;双荧光素酶结合实验也证实let-7a与Lin28A的3’-UTR直接结合,参与影响牙周膜干细胞的成骨分化过程;⑤结果提示:Lin28A参与调控牙周膜干细胞成骨分化,呈正性相关,即过表达Lin28A使牙周膜干细胞成骨能力增强,干扰Lin28A表达后牙周膜干细胞成骨能力减弱;牙周膜干细胞成骨分化受到Lin28A的调控影响。
https://orcid.org/0000-0003-0082-650X (何琴)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: