中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (24): 3810-3817.doi: 10.12307/2023.698
• 牙髓及牙周膜干细胞 Dental pulp and periodontal ligament stem cells • 上一篇 下一篇
静压力作用下三维培养人牙周膜干细胞促进RAW264.7细胞的破骨向分化
韩 行,李雯雯,马文盛
- 河北医科大学口腔医院,河北医科大学口腔医院口腔正畸科,河北省口腔医学重点实验室,河北省口腔疾病临床医学研究中心,河北省石家庄市 050000
Three-dimensional cultured periodontal ligament stem cells promote osteoclastic differentiation of RAW264.7 under static compression
Han Xing, Li Wenwen, Ma Wensheng
- Stomatological Hospital of Hebei Medical University, Department of Orthodontics of Stomatological Hospital of Hebei Medical University, Key Laboratory of Stomatology in Hebei Province, Clinical Medical Research Center of Stomatology in Hebei Province, Shijiazhuang 050000, Hebei Province, China
摘要:
文题释义:
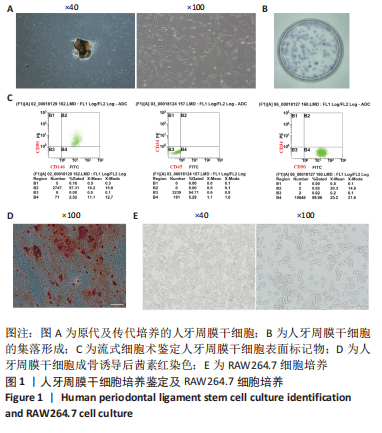
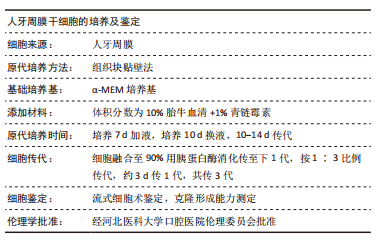
三维培养:是一种特殊的细胞培养方式,是指将具有三维结构不同材料的载体与各种不同种类的细胞在体外共同培养,使细胞能够在载体的三维立体空间结构中迁移、生长,构成三维的细胞-载体复合物。某种程度上更加接近细胞在体内的生理环境,可以维持干细胞的干性,模拟细胞与细胞在空间上的交流,是目前组织工程的研究重点之一。RAW264.7细胞:为小鼠单核巨噬细胞,是用Abelson鼠白血病病毒诱导BALB/c小鼠发生肿瘤后,收集小鼠腹水单核样巨噬细胞得到的细胞株,是目前公认的成系的破骨细胞前体细胞。
背景:牙周膜干细胞作为种子细胞,其成骨潜能成为研究热点,而牙周膜干细胞对破骨细胞活动的调控研究较少,有待进一步探索。
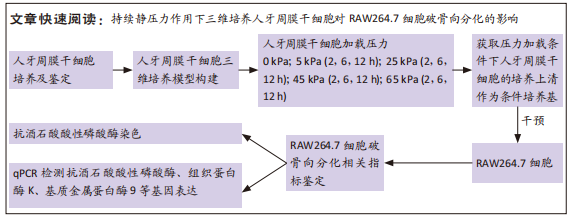
目的:研究持续静压力作用下三维培养人牙周膜干细胞对RAW264.7细胞破骨向分化的影响。
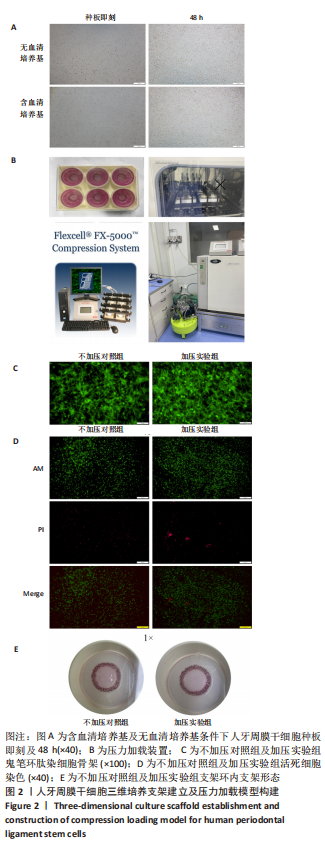
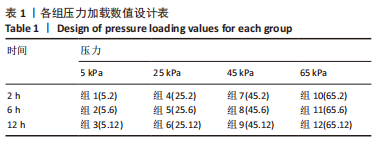
方法:取第3,4代人牙周膜干细胞进行三维培养,随机分为13组,采用FLEXCELL5000C加压仪器,分别施加5 kPa(2,6,12 h),
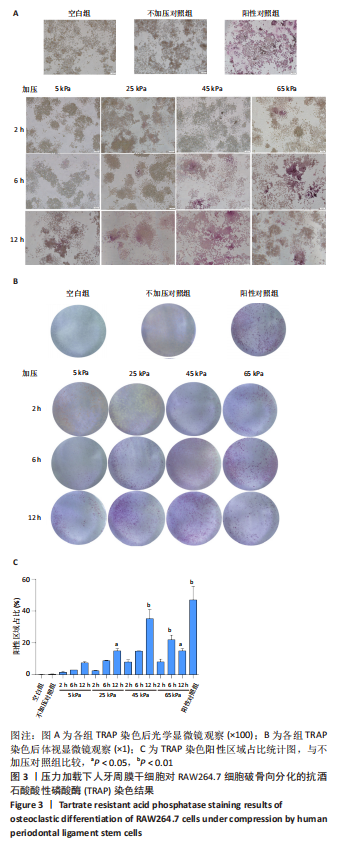
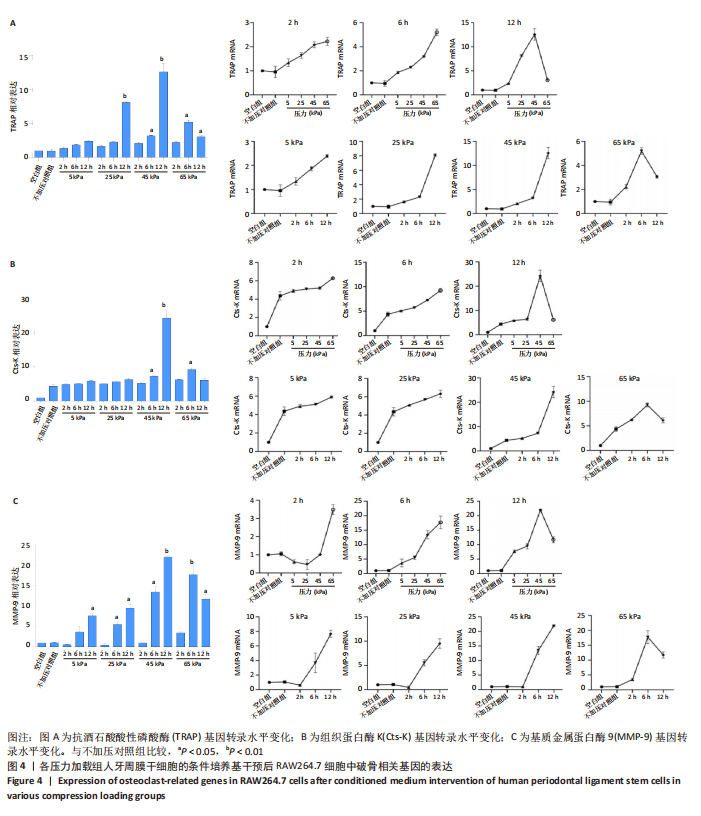
25 kPa(2,6,12 h),45 kPa(2,6,12 h),65 kPa(2,6,12 h)的持续静压力,第13组不加压。将细胞上清作为条件培养基按照一定比例作用于RAW264.7细胞,5 d后抗酒石酸酸性磷酸酶染色及qPCR检测破骨相关基因抗酒石酸酸性磷酸酶、组织蛋白酶K、基质金属蛋白酶9的表达。
结果与结论:①三维培养下加压实验组与不加压对照组支架形态稳定,细胞状态良好;②压力加载组人牙周膜干细胞条件培养基促进RAW264.7细胞的破骨分化;③在一定范围内,促破骨作用与力值加载条件呈正相关,45 kPa,12 h组促RAW264.7细胞破骨分化作用最强;65 kPa,12 h组的促破骨能力减弱;④结果表明,静压力作用下三维培养的牙周膜干细胞通过旁分泌途径促进RAW264.7的破骨分化,力值加载条件与促破骨作用具有相关性。
https://orcid.org/0000-0002-1583-7271(韩行) ;https://orcid.org/0000-0003-3288-1239(马文盛)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: