中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (19): 3097-3102.doi: 10.3969/j.issn.2095-4344.3521
• 干细胞综述 stem cell review • 上一篇 下一篇
间充质干细胞外泌体应用于生殖系统疾病治疗的作用与机制
赵双丹,郑嘉华,亓文博,黄向华
- 河北医科大学第二医院妇产科,河北省石家庄市 050000
-
收稿日期:2020-04-11修回日期:2020-04-18接受日期:2020-06-21出版日期:2021-07-09发布日期:2021-01-14 -
通讯作者:黄向华,博士,教授,河北医科大学第二医院妇产科,河北省石家庄市 050000 -
作者简介:赵双丹,女,1990年生,河北省秦皇岛市人,汉族,2020年河北医科大学毕业,博士,医师,主要从事妇产科临床工作及干细胞领域研究。
Role and mechanism of exosomes derived from mesenchymal stem cells in reproductive system diseases
Zhao Shuangdan, Zheng Jiahua, Qi Wenbo, Huang Xianghua
- Department of Obstetrics and Gynecology, the Second Hospital of Hebei Medical University, Shijiazhuang 050000, Hebei Province, China
-
Received:2020-04-11Revised:2020-04-18Accepted:2020-06-21Online:2021-07-09Published:2021-01-14 -
Contact:Huang Xianghua, MD, Professor, Department of Obstetrics and Gynecology, the Second Hospital of Hebei Medical University, Shijiazhuang 050000, Hebei Province, China -
About author:Zhao Shuangdan, PhD, Physician, Department of Obstetrics and Gynecology, the Second Hospital of Hebei Medical University, Shijiazhuang 050000, Hebei Province, China
摘要:
文题释义:
外泌体:是一种直径为30-150 nm的小囊泡,包含有多种蛋白质和遗传物质,外泌体可以由几乎所有类型哺乳动物细胞分泌,并且广泛分布在各种体液中,能够通过细胞间的传递发挥重要作用,在组织修复、疾病的诊断与治疗领域有重要的前景。
间充质干细胞:来源于发育早期的中胚层,属于多能干细胞。间充质干细胞能够分化成不同的细胞系,分泌细胞因子和细胞外囊泡,在免疫调节、血管生成、伤口愈合和组织再生等方面发挥作用。
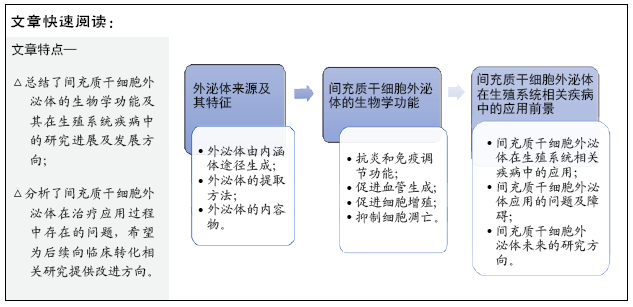
背景:间充质干细胞是再生医学领域最常用的细胞类型之一。近年来研究发现,间充质干细胞来源外泌体在某些生殖系统疾病中发挥重要作用,并且逐渐成为生殖领域研究的热点。
目的:综述间充质干细胞来源外泌体在卵巢早衰、多囊卵巢综合征、宫腔粘连和常见生殖系统肿瘤等疾病中的研究进展,并对间充质干细胞来源外泌体在未来的应用与研究进行了探讨。
方法:在PubMed和CNKI数据库中进行相关文献检索,关键词为“mesenchymal stem cells,exosome,premature ovarian insufficiency,premature ovarian failure,polycystic ovary syndrome,intrauterine adhesions,endometrium,Asherman’s syndrome,ovarian cancer,cervical cancer,endometrial carcinoma,embryo”及“间充质干细胞,外泌体,原发性卵巢功能不全,卵巢早衰,多囊卵巢综合征,宫腔粘连,卵巢癌,宫颈癌,子宫内膜癌,胚胎”,纳入56篇文献进行综述。
结果与结论:间充质干细胞来源外泌体不仅可以作为某些生殖系统疾病的治疗载体,更有可能成为研究疾病发生机制的重要靶点。间充质干细胞来源外泌体有望成为一种新兴的“无细胞”疗法用于生殖系统疾病的治疗。
https://orcid.org/0000-0002-4609-1222(黄向华)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号:
引用本文
赵双丹, 郑嘉华, 亓文博, 黄向华. 间充质干细胞外泌体应用于生殖系统疾病治疗的作用与机制[J]. 中国组织工程研究, 2021, 25(19): 3097-3102.
Zhao Shuangdan, Zheng Jiahua, Qi Wenbo, Huang Xianghua. Role and mechanism of exosomes derived from mesenchymal stem cells in reproductive system diseases[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 3097-3102.
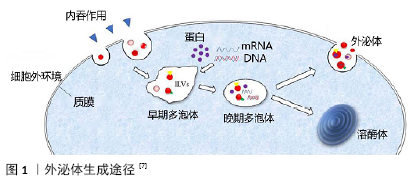
2.2 外泌体的生物学功能 外泌体表面含有各种可以维持其形态的脂类物质,如甘油二脂、胆固醇、鞘脂、磷脂等,这些脂类分子还可以作为参与各种生物学过程的信号分子[12],而且外泌体含有多种蛋白质和遗传物质,在细胞微环境中发挥重要作用[13]。下面,将全面介绍间充质干细胞外泌体在不同生物学行为中的最新研究进展。
2.2.1 抗炎和免疫调节 间充质干细胞具有减轻炎症和免疫反应的内在潜能[14]。外泌体具有与其来源细胞相似的免疫调节功能[15]。研究发现,脂肪间充质干细胞外泌体可以降低干扰素γ和转录因子的表达,上调免疫调节细胞因子的表达,降低局部炎症反应,起到免疫调节作用[16]。在体外脂肪间充质干细胞外泌体可以抑制CD4+和CD8+T细胞向效应细胞或记忆细胞表型分化;此外,脂肪间充质干细胞外泌体还通过减少干扰素γ的分泌来抑制T细胞的激活[17]。ZHAO等[18]
发现脂肪间充质干细胞外泌体可以转移到巨噬细胞中,增加M2相关精氨酸酶1和白细胞介素10的mRNA水平,诱导促炎的M1型巨噬细胞转化为抗炎的M2型巨噬细胞,并显著抑制脂多糖和干扰素γ刺激的巨噬细胞炎性反应。EBRAHIM
等[19]发现在大鼠宫腔粘连模型中骨髓间充质干细胞外泌体可以通过调节炎症反应和减少炎症细胞因子(例如白细胞介素1,白细胞介素6和肿瘤坏死因子α)的释放促进损伤子宫内膜的修复。在许多情况下,间充质干细胞外泌体的治疗作用来源于其抗炎活性。间充质干细胞外泌体含有抗炎成分,这些成分被传递到受体细胞,减轻炎症反应。利用这些特点,间充质干细胞外泌体可以应用于多种炎症性疾病和自身免疫性疾病。
2.2.2 促血管生成 血管生成在胚胎发育、生殖、组织再生修复等不同生理事件中起着至关重要的作用。间充质干细胞可以释放具有增强血管生长功能的外泌体,促进血管内皮细胞的增殖[20]。脂肪间充质干细胞外泌体携带与血管生成相关的miRNA亚类(miR-126,miR-130a,miR-132)[21-22],它们可以通过增加内皮细胞中的几种生长因子水平(例如血管内皮生长因子、表皮细胞生长因子和成纤维细胞生长因子等)来促进血管生成[23]。将间充质干细胞外泌体与小鼠胚胎共培养,结果发现间充质干细胞外泌体触发胚胎中促血管生成分子(血管内皮生长因子和血小板衍生生长因子AA)的释放,这说明间充质干细胞外泌体可以促进子宫内膜血管生成、分化和组织重塑[24]。此外EBRAHIM等[19]和SARIBAS等[25]研究表明外泌体治疗宫腔粘连大鼠的子宫内膜中血管内皮生长因子表达明显增加,说明间充质干细胞外泌体治疗可以促进子宫组织的血管化。细胞分泌外泌体的内容物及其浓度会随着所处环境的改变而变化。HAN等[26]发现脂肪间充质干细胞外泌体可以明显增强人脐静脉内皮细胞的体外血管形成能力,且低氧预处理组脂肪间充质干细胞外泌体效果更好。脂肪间充质干细胞外泌体还提高了人脐静脉内皮细胞中血管生成相关基因促血管生成素1(Ang-1)及其受体Tie-1的表达。Ang-1/Tie-1
是除VEGF/VEGFR之外另一条调控血管生成的重要信号通
路[27]。此外,与常氧处理组脂肪间充质干细胞外泌体相比,蛋白质阵列显示缺氧预处理的脂肪间充质干细胞外泌体中成纤维细胞生长因子、血管内皮生长因子、表皮细胞生长因子和单核细胞趋化蛋白等血管生成相关蛋白富集[28],这表明低氧处理的脂肪间充质干细胞外泌体具有更高的促进血管生成能力。因此,可以通过间充质干细胞的预处理调节外泌体的生物活性,进而增强间充质干细胞外泌体的治疗效果。
2.2.3 促进细胞增殖、抑制细胞凋亡 研究表明,间充质干细胞外泌体通过各种机制在不同类型细胞的增殖和迁移中发挥作用。Wnt/β-catenin信号通路在伤口愈合的增殖期起重要作用[29]。在皮肤损伤模型中,脂肪间充质干细胞外泌体可以通过激活Wnt信号通路促进角质形成细胞(HaCaT)的增殖和迁移,同时上调抗凋亡蛋白Bcl-2的表达,下调促凋亡蛋白Bax的表达,抑制细胞凋亡,从而发挥促进伤口愈合的生物学作用[30]。此外,脂肪间充质干细胞外泌体可以通过转移和调节蛋白质及miRNAs在细胞凋亡中发挥抑制作用。研究表明,在缺氧和无血清培养基诱导后,脂肪间充质干细胞外泌体可显著抑制骨细胞活性氧的过度产生,上调Bcl-2的表达,下调Bax的表达,抑制无血清诱导的骨细胞凋亡[31]。研究表明,与未处理组相比,miR-126过表达的脂肪间充质干细胞外泌体可以通过保护心肌细胞免于凋亡、炎症、纤维化和增加血管生成来防止心肌损伤,具有更强的治疗潜力[32]。在皮瓣移植模型中,H2O2预处理脂肪间充质干细胞外泌体组凋亡细胞明显较少,缺血再灌注损伤后皮瓣存活率较高[33]。此外,研究表明脐带间充质干细胞外泌体特异性miRNA可以通过促进细胞周期和抑制细胞凋亡来促进阴道上皮细胞的增殖,表明脐带间充质干细胞外泌体可能对阴道重建有治疗作用[34]。
总之,间充质干细胞外泌体可以有效转运特异性蛋白、脂质、mRNA和miRNA等多种生物活性物质,进而发挥相应的生物学功能。因此,外泌体可用作临床疾病治疗和再生医学治疗的新载体。
2.3 间充质干细胞外泌体在生殖系统相关疾病中的应用前景 间充质干细胞外泌体的作用和治疗效果已经在许多疾病中得到观察和证实。前期,研究人员只是简单地探索天然来源外泌体的基本功能,并将其应用于疾病模型,对其内容几乎没有任何修改。随着研究的深入,许多研究表明外泌体的一些特性和内容是可以被其他物质修饰的。在某些培养条件下,外泌体可以作为稳定有效的载体,装载特定的蛋白质、脂类和遗传物质,因此可以作为一种极具有治疗前景的运输载体将生物活性物质运送到靶向组织或器官[35]。生殖系统疾病是困扰广大女性的一类常见疾病。在检索数据库后,作者发现外泌体在女性生殖健康领域的研究有限。因此,文章将重点介绍近年来外泌体在女性生殖系统疾病中的研究进展及治疗前景,以提供和总结当前这方面有价值的信息。
2.3.1 外泌体与卵巢功能不全 原发性卵巢功能不全是指女性在40周岁以前因妊娠以外的原因导致闭经至少4个月,而且卵泡期血清检查至少2次出现卵泡刺激素> 25 IU/L,雌二醇< 73.2 pmol/L。过去将卵泡刺激素> 40 IU/L的患者又称为卵巢早衰,其特征是闭经、低雌激素、高促性腺激素、不孕和卵泡数量减少。目前,原发性卵巢功能不全无法逆转,尽管可以使用长期激素替代疗法缓解更年期症状,但很难防止妇女卵巢过早老化[36]。有研究表明原发性卵巢功能不全与卵巢颗粒细胞的损伤和凋亡密切相关,间充质干细胞外泌体在体外可以抑制化疗诱导的卵巢颗粒细胞凋亡,说明间充质干细胞外泌体在原发性卵巢功能不全治疗中具有积极意义[37]。
HUANG等[38]研究发现间充质干细胞外泌体可以通过调节SMAD信号途径显著减轻原发性卵巢功能不全小鼠模型的卵巢损伤;在注射间充质干细胞外泌体后,原发性卵巢功能不全小鼠4个阶段的卵泡数量显著增加,血清激素水平也恢复到正常,说明间充质干细胞外泌体通过调节SMAD信号通路改善原发性卵巢功能不全患者卵巢功能。此外,外泌体中含有大量miRNA,且这些miRNA靶向基因主要富集于PI3K和凋亡途径,与卵泡激活和卵巢功能密切相关[39]。在化疗诱导的卵巢早衰小鼠模型中,人羊膜上皮细胞来源的外泌体主要通过转移miRNAs抑制卵巢颗粒细胞凋亡,在恢复卵巢功能方面发挥了有效的作用[39]。因此,间充质干细胞外泌体具有治疗原发性卵巢功能不全和卵巢早衰的潜能,但是仍然需要进一步研究来证实和探索其可能的机制。
2.3.2 外泌体与多囊卵巢综合征 多囊卵巢综合征是导致育龄女性生殖障碍常见的疾病之一[40],其确切发病机制仍不清楚,但越来越多的证据表明胰岛素抵抗、慢性炎症和氧化应激等参与了多囊卵巢综合征的发病机制,并可能伴有亚临床心血管疾病和一些恶性病变,如子宫内膜癌[41]。研究表明,多囊卵巢综合征患者和健康人的血液、卵泡液和颗粒细胞中的miRNAs存在显著差异[42]。间充质干细胞外泌体中富集了多种miRNA,提示间充质干细胞外泌体可能具有治疗多囊卵巢综合征的潜力。多囊卵巢综合征患者体内氧化还原酶水平显著升高,而氧化还原酶水平与肥胖、高雄激素血症和慢性炎症显著相关,多囊卵巢综合征患者的氧化还原酶水平异常是源于该疾病还是其并发症仍有争议[43]。SHANG等[44]发现间充质干细胞外泌体可以减轻肥胖小鼠的脂肪组织炎症和胰岛素抵抗,对糖尿病有一定的治疗作用,说明间充质干细胞外泌体在多囊卵巢综合征并发症治疗中有积极意义。程序性细胞死亡蛋白4是凋亡过程中高表达的关键因子,在多囊卵巢综合征患者中,程序性细胞死亡蛋白4上调,而敲除程序性细胞死亡蛋白4可以减少多囊卵巢综合征患者颗粒细胞的凋亡,说明程序性细胞死亡蛋白4参与了多囊卵巢综合征的发病机制[45]。ZHAO等[45]研究表明miR-323-3p修饰的脂肪间充质干细胞外泌体通过靶向程序性细胞死亡蛋白4抑制颗粒细胞凋亡减轻多囊卵巢综合征。此外,在多囊卵巢综合征大鼠模型中,骨髓间充质干细胞外泌体可以改善卵巢结构和激素水平[43]。总之,间充质干细胞外泌体可能是改善多囊卵巢综合征的有效途径,但仍需进一步实验探讨。
2.3.3 外泌体与宫腔粘连 宫腔粘连是由创伤、感染等因素引起的子宫内膜纤维化改变。中重度宫腔粘连复发率高,各种抗粘连治疗的远期妊娠结局不容乐观。成纤维细胞是纤维化的来源,转化生长因子刺激肌成纤维细胞诱导纤维化模型[46]。
研究表明骨髓间充质干细胞外泌体通过TGF-β1/Smad途径逆转上皮间质转化,促进受损子宫内膜修复[47]。外泌体携带的抗纤维化miRNAs可作为减轻纤维化的治疗靶点,促进宫腔粘连的预防和治疗[48]。XIAO等[49]发现骨髓间充质干细胞外泌体可通过将miR-340转移到子宫内膜间质细胞发挥抗纤维化作用,而miR-340修饰的骨髓间充质干细胞外泌体是防止宫腔粘连的一种替代方法。此外,脐带间充质干细胞外泌体以剂量依赖性的方式促进子宫内膜间质细胞的增殖,说明间充质干细胞外泌体可作为促进子宫内膜修复的潜在治疗手
段[50]。 EBRAHIM等[19]发现与未治疗的宫腔粘连大鼠相比,应用脐带间充质干细胞外泌体治疗可以减轻损伤内膜的炎症反应,进而促进受损的子宫内膜再生并逆转纤维化。ZHAO等[51]应用脂肪间充质干细胞外泌体不仅可以改善宫腔粘连大鼠受损伤内膜的形态,还提高了内膜的容受性,最终提高了大鼠的生育力。总之,间充质干细胞外泌体在宫腔粘连动物的治疗中获得了可喜的疗效,为其临床转化奠定了理论基础。
2.3.4 外泌体与生殖系统肿瘤 间充质干细胞外泌体在妇科肿瘤,尤其是卵巢癌方面,也发挥了重要的作用。研究发现脂肪间充质干细胞外泌体通过阻断细胞周期和激活线粒体介导的凋亡信号,抑制A2780和SKOV-3癌细胞的增殖、集落形成;而经RNA酶消化的外泌体不能抑制癌细胞的增殖,说明脂肪间充质干细胞外泌体通过miRNAs发挥对卵巢癌细胞的抑制作用[52]。目前,人们越来越关注利用外泌体作为miRNA和药物转移的治疗性生物载体[53]。研究人员已成功将间充质干细胞外泌体作为一种实用的策略来传递化疗药物以增强其疗效和靶向性[54],该发现进一步证实了外泌体可以作为一种新的给药途径投入到抗肿瘤治疗中。然而,对间充质干细胞外泌体在其他肿瘤相关方面(例如在肿瘤血管生成、免疫和微环境中的作用)的研究目前较少,需要进一步的研究来探索并提高间充质干细胞外泌体在肿瘤治疗中的应用水平。
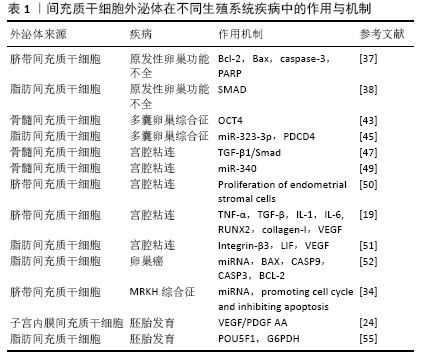
2.3.5 其他 除上述常见生殖系统疾病的诊断和治疗外,间充质干细胞外泌体在促进胚胎发育[24,55]、阴道损伤修复过程中也起着至关重要的作用[34]。以上研究表明,间充质干细胞外泌体可能是改善女性生殖健康的一种新颖、安全、有效的治疗方案,见表1。
2.4 外泌体治疗的局限性 虽然间充质干细胞外泌体在许多疾病诊断和治疗等领域发挥重要作用,但就临床转化而言,间充质干细胞外泌体在某些方面还存在一些局限性:①很多情况下间充质干细胞外泌体发挥作用的确切机制并不清楚;②外泌体在不同疾病中的有效治疗剂量尚未达成共识,相关研究也不充分;③外泌体的有效载荷(例如miRNA含量)具有动态性质,它会随着微环境变化而不断变化,然而目前尚无明确定义的miRNA谱图,也没有最佳定义的培养并重复获得临床有效的间充质干细胞外泌体的条件[56];④所涉及的实验大多是短期研究,无法显示间充质干细胞外泌体的长期疗效。
2.2 外泌体的生物学功能 外泌体表面含有各种可以维持其形态的脂类物质,如甘油二脂、胆固醇、鞘脂、磷脂等,这些脂类分子还可以作为参与各种生物学过程的信号分子[12],而且外泌体含有多种蛋白质和遗传物质,在细胞微环境中发挥重要作用[13]。下面,将全面介绍间充质干细胞外泌体在不同生物学行为中的最新研究进展。
2.2.1 抗炎和免疫调节 间充质干细胞具有减轻炎症和免疫反应的内在潜能[14]。外泌体具有与其来源细胞相似的免疫调节功能[15]。研究发现,脂肪间充质干细胞外泌体可以降低干扰素γ和转录因子的表达,上调免疫调节细胞因子的表达,降低局部炎症反应,起到免疫调节作用[16]。在体外脂肪间充质干细胞外泌体可以抑制CD4+和CD8+T细胞向效应细胞或记忆细胞表型分化;此外,脂肪间充质干细胞外泌体还通过减少干扰素γ的分泌来抑制T细胞的激活[17]。ZHAO等[18]
发现脂肪间充质干细胞外泌体可以转移到巨噬细胞中,增加M2相关精氨酸酶1和白细胞介素10的mRNA水平,诱导促炎的M1型巨噬细胞转化为抗炎的M2型巨噬细胞,并显著抑制脂多糖和干扰素γ刺激的巨噬细胞炎性反应。EBRAHIM
等[19]发现在大鼠宫腔粘连模型中骨髓间充质干细胞外泌体可以通过调节炎症反应和减少炎症细胞因子(例如白细胞介素1,白细胞介素6和肿瘤坏死因子α)的释放促进损伤子宫内膜的修复。在许多情况下,间充质干细胞外泌体的治疗作用来源于其抗炎活性。间充质干细胞外泌体含有抗炎成分,这些成分被传递到受体细胞,减轻炎症反应。利用这些特点,间充质干细胞外泌体可以应用于多种炎症性疾病和自身免疫性疾病。
2.2.2 促血管生成 血管生成在胚胎发育、生殖、组织再生修复等不同生理事件中起着至关重要的作用。间充质干细胞可以释放具有增强血管生长功能的外泌体,促进血管内皮细胞的增殖[20]。脂肪间充质干细胞外泌体携带与血管生成相关的miRNA亚类(miR-126,miR-130a,miR-132)[21-22],它们可以通过增加内皮细胞中的几种生长因子水平(例如血管内皮生长因子、表皮细胞生长因子和成纤维细胞生长因子等)来促进血管生成[23]。将间充质干细胞外泌体与小鼠胚胎共培养,结果发现间充质干细胞外泌体触发胚胎中促血管生成分子(血管内皮生长因子和血小板衍生生长因子AA)的释放,这说明间充质干细胞外泌体可以促进子宫内膜血管生成、分化和组织重塑[24]。此外EBRAHIM等[19]和SARIBAS等[25]研究表明外泌体治疗宫腔粘连大鼠的子宫内膜中血管内皮生长因子表达明显增加,说明间充质干细胞外泌体治疗可以促进子宫组织的血管化。细胞分泌外泌体的内容物及其浓度会随着所处环境的改变而变化。HAN等[26]发现脂肪间充质干细胞外泌体可以明显增强人脐静脉内皮细胞的体外血管形成能力,且低氧预处理组脂肪间充质干细胞外泌体效果更好。脂肪间充质干细胞外泌体还提高了人脐静脉内皮细胞中血管生成相关基因促血管生成素1(Ang-1)及其受体Tie-1的表达。Ang-1/Tie-1
是除VEGF/VEGFR之外另一条调控血管生成的重要信号通
路[27]。此外,与常氧处理组脂肪间充质干细胞外泌体相比,蛋白质阵列显示缺氧预处理的脂肪间充质干细胞外泌体中成纤维细胞生长因子、血管内皮生长因子、表皮细胞生长因子和单核细胞趋化蛋白等血管生成相关蛋白富集[28],这表明低氧处理的脂肪间充质干细胞外泌体具有更高的促进血管生成能力。因此,可以通过间充质干细胞的预处理调节外泌体的生物活性,进而增强间充质干细胞外泌体的治疗效果。
2.2.3 促进细胞增殖、抑制细胞凋亡 研究表明,间充质干细胞外泌体通过各种机制在不同类型细胞的增殖和迁移中发挥作用。Wnt/β-catenin信号通路在伤口愈合的增殖期起重要作用[29]。在皮肤损伤模型中,脂肪间充质干细胞外泌体可以通过激活Wnt信号通路促进角质形成细胞(HaCaT)的增殖和迁移,同时上调抗凋亡蛋白Bcl-2的表达,下调促凋亡蛋白Bax的表达,抑制细胞凋亡,从而发挥促进伤口愈合的生物学作用[30]。此外,脂肪间充质干细胞外泌体可以通过转移和调节蛋白质及miRNAs在细胞凋亡中发挥抑制作用。研究表明,在缺氧和无血清培养基诱导后,脂肪间充质干细胞外泌体可显著抑制骨细胞活性氧的过度产生,上调Bcl-2的表达,下调Bax的表达,抑制无血清诱导的骨细胞凋亡[31]。研究表明,与未处理组相比,miR-126过表达的脂肪间充质干细胞外泌体可以通过保护心肌细胞免于凋亡、炎症、纤维化和增加血管生成来防止心肌损伤,具有更强的治疗潜力[32]。在皮瓣移植模型中,H2O2预处理脂肪间充质干细胞外泌体组凋亡细胞明显较少,缺血再灌注损伤后皮瓣存活率较高[33]。此外,研究表明脐带间充质干细胞外泌体特异性miRNA可以通过促进细胞周期和抑制细胞凋亡来促进阴道上皮细胞的增殖,表明脐带间充质干细胞外泌体可能对阴道重建有治疗作用[34]。
总之,间充质干细胞外泌体可以有效转运特异性蛋白、脂质、mRNA和miRNA等多种生物活性物质,进而发挥相应的生物学功能。因此,外泌体可用作临床疾病治疗和再生医学治疗的新载体。
2.3 间充质干细胞外泌体在生殖系统相关疾病中的应用前景 间充质干细胞外泌体的作用和治疗效果已经在许多疾病中得到观察和证实。前期,研究人员只是简单地探索天然来源外泌体的基本功能,并将其应用于疾病模型,对其内容几乎没有任何修改。随着研究的深入,许多研究表明外泌体的一些特性和内容是可以被其他物质修饰的。在某些培养条件下,外泌体可以作为稳定有效的载体,装载特定的蛋白质、脂类和遗传物质,因此可以作为一种极具有治疗前景的运输载体将生物活性物质运送到靶向组织或器官[35]。生殖系统疾病是困扰广大女性的一类常见疾病。在检索数据库后,作者发现外泌体在女性生殖健康领域的研究有限。因此,文章将重点介绍近年来外泌体在女性生殖系统疾病中的研究进展及治疗前景,以提供和总结当前这方面有价值的信息。
2.3.1 外泌体与卵巢功能不全 原发性卵巢功能不全是指女性在40周岁以前因妊娠以外的原因导致闭经至少4个月,而且卵泡期血清检查至少2次出现卵泡刺激素> 25 IU/L,雌二醇< 73.2 pmol/L。过去将卵泡刺激素> 40 IU/L的患者又称为卵巢早衰,其特征是闭经、低雌激素、高促性腺激素、不孕和卵泡数量减少。目前,原发性卵巢功能不全无法逆转,尽管可以使用长期激素替代疗法缓解更年期症状,但很难防止妇女卵巢过早老化[36]。有研究表明原发性卵巢功能不全与卵巢颗粒细胞的损伤和凋亡密切相关,间充质干细胞外泌体在体外可以抑制化疗诱导的卵巢颗粒细胞凋亡,说明间充质干细胞外泌体在原发性卵巢功能不全治疗中具有积极意义[37]。
HUANG等[38]研究发现间充质干细胞外泌体可以通过调节SMAD信号途径显著减轻原发性卵巢功能不全小鼠模型的卵巢损伤;在注射间充质干细胞外泌体后,原发性卵巢功能不全小鼠4个阶段的卵泡数量显著增加,血清激素水平也恢复到正常,说明间充质干细胞外泌体通过调节SMAD信号通路改善原发性卵巢功能不全患者卵巢功能。此外,外泌体中含有大量miRNA,且这些miRNA靶向基因主要富集于PI3K和凋亡途径,与卵泡激活和卵巢功能密切相关[39]。在化疗诱导的卵巢早衰小鼠模型中,人羊膜上皮细胞来源的外泌体主要通过转移miRNAs抑制卵巢颗粒细胞凋亡,在恢复卵巢功能方面发挥了有效的作用[39]。因此,间充质干细胞外泌体具有治疗原发性卵巢功能不全和卵巢早衰的潜能,但是仍然需要进一步研究来证实和探索其可能的机制。
2.3.2 外泌体与多囊卵巢综合征 多囊卵巢综合征是导致育龄女性生殖障碍常见的疾病之一[40],其确切发病机制仍不清楚,但越来越多的证据表明胰岛素抵抗、慢性炎症和氧化应激等参与了多囊卵巢综合征的发病机制,并可能伴有亚临床心血管疾病和一些恶性病变,如子宫内膜癌[41]。研究表明,多囊卵巢综合征患者和健康人的血液、卵泡液和颗粒细胞中的miRNAs存在显著差异[42]。间充质干细胞外泌体中富集了多种miRNA,提示间充质干细胞外泌体可能具有治疗多囊卵巢综合征的潜力。多囊卵巢综合征患者体内氧化还原酶水平显著升高,而氧化还原酶水平与肥胖、高雄激素血症和慢性炎症显著相关,多囊卵巢综合征患者的氧化还原酶水平异常是源于该疾病还是其并发症仍有争议[43]。SHANG等[44]发现间充质干细胞外泌体可以减轻肥胖小鼠的脂肪组织炎症和胰岛素抵抗,对糖尿病有一定的治疗作用,说明间充质干细胞外泌体在多囊卵巢综合征并发症治疗中有积极意义。程序性细胞死亡蛋白4是凋亡过程中高表达的关键因子,在多囊卵巢综合征患者中,程序性细胞死亡蛋白4上调,而敲除程序性细胞死亡蛋白4可以减少多囊卵巢综合征患者颗粒细胞的凋亡,说明程序性细胞死亡蛋白4参与了多囊卵巢综合征的发病机制[45]。ZHAO等[45]研究表明miR-323-3p修饰的脂肪间充质干细胞外泌体通过靶向程序性细胞死亡蛋白4抑制颗粒细胞凋亡减轻多囊卵巢综合征。此外,在多囊卵巢综合征大鼠模型中,骨髓间充质干细胞外泌体可以改善卵巢结构和激素水平[43]。总之,间充质干细胞外泌体可能是改善多囊卵巢综合征的有效途径,但仍需进一步实验探讨。
2.3.3 外泌体与宫腔粘连 宫腔粘连是由创伤、感染等因素引起的子宫内膜纤维化改变。中重度宫腔粘连复发率高,各种抗粘连治疗的远期妊娠结局不容乐观。成纤维细胞是纤维化的来源,转化生长因子刺激肌成纤维细胞诱导纤维化模型[46]。
研究表明骨髓间充质干细胞外泌体通过TGF-β1/Smad途径逆转上皮间质转化,促进受损子宫内膜修复[47]。外泌体携带的抗纤维化miRNAs可作为减轻纤维化的治疗靶点,促进宫腔粘连的预防和治疗[48]。XIAO等[49]发现骨髓间充质干细胞外泌体可通过将miR-340转移到子宫内膜间质细胞发挥抗纤维化作用,而miR-340修饰的骨髓间充质干细胞外泌体是防止宫腔粘连的一种替代方法。此外,脐带间充质干细胞外泌体以剂量依赖性的方式促进子宫内膜间质细胞的增殖,说明间充质干细胞外泌体可作为促进子宫内膜修复的潜在治疗手
段[50]。 EBRAHIM等[19]发现与未治疗的宫腔粘连大鼠相比,应用脐带间充质干细胞外泌体治疗可以减轻损伤内膜的炎症反应,进而促进受损的子宫内膜再生并逆转纤维化。ZHAO等[51]应用脂肪间充质干细胞外泌体不仅可以改善宫腔粘连大鼠受损伤内膜的形态,还提高了内膜的容受性,最终提高了大鼠的生育力。总之,间充质干细胞外泌体在宫腔粘连动物的治疗中获得了可喜的疗效,为其临床转化奠定了理论基础。
2.3.4 外泌体与生殖系统肿瘤 间充质干细胞外泌体在妇科肿瘤,尤其是卵巢癌方面,也发挥了重要的作用。研究发现脂肪间充质干细胞外泌体通过阻断细胞周期和激活线粒体介导的凋亡信号,抑制A2780和SKOV-3癌细胞的增殖、集落形成;而经RNA酶消化的外泌体不能抑制癌细胞的增殖,说明脂肪间充质干细胞外泌体通过miRNAs发挥对卵巢癌细胞的抑制作用[52]。目前,人们越来越关注利用外泌体作为miRNA和药物转移的治疗性生物载体[53]。研究人员已成功将间充质干细胞外泌体作为一种实用的策略来传递化疗药物以增强其疗效和靶向性[54],该发现进一步证实了外泌体可以作为一种新的给药途径投入到抗肿瘤治疗中。然而,对间充质干细胞外泌体在其他肿瘤相关方面(例如在肿瘤血管生成、免疫和微环境中的作用)的研究目前较少,需要进一步的研究来探索并提高间充质干细胞外泌体在肿瘤治疗中的应用水平。
2.3.5 其他 除上述常见生殖系统疾病的诊断和治疗外,间充质干细胞外泌体在促进胚胎发育[24,55]、阴道损伤修复过程中也起着至关重要的作用[34]。以上研究表明,间充质干细胞外泌体可能是改善女性生殖健康的一种新颖、安全、有效的治疗方案,见表1。
2.4 外泌体治疗的局限性 虽然间充质干细胞外泌体在许多疾病诊断和治疗等领域发挥重要作用,但就临床转化而言,间充质干细胞外泌体在某些方面还存在一些局限性:①很多情况下间充质干细胞外泌体发挥作用的确切机制并不清楚;②外泌体在不同疾病中的有效治疗剂量尚未达成共识,相关研究也不充分;③外泌体的有效载荷(例如miRNA含量)具有动态性质,它会随着微环境变化而不断变化,然而目前尚无明确定义的miRNA谱图,也没有最佳定义的培养并重复获得临床有效的间充质干细胞外泌体的条件[56];④所涉及的实验大多是短期研究,无法显示间充质干细胞外泌体的长期疗效。

| [1] BHARTIYA D. Pluripotent Stem Cells in Adult Tissues: Struggling To Be Acknowledged Over Two Decades. Stem Cell Rev Rep. 2017;13(6): 713-724. [2] ARGENTATI C, MORENA F, BAZZUCCHI M, et al. Adipose Stem Cell Translational Applications: From Bench-to-Bedside. Int J Mol Sci. 2018; 19(11):3475. [3] XU S, LIU C, JI HL. Concise Review: Therapeutic Potential of the Mesenchymal Stem Cell Derived Secretome and Extracellular Vesicles for Radiation-Induced Lung Injury: Progress and Hypotheses. Stem Cells Transl Med. 2019;8(4):344-354. [4] PAN BT, JOHNSTONE RM. Fate of the transferrin receptor during maturation of sheep reticulocytes in vitro: selective externalization of the receptor. Cell. 1983;33(3):967-978. [5] JOHNSTONE RM, ADAM M, HAMMOND JR, et al. Vesicle formation during reticulocyte maturation. Association of plasma membrane activities with released vesicles (exosomes). J Biol Chem. 1987;262(19): 9412-9420. [6] MATHIVANAN S, FAHNER CJ, REID GE, et al. ExoCarta 2012: database of exosomal proteins, RNA and lipids. Nucleic Acids Res. 2012;40(Database issue):D1241-1244. [7] HONG P, YANG H, WU Y, et al. The functions and clinical application potential of exosomes derived from adipose mesenchymal stem cells: a comprehensive review. Stem Cell Res Ther. 2019;10(1):242. [8] YAO ZY, CHEN WB, SHAO SS, et al. Role of exosome-associated microRNA in diagnostic and therapeutic applications to metabolic disorders. J Zhejiang Univ Sci B. 2018;19(3):183-198. [9] LI P, KASLAN M, LEE SH, et al. Progress in Exosome Isolation Techniques. Theranostics. 2017;7(3):789-804. [10] THÉRY C, WITWER KW, AIKAWA E, et al. Minimal information for studies of extracellular vesicles 2018 (MISEV2018): a position statement of the International Society for Extracellular Vesicles and update of the MISEV2014 guidelines. J Extracell Vesicles. 2018;7(1):1535750. [11] FRANQUESA M, HOOGDUIJN MJ, RIPOLL E, et al. Update on controls for isolation and quantification methodology of extracellular vesicles derived from adipose tissue mesenchymal stem cells. Front Immunol. 2014;5:525. [12] TURCHINOVICH A, SAMATOV TR, TONEVITSKY AG, et al. Circulating miRNAs: cell-cell communication function? Front Genet. 2013;4:119. [13] KOWAL J, TKACH M, THÉRY C. Biogenesis and secretion of exosomes. Curr Opin Cell Biol. 2014;29:116-125. [14] CHANG CL, SUNG PH, CHEN KH, et al. Adipose-derived mesenchymal stem cell-derived exosomes alleviate overwhelming systemic inflammatory reaction and organ damage and improve outcome in rat sepsis syndrome. Am J Transl Res. 2018;10(4):1053-1070. [15] SEO Y, KIM HS, HONG IS. Stem Cell-Derived Extracellular Vesicles as Immunomodulatory Therapeutics. Stem Cells Int. 2019;2019:5126156. [16] MOHAMMADZADEH A, POURFATHOLLAH AA, SHAHROKHI S, et al. Immunomodulatory effects of adipose-derived mesenchymal stem cells on the gene expression of major transcription factors of T cell subsets. Int Immunopharmacol. 2014;20(2):316-321. [17] BLAZQUEZ R, SANCHEZ-MARGALLO FM, DE LA ROSA O, et al. Immunomodulatory Potential of Human Adipose Mesenchymal Stem Cells Derived Exosomes on in vitro Stimulated T Cells. Front Immunol. 2014;5:556. [18] ZHAO H, SHANG Q, PAN Z, et al. Exosomes From Adipose-Derived Stem Cells Attenuate Adipose Inflammation and Obesity Through Polarizing M2 Macrophages and Beiging in White Adipose Tissue. Diabetes. 2018; 67(2):235-247. [19] EBRAHIM N, MOSTAFA O, EL DOSOKY RE, et al. Human mesenchymal stem cell-derived extracellular vesicles/estrogen combined therapy safely ameliorates experimentally induced intrauterine adhesions in a female rat model. Stem Cell Res Ther. 2018;9(1):175. [20] LOPATINA T, BRUNO S, TETTA C, et al. Platelet-derived growth factor regulates the secretion of extracellular vesicles by adipose mesenchymal stem cells and enhances their angiogenic potential. Cell Commun Signal. 2014;12:26. [21] ZHU LL, HUANG X, YU W, et al. Transplantation of adipose tissue-derived stem cell-derived exosomes ameliorates erectile function in diabetic rats. Andrologia. 2018;50(2):e12871. [22] YANG WZ, YANG J, XUE LP, et al. MiR-126 overexpression inhibits high glucose-induced migration and tube formation of rhesus macaque choroid-retinal endothelial cells by obstructing VEGFA and PIK3R2. J Diabetes Complications. 2017;31(4):653-663. [23] WANG S, OLSON EN. AngiomiRs--key regulators of angiogenesis. Curr Opin Genet Dev. 2009;19(3):205-211. [24] BLÁZQUEZ R, SÁNCHEZ-MARGALLO FM, ÁLVAREZ V, et al. Murine embryos exposed to human endometrial MSCs-derived extracellular vesicles exhibit higher VEGF/PDGF AA release, increased blastomere count and hatching rates. PLoS One. 2018;13(4):e0196080. [25] SARIBAS GS, OZOGUL C, TIRYAKI M, et al. Effects of uterus derived mesenchymal stem cells and their exosomes on asherman’s syndrome. Acta Histochem. 2020;122(1):151465. [26] HAN YD, BAI Y, YAN XL, et al. Co-transplantation of exosomes derived from hypoxia-preconditioned adipose mesenchymal stem cells promotes neovascularization and graft survival in fat grafting. Biochem Biophys Res Commun. 2018;497(1):305-312. [27] ZHANG J, CHEN C, HU B, et al. Exosomes Derived from Human Endothelial Progenitor Cells Accelerate Cutaneous Wound Healing by Promoting Angiogenesis Through Erk1/2 Signaling. Int J Biol Sci. 2016;12(12):1472-1487. [28] HAN Y, REN J, BAI Y, et al. Exosomes from hypoxia-treated human adipose-derived mesenchymal stem cells enhance angiogenesis through VEGF/VEGF-R. Int J Biochem Cell Biol. 2019;109:59-68. [29] CHEON SS, WEI Q, GURUNG A, et al. Beta-catenin regulates wound size and mediates the effect of TGF-beta in cutaneous healing. FASEB J. 2006;20(6):692-701. [30] MA T, FU B, YANG X, et al. Adipose mesenchymal stem cell-derived exosomes promote cell proliferation, migration, and inhibit cell apoptosis via Wnt/β-catenin signaling in cutaneous wound healing. J Cell Biochem. 2019;120(6):10847-10854. [31] REN L, SONG ZJ, CAI QW, et al. Adipose mesenchymal stem cell-derived exosomes ameliorate hypoxia/serum deprivation-induced osteocyte apoptosis and osteocyte-mediated osteoclastogenesis in vitro. Biochem Biophys Res Commun. 2019;508(1):138-144. [32] LUO Q, GUO D, LIU G, et al. Exosomes from MiR-126-Overexpressing Adscs Are Therapeutic in Relieving Acute Myocardial Ischaemic Injury. Cell Physiol Biochem. 2017;44(6):2105-2116. [33] BAI Y, HAN YD, YAN XL, et al. Adipose mesenchymal stem cell-derived exosomes stimulated by hydrogen peroxide enhanced skin flap recovery in ischemia-reperfusion injury. Biochem Biophys Res Commun. 2018;500(2):310-317. [34] ZHU Z, ZHANG Y, ZHANG Y, et al. Exosomes derived from human umbilical cord mesenchymal stem cells accelerate growth of VK2 vaginal epithelial cells through MicroRNAs in vitro. Hum Reprod. 2019;34(2):248-260. [35] BUNGGULAWA EJ, WANG W, YIN T, et al. Recent advancements in the use of exosomes as drug delivery systems. J Nanobiotechnology. 2018;16(1):81. [36] US PREVENTIVE SERVICES TASK FORCE, GROSSMAN DC, CURRY SJ, et al. Hormone Therapy for the Primary Prevention of Chronic Conditions in Postmenopausal Women: US Preventive Services Task Force Recommendation Statement. JAMA. 2017;318(22):2224-2233. [37] SUN L, LI D, SONG K, et al. Exosomes derived from human umbilical cord mesenchymal stem cells protect against cisplatin-induced ovarian granulosa cell stress and apoptosis in vitro. Sci Rep. 2017;7(1):2552. [38] HUANG B, LU J, DING C, et al. Exosomes derived from human adipose mesenchymal stem cells improve ovary function of premature ovarian insufficiency by targeting SMAD. Stem Cell Res Ther. 2018;9(1):216. [39] ZHANG Q, SUN J, HUANG Y, et al. Human Amniotic Epithelial Cell-Derived Exosomes Restore Ovarian Function by Transferring MicroRNAs against Apoptosis. Mol Ther Nucleic Acids. 2019;16:407-418. [40] AZZIZ R, CARMINA E, CHEN Z, et al. Polycystic ovary syndrome. Nat Rev Dis Primers. 2016;2:16057. [41] ILIE IR. Advances in PCOS Pathogenesis and Progression-Mitochondrial Mutations and Dysfunction. Adv Clin Chem. 2018;86:127-155. [42] SØRENSEN AE, WISSING ML, SALÖ S, et al. MicroRNAs Related to Polycystic Ovary Syndrome (PCOS). Genes (Basel). 2014;5(3):684-708. [43] FARUK EM, EL-DESOKY RE, AL-SHAZLY AM, et al. Does Exosomes Derived Bone Marrow Mesenchymal Stem Cells Restore Ovarian Function by Promoting Stem Cell Survival on Experimentally Induced Polycystic Ovary in Adult Female Albino Rats? (Histological and Immunohistochemical Study). Stem Cell Res Ther. 2018;8(12):1000442. [44] SHANG Q, BAI Y, WANG G, et al. Delivery of Adipose-Derived Stem Cells Attenuates Adipose Tissue Inflammation and Insulin Resistance in Obese Mice Through Remodeling Macrophage Phenotypes. Stem Cells Dev. 2015;24(17):2052-2064. [45] ZHAO Y, TAO M, WEI M, et al. Mesenchymal stem cells derived exosomal miR-323-3p promotes proliferation and inhibits apoptosis of cumulus cells in polycystic ovary syndrome (PCOS). Artif Cells Nanomed Biotechnol. 2019;47(1):3804-3813. [46] AKHURST RJ, HATA A. Targeting the TGFβ signalling pathway in disease. Nat Rev Drug Discov. 2012;11(10):790-811. [47] YAO Y, CHEN R, WANG G, et al. Exosomes derived from mesenchymal stem cells reverse EMT via TGF-β1/Smad pathway and promote repair of damaged endometrium. Stem Cell Res Ther. 2019;10(1):225. [48] NAKAMURA K, JINNIN M, HARADA M, et al. Altered expression of CD63 and exosomes in scleroderma dermal fibroblasts. J Dermatol Sci. 2016;84(1):30-39. [49] XIAO B, ZHU Y, HUANG J, et al. Exosomal transfer of bone marrow mesenchymal stem cell-derived miR-340 attenuates endometrial fibrosis. Biol Open. 2019;8(5):bio039958. [50] LV CX, DUAN H, WANG S, et al. Exosomes Derived from Human Umbilical Cord Mesenchymal Stem Cells Promote Proliferation of Allogeneic Endometrial Stromal Cells. Reprod Sci. 2020;27(6): 1372-1381. [51] ZHAO S, QI W, ZHENG J, et al. Exosomes Derived from Adipose Mesenchymal Stem Cells Restore Functional Endometrium in a Rat Model of Intrauterine Adhesions. Reprod Sci. 2020;27(6):1266-1275. [52] REZA AMMT, CHOI YJ, YASUDA H, et al. Human adipose mesenchymal stem cell-derived exosomal-miRNAs are critical factors for inducing anti-proliferation signalling to A2780 and SKOV-3 ovarian cancer cells. Sci Rep. 2016;6:38498. [53] HANNAFON BN, DING WQ. Intercellular communication by exosome-derived microRNAs in cancer. Int J Mol Sci. 2013;14(7):14240-14269. [54] MELZER C, REHN V, YANG Y, et al. Taxol-Loaded MSC-Derived Exosomes Provide a Therapeutic Vehicle to Target Metastatic Breast Cancer and Other Carcinoma Cells. Cancers (Basel). 2019;11(6):798. [55] MIRANDA MS, NASCIMENTO HS, COSTA MP, et al. Increasing of blastocyst rate and gene expression in co-culture of bovine embryos with adult adipose tissue-derived mesenchymal stem cells. J Assist Reprod Genet. 2016;33(10):1395-1403. [56] BELLIN G, GARDIN C, FERRONI L, et al. Exosome in Cardiovascular Diseases: A Complex World Full of Hope. Cells. 2019;8(2):166. |
| [1] | 林清凡, 解一新, 陈婉清, 叶振忠, 陈幼芳. 人胎盘源间充质干细胞条件培养液可上调缺氧状态下BeWo细胞活力和紧密连接因子的表达[J]. 中国组织工程研究, 2021, 25(在线): 4970-4975. |
| [2] | 蒲 锐, 陈子扬, 袁凌燕. 不同细胞来源外泌体保护心脏的特点与效应[J]. 中国组织工程研究, 2021, 25(在线): 1-. |
| [3] | 张 超, 吕 欣. 髋臼骨折固定后的异位骨化:危险因素、预防及其治疗进展[J]. 中国组织工程研究, 2021, 25(9): 1434-1439. |
| [4] | 周继辉, 李新志, 周 游, 黄 卫, 陈文瑶. 髌骨骨折修复内植物选择的多重问题[J]. 中国组织工程研究, 2021, 25(9): 1440-1445. |
| [5] | 王德斌, 毕郑刚. 尺骨鹰嘴骨折-脱位解剖力学、损伤特点、固定修复及3D技术应用的相关问题[J]. 中国组织工程研究, 2021, 25(9): 1446-1451. |
| [6] | 姬志祥, 蓝常贡. 尿酸盐转运蛋白在痛风中的多态性和治疗相关性[J]. 中国组织工程研究, 2021, 25(8): 1290-1298. |
| [7] | 袁 美, 张新新, 郭祎莎, 毕 霞. 循环microRNA在血管性认知障碍诊断中的应用[J]. 中国组织工程研究, 2021, 25(8): 1299-1304. |
| [8] | 张秀梅, 翟运开, 赵 杰, 赵 萌. 类器官模型国内外数据库近10年文献研究热点分析[J]. 中国组织工程研究, 2021, 25(8): 1249-1255. |
| [9] | 王正东, 黄 娜, 陈婧娴, 郑作兵, 胡鑫宇, 李 梅, 苏 晓, 苏学森, 颜 南. 丁酸钠抑制氟中毒可诱导小胶质细胞活化及炎症因子表达增多[J]. 中国组织工程研究, 2021, 25(7): 1075-1080. |
| [10] | 汪显耀, 关亚琳, 刘忠山. 提高间充质干细胞治疗难愈性创面的策略[J]. 中国组织工程研究, 2021, 25(7): 1081-1087. |
| [11] | 万 然, 史 旭, 刘京松, 王岩松. 间充质干细胞分泌组治疗脊髓损伤的研究进展[J]. 中国组织工程研究, 2021, 25(7): 1088-1095. |
| [12] | 廖成成, 安家兴, 谭张雪, 王 倩, 刘建国. 口腔鳞状细胞癌干细胞的治疗靶点及应用前景[J]. 中国组织工程研究, 2021, 25(7): 1096-1103. |
| [13] | 赵 敏, 冯柳祥, 陈 垚, 顾 霞, 王平义, 李一梅, 李文华. 低氧环境下外泌体可作为疾病的标志物[J]. 中国组织工程研究, 2021, 25(7): 1104-1108. |
| [14] | 谢文佳, 夏天娇, 周卿云, 刘羽佳, 顾小萍. 小胶质细胞介导神经元损伤在神经退行性疾病中的作用[J]. 中国组织工程研究, 2021, 25(7): 1109-1115. |
| [15] | 李珊珊, 郭笑霄, 尤 冉, 杨秀芬, 赵 露, 陈 曦, 王艳玲. 感光细胞替代治疗视网膜变性疾病[J]. 中国组织工程研究, 2021, 25(7): 1116-1121. |
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
adhesions),(mesenchymal stem cells) AND (exosome) AND (endometrium),(mesenchymal stem cells) AND (exosome) AND (Asherman’s syndrome),(mesenchymal stem cells) AND
(exosome) AND (ovarian cancer),(mesenchymal stem cells) AND (exosome) AND (cervical cancer),(mesenchymal stem cells) AND (exosome) AND (endometrial carcinoma),
(mesenchymal stem cells) AND (exosome) AND (embryo)”。中文检索词为“(间充质干细胞) AND (外泌体) AND (卵巢早衰),(间充质干细胞) AND (外泌体) AND (多囊卵巢综合征),(间充质干细胞) AND (外泌体) AND (宫腔粘连),(间充质干细胞) AND (外泌体) AND (卵巢癌),(间充质干细胞) AND (外泌体) AND (宫颈癌),(间充质干细胞) AND (外泌体) AND (子宫内膜癌),(间充质干细胞) AND (外泌体) AND (胚胎)”。检索的文献时间范围为2000至2020年。重点检索时间范围为近5年内。
1.2 入选标准 筛选文献,去除重复文献,选择与研究目的和研究内容紧密联系的文献。
1.3 质量评估 由2人进行信息情报检索,选取56篇相关文献进行归纳整理。
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程

文题释义:#br# 外泌体:是一种直径为30-150 nm的小囊泡,包含有多种蛋白质和遗传物质,外泌体可以由几乎所有类型哺乳动物细胞分泌,并且广泛分布在各种体液中,能够通过细胞间的传递发挥重要作用,在组织修复、疾病的诊断与治疗领域有重要的前景。#br# 间充质干细胞:来源于发育早期的中胚层,属于多能干细胞。间充质干细胞能够分化成不同的细胞系,分泌细胞因子和细胞外囊泡,在免疫调节、血管生成、伤口愈合和组织再生等方面发挥作用。#br# 背景:间充质干细胞是再生医学领域最常用的细胞类型之一。近年来研究发现,间充质干细胞来源外泌体在某些生殖系统疾病中发挥重要作用,并且逐渐成为生殖领域研究的热点。#br# 目的:综述间充质干细胞来源外泌体在卵巢早衰、多囊卵巢综合征、宫腔粘连和常见生殖系统肿瘤等疾病中的研究进展,并对间充质干细胞来源外泌体在未来的应用与研究进行了探讨。#br# 方法:在PubMed和CNKI数据库中进行相关文献检索,关键词为“mesenchymal stem cells,exosome,premature ovarian insufficiency,premature ovarian failure,polycystic ovary syndrome,intrauterine adhesions,endometrium,Asherman’s syndrome,ovarian cancer,cervical cancer,endometrial carcinoma,embryo”及“间充质干细胞,外泌体,原发性卵巢功能不全,卵巢早衰,多囊卵巢综合征,宫腔粘连,卵巢癌,宫颈癌,子宫内膜癌,胚胎”,纳入56篇文献进行综述。#br# 结果与结论:间充质干细胞来源外泌体不仅可以作为某些生殖系统疾病的治疗载体,更有可能成为研究疾病发生机制的重要靶点。间充质干细胞来源外泌体有望成为一种新兴的“无细胞”疗法用于生殖系统疾病的治疗。#br# https://orcid.org/0000-0002-4609-1222(黄向华)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||