中国组织工程研究 ›› 2018, Vol. 22 ›› Issue (28): 4440-4446.doi: 10.3969/j.issn.2095-4344.0193
• 骨组织构建 bone tissue construction • 上一篇 下一篇
骨形态发生蛋白2联合突变型低氧诱导因子1α修复激素性股骨头缺血性坏死
胡 亮1,王军海1,王志烈1,谢金元1,陈 登1,丁 凡2
- 荆门市第一人民医院,1关节外科,2创伤手足外科,湖北省荆门市 448000
Combination of bone morphogenetic protein 2 and mutant hypoxia-inducible factor 1α alpha repairs steroid-induced avascular necrosis of the femoral head
Hu Liang1, Wang Jun-hai1, Wang Zhi-lie1, Xie Jin-yuan1, Chen Deng1, Ding Fan2
- 1Department of Joint Surgery, 2Department of Traumatic Hand and Foot Surgery, Jingmen First People’s Hospital, Jingmen 448000, Hubei Province, China
摘要:
文章快速阅读:
.jpg)
.jpg)
文题释义:
低氧诱导因子1:是一种具有很强诱导新生血管能力的蛋白质,属碱性螺旋环螺旋蛋白家族,是一种在低氧/缺氧条件下对哺乳动物和人体细胞产生适应性反应的重要转录因子,是由α和β亚基的组合因子,其在缺氧条件时表达非常稳定,影响着人体中许多的病理生理过程。
突变型低氧诱导因子1α(HIF1αmu):低氧诱导因子1α在常氧条件时5 min便开始降解变性,这与低氧诱导因子1α在常氧条件下的氧依赖降解区Pro402和Pro564的化学结构发生羟基化有联系,作者在条件限定在突变其Pro564为丙氨酸(Ala)情况下,常氧状态时采取分子生物学技术创建可展现出重组双基因突变型低氧诱导因子1α的真核表达载体即pShut-tle2-HIF1α-Ala402-Ala564,记为HIF1αmu,使其在低氧和常氧条件均可高标准发挥HIF1α的作用。
摘要
背景:骨形态发生蛋白2是目前发现的唯一的一种可单独诱导骨形成的生长因子,但是研究发现骨形态发生蛋白2单一基因的促血管生成作用较弱,无法在新生骨组织处产生足量的毛细血管,所以在诱导骨形成过程中还需要与其他诱导因子协同作用。低氧诱导因子1α在促进新生血管的形成方面有重要作用。
目的:观察腺病毒介导的人骨形态发生蛋白2联合突变型低氧诱导因子1α(Ad-BMP-2-IRES-HIF-1αmu)转染骨髓间充质干细胞对激素性股骨头缺血性坏死的修复作用。
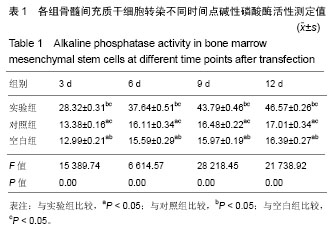
方法:①转染Ad-BMP-2-IRES-HIF-1αmu到骨髓间充质干细胞,检测碱性磷酸酶活性、钙结节茜素红染色检测其成骨能力;②建立激素性股骨头缺血性坏死兔模型,随机分为3组:实验组股骨坏死部位移植转染Ad-BMP-2-IRES-HIF-1αmu的骨髓间充质干细胞;对照组移植未转染的骨髓间充质干细胞;空白组移植细胞培养液。移植8周后,Westen blot法检测骨形态发生蛋白2和低氧诱导因子1α蛋白表达;苏木精-伊红染色组织学观察股骨头缺血性坏死修复情况;墨汁灌注透明切片血管形态学观察股骨头缺损区域血管生成情况。
结果与结论:①转染Ad-BMP-2-IRES-HIF-1αmu的骨髓间充质干细胞的碱性磷酸酶活性和钙结节数量均高于未转染的细胞,说明转染Ad-BMP-2-IRES-HIF-1αmu能促进骨髓间充质干细胞的成骨分化;②实验组骨形态发生蛋白2和低氧诱导因子1α蛋白表达高于对照组与空白组(P < 0.05);移植8周后,实验组缺损区周边观察到明显的成骨反应,与对照组及空白组相比,实验组空骨陷窝率低(P < 0.05),骨小梁面积百分比高(P < 0.05);墨汁灌注实验显示:实验组出现血管化现象,并出现骨陷窝结构,血管间有清晰的连通脉络相互间构成网络,股骨头下血管分布及血管网的形成基本正常,实验组墨汁灌注血管面积为114.22±3.78,高于对照组(63.78±2.61)和空白组(21.39±3.52),差异有显著性意义(P < 0.05);③提示:骨形态发生蛋白2联合突变型低氧诱导因子1α可以促进激素性股骨头缺血性坏死的修复。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID: 0000-0003-4580-4953(胡亮)
中图分类号:
.jpg)