中国组织工程研究 ›› 2019, Vol. 23 ›› Issue (31): 5005-5009.doi: 10.3969/j.issn.2095-4344.1464
• 组织构建实验造模 experimental modeling in tissue construction • 上一篇 下一篇
SD大鼠脊柱侧凸模型构建及凸凹方向应力对骨结构发育的影响
王滋润,肖成伟,胡 豇
- (四川省医学科学院,四川省人民医院骨科,四川省成都市 610072
Construction of SD rat scoliosis model and the effect of asymmetric tension on bone structure development
Wang Zirun, Xiao Chengwei, Hu Jiang
- (Department of Orthopedics, Sichuan Academy of Medical Sciences & Sichuan Provincial People’s Hospital, Chengdu 610072, Sichuan Province, China)
摘要:
文章快速阅读:
.jpg) 文题释义:
脊柱侧凸:是指脊柱在冠状面上的侧向弯曲,根据侧卧时是否可以恢复脊柱中立位分为功能性脊柱侧凸与结构性脊柱侧凸,功能性脊柱侧凸往往是由于姿势不良所致,可以通过姿势矫正自行恢复;结构性脊柱侧凸不可自行恢复,必要时采取治疗手段。一般认为,脊髓相对缩短或脊柱生长过快是导致脊柱侧凸的主要病因。
不对称张力:根据Huter-Volkmann定律,脊柱侧弯一旦发生,凹侧生长板受到的压应力大于凸侧,则会出现凸侧部分生长板活性更高,成骨能力更强,使侧弯进行性加重,这种力可能与脊柱侧凸发展形成恶性循环。
文题释义:
脊柱侧凸:是指脊柱在冠状面上的侧向弯曲,根据侧卧时是否可以恢复脊柱中立位分为功能性脊柱侧凸与结构性脊柱侧凸,功能性脊柱侧凸往往是由于姿势不良所致,可以通过姿势矫正自行恢复;结构性脊柱侧凸不可自行恢复,必要时采取治疗手段。一般认为,脊髓相对缩短或脊柱生长过快是导致脊柱侧凸的主要病因。
不对称张力:根据Huter-Volkmann定律,脊柱侧弯一旦发生,凹侧生长板受到的压应力大于凸侧,则会出现凸侧部分生长板活性更高,成骨能力更强,使侧弯进行性加重,这种力可能与脊柱侧凸发展形成恶性循环。
.jpg) 文题释义:
脊柱侧凸:是指脊柱在冠状面上的侧向弯曲,根据侧卧时是否可以恢复脊柱中立位分为功能性脊柱侧凸与结构性脊柱侧凸,功能性脊柱侧凸往往是由于姿势不良所致,可以通过姿势矫正自行恢复;结构性脊柱侧凸不可自行恢复,必要时采取治疗手段。一般认为,脊髓相对缩短或脊柱生长过快是导致脊柱侧凸的主要病因。
不对称张力:根据Huter-Volkmann定律,脊柱侧弯一旦发生,凹侧生长板受到的压应力大于凸侧,则会出现凸侧部分生长板活性更高,成骨能力更强,使侧弯进行性加重,这种力可能与脊柱侧凸发展形成恶性循环。
文题释义:
脊柱侧凸:是指脊柱在冠状面上的侧向弯曲,根据侧卧时是否可以恢复脊柱中立位分为功能性脊柱侧凸与结构性脊柱侧凸,功能性脊柱侧凸往往是由于姿势不良所致,可以通过姿势矫正自行恢复;结构性脊柱侧凸不可自行恢复,必要时采取治疗手段。一般认为,脊髓相对缩短或脊柱生长过快是导致脊柱侧凸的主要病因。
不对称张力:根据Huter-Volkmann定律,脊柱侧弯一旦发生,凹侧生长板受到的压应力大于凸侧,则会出现凸侧部分生长板活性更高,成骨能力更强,使侧弯进行性加重,这种力可能与脊柱侧凸发展形成恶性循环。摘要
背景:脊柱侧凸是一种发生于脊柱的三维复杂畸形,研究发现聚集蛋白聚糖、Ⅱ型胶原蛋白、Sox9、血管内皮生长因子蛋白等分子机制参与了脊柱侧凸病程,并可能发挥着与力学机制相似的不良作用,但目前缺少对脊柱侧凸发生发展机制的实验性研究。
目的:构建SD大鼠脊柱侧凸模型,并探讨凸凹方向应力对骨结构发育的影响。
方法:选取6只断乳前SD大鼠进行肩关节离断及鼠尾截断,高笼喂养3个月后进行X射线摄片。采用Mimics软件进行脊柱三维重建,分析不对称张力分布。采用μCT扫描检测骨小梁结构。麻醉处死大鼠后,提取凹侧及凸侧椎体骺软骨,检测聚集蛋白聚糖、Ⅱ型胶原蛋白、Sox9、血管内皮生长因子蛋白的表达水平。
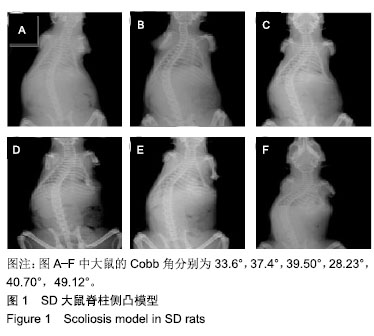
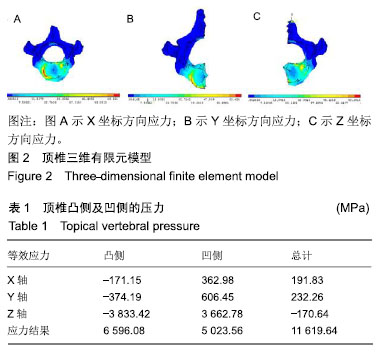
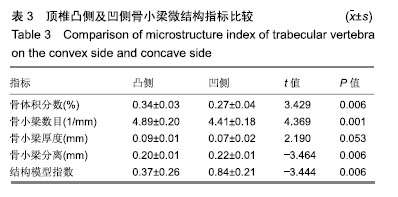
结果与结论:①6只SD大鼠均成功造模,均出现明显的后凸及左侧胸廓畸形;②应力结果显示,椎体承受的应力不对称,凸侧垂直方向的应力显著高于凹侧;③Western-Blot检测结果显示,凸侧的聚集蛋白聚糖、Ⅱ型胶原蛋白、Sox9、血管内皮生长因子蛋白的表达水平显著高于凹侧;且相应的凸侧积分吸光度值也显著增高,差异均有显著性意义(P < 0.05);④凸、凹两侧的骨小梁微结构存在显著的不对称性。与凹侧相比,凸侧的骨体积分数、骨小梁数目显著增高(P < 0.05),而骨小梁分离、结构模型指数明显降低(P < 0.05);⑤结果表明,凸凹方向的不对称应力可能通过影响相关蛋白表达及骨小梁结构的变化,促进脊柱侧凸的发生发展。
中图分类号:

.jpg) 文题释义:
脊柱侧凸:是指脊柱在冠状面上的侧向弯曲,根据侧卧时是否可以恢复脊柱中立位分为功能性脊柱侧凸与结构性脊柱侧凸,功能性脊柱侧凸往往是由于姿势不良所致,可以通过姿势矫正自行恢复;结构性脊柱侧凸不可自行恢复,必要时采取治疗手段。一般认为,脊髓相对缩短或脊柱生长过快是导致脊柱侧凸的主要病因。
不对称张力:根据Huter-Volkmann定律,脊柱侧弯一旦发生,凹侧生长板受到的压应力大于凸侧,则会出现凸侧部分生长板活性更高,成骨能力更强,使侧弯进行性加重,这种力可能与脊柱侧凸发展形成恶性循环。
文题释义:
脊柱侧凸:是指脊柱在冠状面上的侧向弯曲,根据侧卧时是否可以恢复脊柱中立位分为功能性脊柱侧凸与结构性脊柱侧凸,功能性脊柱侧凸往往是由于姿势不良所致,可以通过姿势矫正自行恢复;结构性脊柱侧凸不可自行恢复,必要时采取治疗手段。一般认为,脊髓相对缩短或脊柱生长过快是导致脊柱侧凸的主要病因。
不对称张力:根据Huter-Volkmann定律,脊柱侧弯一旦发生,凹侧生长板受到的压应力大于凸侧,则会出现凸侧部分生长板活性更高,成骨能力更强,使侧弯进行性加重,这种力可能与脊柱侧凸发展形成恶性循环。