中国组织工程研究 ›› 2019, Vol. 23 ›› Issue (7): 1090-1096.doi: 10.3969/j.issn.2095-4344.1066
• 组织构建细胞学实验 cytology experiments in tissue construction • 上一篇 下一篇
人参皂苷Rg1对氧糖剥夺/复氧复糖损伤PC12细胞的保护机制
叶劲涛1,李锋涛1,宋焕瑾1,薛建利1,林 磊2,程 斌1
- (1西安交通大学医学院第二附属医院骨科,陕西省西安市 710004;2汉中市中心医院骨科,陕西省汉中市 723000)
Ginsenoside Rg1 protects against oxygen-glucose deprivation/reperfusion injury in PC12 cells
Ye Jintao1, Li Fengtao1, Song Huanjin1, Xue Jianli1, Lin Lei2, Cheng Bin1
- (1Department of Orthopedics, Second Affiliated Hospital of Xi’an Jiaotong University Medical School, Xi’an 710004, Shaanxi Province, China; 2Department of Orthopedics, Hanzhong Central University, Hanzhong 723000, Shaanxi Province, China)
摘要:
文章快速阅读:
.jpg) 文题释义:
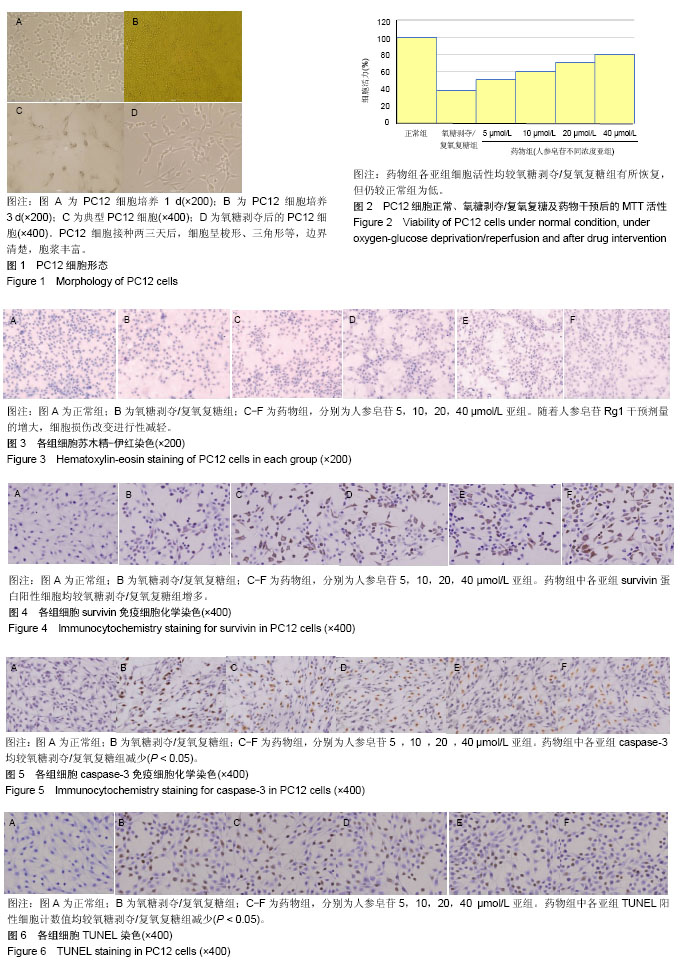
缺血再灌注损伤:缺血一定时间恢复血液供应后,其功能不但未能恢复,却出现了更加严重的功能障碍,称为缺血/再灌注损伤,其机制较为复杂,主要与细胞凋亡、自由基过度形成、兴奋性氨基酸毒性作用、细胞内钙超载、炎性反应、线粒体损伤等多种机制有关。在体外模拟神经缺血再灌注损伤时,常使用大鼠肾上腺嗜铬细胞瘤细胞,因其具有:①胞体圆、明亮,可迅速增殖,生长速度较快,接种两三天后,即可在倒置显微镜下看到细胞的贴壁生长;②通过神经生长因子诱导,PC12细胞可以长出大量轴突,最长的轴突超过 500 μm,具有神经元的形态,并且表现出多种神经细胞的生理特性。
存活素(survivin):是凋亡蛋白抑制因子家族中最小的成员,包括142个氨基酸,其功能型为同型二聚体。在细胞中呈周期依赖性表达,与有丝分裂期纺锤体微管相互作用,调节G2/M期,并可直接抑制caspase-3和caspase-7的活性。在肿瘤发生发展中,存活素与肿瘤细胞的凋亡负相关,与细胞增殖活性和血管生成正相关。在缺血/再灌注中考虑其通过直接调控caspase家族参与凋亡,或者通过介导血管生成参与其中。
文题释义:
缺血再灌注损伤:缺血一定时间恢复血液供应后,其功能不但未能恢复,却出现了更加严重的功能障碍,称为缺血/再灌注损伤,其机制较为复杂,主要与细胞凋亡、自由基过度形成、兴奋性氨基酸毒性作用、细胞内钙超载、炎性反应、线粒体损伤等多种机制有关。在体外模拟神经缺血再灌注损伤时,常使用大鼠肾上腺嗜铬细胞瘤细胞,因其具有:①胞体圆、明亮,可迅速增殖,生长速度较快,接种两三天后,即可在倒置显微镜下看到细胞的贴壁生长;②通过神经生长因子诱导,PC12细胞可以长出大量轴突,最长的轴突超过 500 μm,具有神经元的形态,并且表现出多种神经细胞的生理特性。
存活素(survivin):是凋亡蛋白抑制因子家族中最小的成员,包括142个氨基酸,其功能型为同型二聚体。在细胞中呈周期依赖性表达,与有丝分裂期纺锤体微管相互作用,调节G2/M期,并可直接抑制caspase-3和caspase-7的活性。在肿瘤发生发展中,存活素与肿瘤细胞的凋亡负相关,与细胞增殖活性和血管生成正相关。在缺血/再灌注中考虑其通过直接调控caspase家族参与凋亡,或者通过介导血管生成参与其中。
.jpg) 文题释义:
缺血再灌注损伤:缺血一定时间恢复血液供应后,其功能不但未能恢复,却出现了更加严重的功能障碍,称为缺血/再灌注损伤,其机制较为复杂,主要与细胞凋亡、自由基过度形成、兴奋性氨基酸毒性作用、细胞内钙超载、炎性反应、线粒体损伤等多种机制有关。在体外模拟神经缺血再灌注损伤时,常使用大鼠肾上腺嗜铬细胞瘤细胞,因其具有:①胞体圆、明亮,可迅速增殖,生长速度较快,接种两三天后,即可在倒置显微镜下看到细胞的贴壁生长;②通过神经生长因子诱导,PC12细胞可以长出大量轴突,最长的轴突超过 500 μm,具有神经元的形态,并且表现出多种神经细胞的生理特性。
存活素(survivin):是凋亡蛋白抑制因子家族中最小的成员,包括142个氨基酸,其功能型为同型二聚体。在细胞中呈周期依赖性表达,与有丝分裂期纺锤体微管相互作用,调节G2/M期,并可直接抑制caspase-3和caspase-7的活性。在肿瘤发生发展中,存活素与肿瘤细胞的凋亡负相关,与细胞增殖活性和血管生成正相关。在缺血/再灌注中考虑其通过直接调控caspase家族参与凋亡,或者通过介导血管生成参与其中。
文题释义:
缺血再灌注损伤:缺血一定时间恢复血液供应后,其功能不但未能恢复,却出现了更加严重的功能障碍,称为缺血/再灌注损伤,其机制较为复杂,主要与细胞凋亡、自由基过度形成、兴奋性氨基酸毒性作用、细胞内钙超载、炎性反应、线粒体损伤等多种机制有关。在体外模拟神经缺血再灌注损伤时,常使用大鼠肾上腺嗜铬细胞瘤细胞,因其具有:①胞体圆、明亮,可迅速增殖,生长速度较快,接种两三天后,即可在倒置显微镜下看到细胞的贴壁生长;②通过神经生长因子诱导,PC12细胞可以长出大量轴突,最长的轴突超过 500 μm,具有神经元的形态,并且表现出多种神经细胞的生理特性。
存活素(survivin):是凋亡蛋白抑制因子家族中最小的成员,包括142个氨基酸,其功能型为同型二聚体。在细胞中呈周期依赖性表达,与有丝分裂期纺锤体微管相互作用,调节G2/M期,并可直接抑制caspase-3和caspase-7的活性。在肿瘤发生发展中,存活素与肿瘤细胞的凋亡负相关,与细胞增殖活性和血管生成正相关。在缺血/再灌注中考虑其通过直接调控caspase家族参与凋亡,或者通过介导血管生成参与其中。摘要
背景:人参皂苷具有抗肿瘤、抗氧化、抗疲劳、抗衰老、降血脂、增强记忆力、提高免疫力等作用,其中Rb1和Rg1是人参皂苷的最主要的活性成分。但人参皂苷Rg1对氧糖剥夺诱导的PC12细胞凋亡是否也有保护作用,尚不清楚。
目的:观察人参皂苷Rg1预处理对于PC12细胞氧糖剥夺/复氧复糖模型中PC12细胞活力、survivin及caspase-3表达和细胞凋亡的影响。
方法:采用构建的PC12细胞氧糖剥夺/复氧复糖模型,并使用5,10,20,40 μmol/L的人参皂苷Rg1对其进行预处理,以正常细胞做对照。通过MTT法检测细胞活性,通过免疫细胞化学技术检测survivin及caspase-3蛋白,通过TUNEL法检测细胞凋亡。
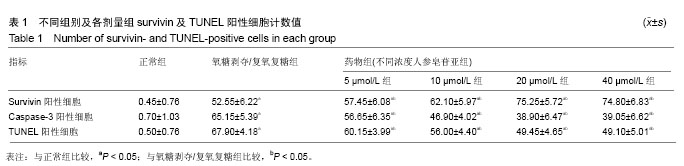
结果与结论:①细胞活力检测氧糖剥夺/复氧复糖组细胞活性明显下降(P < 0.05),人参皂苷Rg1干预后药物组各亚组细胞活性均较氧糖剥夺/复氧复糖组有所恢复,但仍较正常组为低(P < 0.05);②人参皂苷Rg1干预使survivin阳性细胞增多,caspase-3阳性细胞和TUNEL阳性细胞计数值减少;③神经元凋亡出现与人参皂苷Rg1诱导的survivin成负相关,与caspase-3成正相关。④结果说明,人参皂苷Rg1对于PC12细胞氧糖剥夺/复氧复糖处理后的survivin蛋白表达具有促进作用,并通过促进survivin蛋白的表达来对抗caspase-3的表达,从而抑制细胞凋亡,且该作用具有剂量依赖关系。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID: 0000-0003-1572-627X(叶劲涛)
中图分类号:
.jpg) 文题释义:
缺血再灌注损伤:缺血一定时间恢复血液供应后,其功能不但未能恢复,却出现了更加严重的功能障碍,称为缺血/再灌注损伤,其机制较为复杂,主要与细胞凋亡、自由基过度形成、兴奋性氨基酸毒性作用、细胞内钙超载、炎性反应、线粒体损伤等多种机制有关。在体外模拟神经缺血再灌注损伤时,常使用大鼠肾上腺嗜铬细胞瘤细胞,因其具有:①胞体圆、明亮,可迅速增殖,生长速度较快,接种两三天后,即可在倒置显微镜下看到细胞的贴壁生长;②通过神经生长因子诱导,PC12细胞可以长出大量轴突,最长的轴突超过 500 μm,具有神经元的形态,并且表现出多种神经细胞的生理特性。
存活素(survivin):是凋亡蛋白抑制因子家族中最小的成员,包括142个氨基酸,其功能型为同型二聚体。在细胞中呈周期依赖性表达,与有丝分裂期纺锤体微管相互作用,调节G2/M期,并可直接抑制caspase-3和caspase-7的活性。在肿瘤发生发展中,存活素与肿瘤细胞的凋亡负相关,与细胞增殖活性和血管生成正相关。在缺血/再灌注中考虑其通过直接调控caspase家族参与凋亡,或者通过介导血管生成参与其中。
文题释义:
缺血再灌注损伤:缺血一定时间恢复血液供应后,其功能不但未能恢复,却出现了更加严重的功能障碍,称为缺血/再灌注损伤,其机制较为复杂,主要与细胞凋亡、自由基过度形成、兴奋性氨基酸毒性作用、细胞内钙超载、炎性反应、线粒体损伤等多种机制有关。在体外模拟神经缺血再灌注损伤时,常使用大鼠肾上腺嗜铬细胞瘤细胞,因其具有:①胞体圆、明亮,可迅速增殖,生长速度较快,接种两三天后,即可在倒置显微镜下看到细胞的贴壁生长;②通过神经生长因子诱导,PC12细胞可以长出大量轴突,最长的轴突超过 500 μm,具有神经元的形态,并且表现出多种神经细胞的生理特性。
存活素(survivin):是凋亡蛋白抑制因子家族中最小的成员,包括142个氨基酸,其功能型为同型二聚体。在细胞中呈周期依赖性表达,与有丝分裂期纺锤体微管相互作用,调节G2/M期,并可直接抑制caspase-3和caspase-7的活性。在肿瘤发生发展中,存活素与肿瘤细胞的凋亡负相关,与细胞增殖活性和血管生成正相关。在缺血/再灌注中考虑其通过直接调控caspase家族参与凋亡,或者通过介导血管生成参与其中。