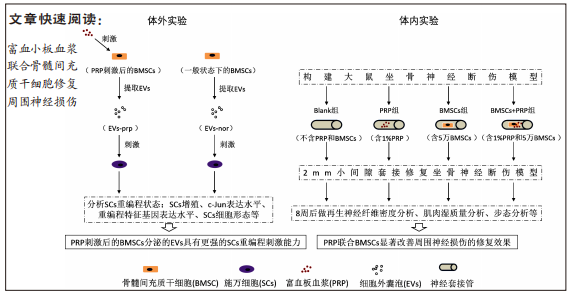
1.1 设计 体外细胞学实验和随机对照动物实验。多组样本比较(≥3组)采用单因素方差分析。
1.2 时间及地点 实验于2021年10月至2022年9月在北京大学人民医院科研教学楼完成。
1.3 材料
1.3.1 实验动物 选取出生后1-3 d龄雌性SD大鼠16只用于提取施万细胞和BMSCs;6-8周龄雌性SD大鼠30只用于提取富血小板血浆和坐骨神经切断伤造模。所有大鼠由北京大学人民医院动物实验室代购自北京维通利华实验动物技术有限公司,动物合格证编号:SCXK(京)2021-0011。该实验由北京大学人民医院伦理委员会批准(批号:2021PHE126,2022PHE048)。
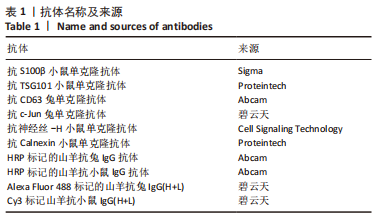
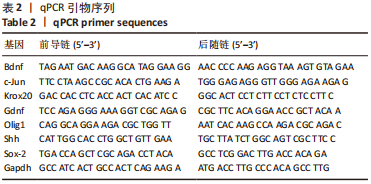
1.3.2 实验主要试剂 DMEM高糖培养基(HyClone);DMEM低糖培养基(HyClone);青-链霉素双抗(HyClone);GlutaMAX (Gibco);胎牛血清(Gibco);EGF-D(Abcam);Forskolin (Sigma);右旋多聚赖氨酸(Sigma);磷酸盐缓冲液(HyClone);Hank’s平衡盐溶液(索莱宝);Ⅰ型胶原酶(Sigma);阿糖胞苷(Sigma);L-15培养基(索莱宝);EdU实验试剂盒(碧云天);大鼠间充质干细胞成脂分化试剂盒(内含油红O染色液,赛业生物);大鼠间充质干细胞成软骨分化试剂盒(内含阿尔辛蓝染色液,赛业生物);地塞米松(用于成骨分化培养基配制,Sigma);β-甘油磷酸(用于成骨分化培养基配制,Sigma);L-抗坏血酸(用于成骨分化培养基配制,麦克林);茜素红染色试剂盒(碧云天);RNA提取试剂盒(奕杉生物);反转录试剂盒(ABM);SYBR(Toyobo);蛋白提取试剂盒(索莱宝);BCA 蛋白定量试剂盒(索莱宝);DAPI染色液(翌圣生物);40 g/L多聚甲醛(碧云天);10%TritonX-100(碧云天);DAPI染色液(翌圣生物);Tissue-Tek® O.C.T. 冷冻包埋剂(SAKURA);壳聚糖(麦克林);冰醋酸(国药);乙酸酐(国药);丙酮(国药);氢氧化钠(麦克林);明胶(Sigma);Matrigel(Corning)。抗体名称及来源见表1,qPCR引物见表2。
1.3.3 实验主要仪器 台式离心机(Eppendorf);超净台(Thermo);蛋白电泳仪(Bio-Rad);PCR仪(Bio-Rad);荧光显微镜(Zeiss);蛋白条带成像仪(Bio-Rad);光学显微镜(Zeiss);超速离心机(Beckman);透射电子显微镜(JEOL);NanoSight纳米颗粒示踪分析仪(Malvern);纯水仪(重庆摩尔);冰冻切片机(Leica);电子天平(Mettler Toledo)。
1.4 实验方法
1.4.1 BMSCs提取、培养与鉴定 利用碎骨块培养法提取BMSCs[23]。首先,将出生后1-3 d的大鼠安乐死,取其胫骨和股骨,尽可能去除表面带有的软组织,之后将骨组织剪碎成约1 mm3的碎块,将碎骨块培养于间充质干细胞完全培养基中(DMEM低糖培养基+体积分数为10%胎牛血清+1x双抗),3-5 d即可在光学显微镜下看见原代细胞从碎骨块中迁移出来(第0代),此时给细胞换液,再培养3 d左右细胞融合度即可达到80%-90%,此时可以按1∶3的比例传代。该研究使用第2代BMSCs进行实验。
使用间充质干细胞三系分化实验来鉴定BMSCs[24]。对于成骨分化实验,细胞培养至80%-90%融合度后将培养基换为成骨分化培养基(DMEM高糖培养基+体积分数为10%胎牛血清+10 nmol/L地塞米松+10 mmol/L β-甘油磷酸+ 50 μmol/L L-抗坏血酸+1x双抗),每3 d换1次成骨分化培养基,诱导培养7-14 d后进行茜素红染色;对于成脂分化实验,将BMSCs培养至90%以上融合度后更换成脂分化培养基,诱导5 d左右进行油红O染色;对于成软骨分化实验,将BMSCs培养至一定数量[(3.0-4.0)×105],用胰酶将细胞消化下来,离心获得细胞沉淀,加入成软骨分化诱导液,诱导6 d后即可进行阿尔辛蓝染色。
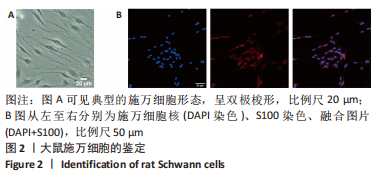
1.4.2 施万细胞提取、培养与鉴定 提取施万细胞的方法是在MAUREL[25]提出的方法上稍加改进的。首先,将出生1-3 d的SD大鼠安乐死,取其坐骨神经置于冰L-15培养基中,离心后用预热的 1 mg/mL Ⅰ型胶原酶重悬,在保温摇床中37 ℃消化30 min;消化完成后,用0.25%胰酶重悬组织,继续在保温摇床中消化5 min;胰酶消化完毕后,用SC-BM培养基(DMEM高糖培养基+体积分数为10%胎牛血清+1x双抗+2 mmol/L GlutaMAX)重悬以清洗消化酶;离心后再用SC-BM重悬神经组织,吹打使神经组织变得分散形成悬液;将悬液接种于右旋多聚赖氨酸包被的培养皿中,放入37 ℃,体积分数为5%CO2培养箱培养,24 h后可见贴壁的施万细胞(第0代)。此时将培养基更换为含10 μmol/L 阿糖胞苷的SC-BM,培养72 h以清除成纤维细胞;最后将培养液更换为SC-EM (SC-BM+2 μmol/L forskolin +10 ng/mL EGF-D)扩增施万细胞;细胞生长至80%-90%融合度时,1∶3传代。该研究使用第3代施万细胞进行实验。
S100是施万细胞特异性表达的蛋白,该研究使用S100免疫荧光染色来鉴别施万细胞。将细胞培养至约50%融合度,PBS清洗后用40 g/L多聚甲醛固定,然后用0.5%Triton X-100通透,通透完成后加入免疫染色封闭液封闭30 min,去除封闭液,加入抗S100β小鼠单克隆抗体(稀释比例为1∶200),4 ℃孵育过夜,第二天吸去一抗并用PBS清洗,加入Cy3标记山羊抗小鼠二抗(稀释比例为1∶500),室温避光孵育2 h,吸去二抗,PBS清洗,加入DAPI染色液,室温避光孵育10 min,PBS清洗后用荧光显微镜观察。
1.4.3 PRP制备 在LI等[26]提出的方法上稍加改进提取PRP。将大鼠麻醉后从心脏抽取全血并通过肝素抗凝管收集,然后将抗凝血转移到含有肝素的离心管中,并在室温下以300×g离心10 min;离心后将血液分成3层,小心地将顶层转移到无菌离心管中,在室温下以3 000×g离心15 min,将得到的上清液视为贫血小板血浆并转移至新管中,使用少量贫血小板血浆重悬沉淀物(血小板)以获得PRP。
1.4.4 EVs的提取 将BMSCs来源EVs分为两类:一类是BMSCs培养于一般条件下所分泌的EVs,命名为EVs-nor;一类是BMSCs培养于含体积分数1% PRP的间充质干细胞完全培养基中所分泌的EVs,命名为EVs-prp。收集细胞上清液,然后用超速离心法提取上清液中的EVs[27]。简要地说,首先4 ℃,300×g离心10 min去除细胞残骸;然后4 ℃,2 000×g离心20 min去除凋亡小体;将上清转入超速离心管,4 ℃,110 000×g第1次离心70 min获得EVs沉淀。为了去除EVs沉淀中可能含有的可溶性蛋白成分,将EVs沉淀重悬于PBS,4 ℃,110 000×g第2次离心70 min,获得较为清洁的EVs。
1.4.5 EVs的鉴定 从3个方面对EVs进行鉴定:①电镜拍照;取 10 μL上述EVs样品,滴加于承载样品的铜网上,在室温下吸附10 min后用滤纸小心吸去多余液体,再滴加2%磷钨酸溶液染色,在室温下晾干处理,通过透射电子显微镜观察;②纳米颗粒示踪分析:用1 mL注射器吸取200倍稀释后的EVs 1 mL左右置于NanoSight纳米颗粒示踪分析仪的微量推注泵上,仪器可自动分析EVs的粒径分布;③EVs标志物蛋白分析:选取TSG-101和CD63两种蛋白进行Western blot检测,具体实验过程见1.4.9。
1.4.6 体外细胞学实验分组及处理 将施万细胞分为3组:PBS组、EVs-nor组、EVs-prp组。EVs-nor组施万细胞接受EVs-nor处理,EVs-prp组施万细胞接受EVs-prp处理,PBS组作为空白对照,接受等体积的PBS处理。EVs的使用质量浓度为5 μg/mL。
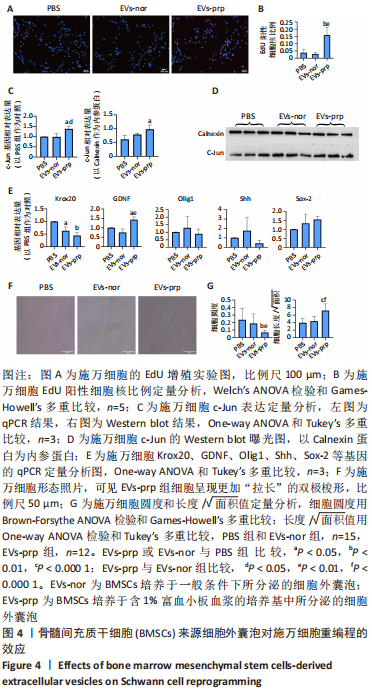
1.4.7 EdU细胞增殖检测 将第3代施万细胞以5 000个/孔的密度种植于96孔板,24 h之后更换培养基为不含EVs的SC-BM,然后按照1.4.6所述方法进行相应处理,24 h之后按照EdU试剂盒说明书的操作步骤检测细胞增殖情况。
1.4.8 qRT-PCR实验 将第3代施万细胞以1×105个/孔的密度接种于6孔板,24 h之后更换培养基为不含EVs的SC-BM,然后按照1.4.6所述方法进行相应处理24 h,处理完成后用RNA提取试剂盒提取RNA,然后用反转录试剂盒将RNA反转录成cDNA,然后用Bio-rad CFX96 PCR仪进行qRT-PCR分析。实验以GAPDH作为内参基因,用2-ΔΔCT法计算基因的相对表达量。
1.4.9 Western blot实验 该研究的Western blot实验有两部分,一是用Western blot对EVs标志物蛋白进行分析,二是对施万细胞重编程的关键蛋白c-Jun进行分析。
对于EVs标志物蛋白分析,由于EVs样本较珍贵,对样本蛋白浓度定量后,取3 μg蛋白量的EVs上样,作为对照,取同样3 μg的BMSCs裂解蛋白上样,经SDS-PAGE凝胶电泳(浓缩胶恒压80 V,分离胶恒压120 V)后转移到PVDF膜上转膜(200 mA电流,转膜2 h)。转膜结束后将膜取出,用5%脱脂奶粉封闭液室温封闭 1 h,然后1×TBST洗膜后加入抗TSG101小鼠单克隆抗体(稀释比例为1∶10 000)和抗CD63兔单克隆抗体(稀释比例为1∶1 000),4 ℃孵育过夜,第2天用1×TBST洗膜后加入HRP标记的山羊抗兔二抗或HRP标记的山羊抗小鼠二抗,室温孵育1 h后,再用1×TBST洗膜,用Bio-Rad蛋白条带成像仪对蛋白进行曝光显像。
对于c-Jun蛋白分析,首先将第3代施万细胞以1×105个/孔的密度接种于6孔板,24 h之后更换培养基为不含EVs的SC-BM,然后按照1.4.6所述方法进行相应处理24 h,处理完成后用蛋白提取试剂盒提取SCs的总蛋白,取20 μg蛋白上样,然后同上述步骤进行实验。
1.4.10 施万细胞形态学分析 将第3代施万细胞在SC-BM培养基下连续培养,每2 d换1次SC-BM培养基,每次换液都按照1.4.6所述方法进行相应处理,10 d后用光学显微镜对施万细胞进行拍照,然后用Image J软件分析施万细胞的细胞圆度(4*π*面积/周长2)和长度/√面积值。
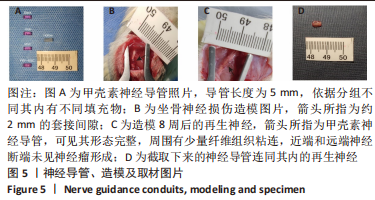
1.4.11 甲壳素神经导管的制作 将壳聚糖粉末溶解在2%冰醋酸中制备4%壳聚糖溶液;将明胶粉末溶解在超纯水中制备1.6%明胶溶液。将壳聚糖溶液与明胶溶液混合并通过搅拌器搅拌成均匀的混合物,使用金属过滤网过滤混合物,然后用超声波清洗器除去气泡。
制备甲壳素导管时,将2 mm直径的克氏针浸入上述混合物中并缓慢拉出,混合物的黏度使其保留在克氏针的表面;将克氏针转移到5%氢氧化钠溶液中15 min固化克氏针表面的混合物;然后用超纯水洗涤固化的混合物24 h;之后将混合物用丙酮脱水并使其在室温下干燥,再浸入乙酸酐中15 min使其乙酰化直至其变得半透明;将混合物推挤出克氏针形成管状结构,使用剪刀将其剪成数个5 mm长的导管,即甲壳素神经导管。在动物实验中,这些神经导管内会填充有各种凝胶成分(见1.4.12)。
1.4.12 动物实验 动物实验旨在验证PRP是否能够增强BMSCs修复周围神经损伤的效果。周围神经损伤模型选用大鼠坐骨神经断伤,使用含有不同填充物的神经导管对断端进行2 mm小间隙套接。实验分组及各组导管填充物描述如下:将20只大鼠随机分为4组,每组5只,即①空白组:神经导管内填充有基础填充物(Matrigel和DMEM低糖培养基以1∶1体积比混合);②PRP组:神经导管内填充有基础填充物+1%PRP;③BMSCs组:神经导管内填充有基础填充物+5×104 BMSCs;④BMSCs+PRP组:神经导管内填充有基础填充物+1%PRP+5×104 BMSCs。Matrigel的作用是更好地使细胞或PRP保持在神经导管内,不易流失。每根导管约能容纳10 μL填充物。
坐骨神经断伤模型造模依据课题组之前已提出的方法实施[28-29]。首先,将大鼠麻醉后,剃去大鼠右后肢的毛发,用碘伏消毒皮肤;然后切开一个小切口,钝性解剖分离周围的肌肉以暴露坐骨神经;在坐骨神经分叉上方7 mm处横切,并且在手术显微镜下使用7-0缝线将神经断端用上述神经导管桥接,在神经残端之间留下2 mm间隙。肌肉和皮肤开口用4-0缝线关闭。
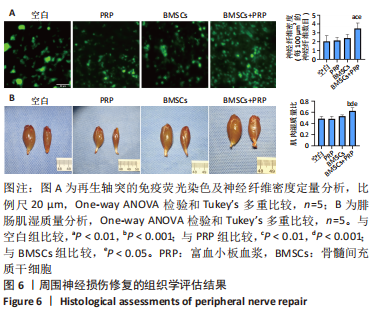
1.4.13 神经纤维免疫荧光染色 术后8周,每组取5只大鼠,将大鼠安乐死,截取再生神经并将其包埋在O.C.T.中;然后使用冰冻切片机在再生神经的中段将神经横切形成10 μm厚的切片;将切片进行PBS清洗,40 g/L多聚甲醛固定,0.5%TritonX-100透膜,5%BSA封闭液封闭等处理之后,再与抗Neurofilament-H一抗(稀释比例为1∶200)孵育,4 ℃过夜,PBS清洗后与Alexa Fluor 488标记的二抗孵育2 h,PBS清洗切片后使用荧光显微镜观察。
1.4.14 腓肠肌肌肉湿质量分析 术后8周,每组取5只大鼠(与1.4.13为同一批大鼠,即取完神经之后取肌肉),将大鼠安乐死,分离手术侧和正常侧腓肠肌,立即用电子天平称质量,并使用以下公式获得湿质量比:湿质量比=m1/m2×100%,其中m1是手术侧肌肉的湿质量,m2是正常侧肌肉的湿质量。
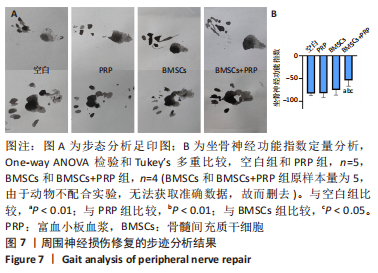
1.4.15 步态分析 术后8周,每组5只大鼠(取材之前进行步态分析),将大鼠置于步道上进行几次适应实验,直到它们学会稳定地在步道上行走。将适当尺寸的白纸放在步道的底部,然后在大鼠的后爪上沾上墨水,让大鼠沿着步道行走,它们的后足印将保留在纸上。对手术侧和正常侧的足印进行以下几个指标的测量:①足印长度(PL,从足后跟到第三足趾的距离);②足趾伸展度(TS,从第一足趾到第五足趾的距离);③中间足趾伸展度(ITS,从第二足趾到第四足趾的距离)。手术侧的上述指标记为ePL、eTS、eITS;正常侧的上述指标记作nPL、nTS、nITS。所有这些指标用于计算以下参数:①足印长度因子(PLF)=(ePL-nPL)/nPL;②足趾伸展因子(TSF)=(eTS-nTS)/nTS;③中间足趾伸展因子(ITSF)=(eITS-nITS)/nITS。使用这些参数,通过Bain-Mackinnon-Hunter(BMH)公式计算坐骨神经功能指数(SFI)。SFI接近0表示正常,SFI为-100表示坐骨神经功能完全受损。BMH公式为SFI=-38.3*PLF+109.5*TSF+13.3*ITSF-8.8。
1.5 主要观察指标 ①BMSCs和施万细胞的鉴定结果;②EVs的鉴定结果;③施万细胞重编程过程;④坐骨神经损伤修复情况。
1.6 统计学分析 使用GraphPad Prism 8.0软件进行数据分析。数据表示为x±s。通过F检验和Brown-Forsythe检验进行方差齐性验证。当满足方差齐性时,使用One-way ANOVA进行差异分析,然后进行Tukey’s多重比较分析;当不满足方差齐性时,使用Welch’s ANOVA检验或Brown-Forsythe ANOVA检验进行差异分析,并用Games-Howell法进行多重比较分析。P < 0.05为差异有显著性意义。文章统计学方法已经通过北京大学人民医院生物统计学专家审核。