1.1 设计 体外细胞学实验,两组间比较采用t检验,多组间比较采用单因素方差分析。
1.2 时间及地点 实验于2020年10月至2022年3月在徐州医科大学口腔医学院实验室和徐州医科大学附属口腔医院完成。
1.3 材料
1.3.1 实验仪器 生物安全柜(力康,中国);二氧化碳培养箱(Thermo Fisher,美国);倒置荧光显微镜(Olympus,日本);NanoDrop 2000 超微量分光光度计(Thermo,美国);实时荧光定量PCR仪(Roche,美国);酶标仪(BioTek,美国);全自动化学发光图像处理系统(天能,中国);移液枪(Eppendorf,德国)。
1.3.2 实验试剂 α-MEM培养基(Gibco,美国);胎牛血清(碧云天,中国);青链霉素(Vicmed,中国);0.25%胰蛋白酶(Vicmed,中国);过表达Sema3A慢病毒载体及其对照慢病毒载体(复能基因,美国);嘌呤霉素(Vicmed,中国);SEMA3A检测试剂盒(酶联免疫吸附试验法)(武汉云克隆,中国);抗坏血酸、地塞米松、β-甘油磷酸钠、CCK-8试剂盒、40 g/L多聚甲醛(Vicmed,中国);碱性磷酸酶(ALP/AKP)测定试剂盒(南京建成,中国);反转录试剂盒PrimeScript RT Master Mix(Takara,日本);UltraSYBR Mixture(康维世纪,中国);BCIP/NBT碱性磷酸酯酶显色试剂盒、茜素红S染色液(2%,pH 4.2)、RIPA裂解液、蛋白酶抑制剂、BCA蛋白浓度测定试剂盒、SDS-PAGE蛋白上样缓冲液、
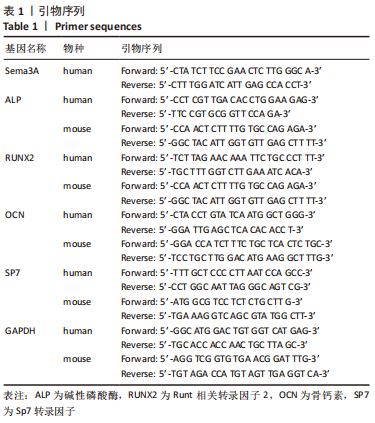
SDS-PAGE凝胶配制试剂盒(碧云天,中国);NC膜(Pall Corp,美国);抗Sema3A抗体(1∶1 000;Proteintech,中国);抗β-actin抗体(1∶10 000;Proteintech,中国);超敏ECL化学发光试剂盒(Merck millipore,美国)。PCR引物由上海生工合成,具体引物序列见表1 。
1.4 实验方法
1.4.1 细胞培养 课题组前期分离培养的DPSCs用于此实验。该细胞收集自5位健康的志愿者(男2例,女3例),为尽量避免个体差异,将5位志愿者的牙髓组织进行了混合。该研究的实施符合徐州市口腔医院的相关伦理要求(医院伦理批件号2019-010)。细胞分离培养步骤简述如下:在获得志愿者(18-25岁)书面知情同意后,收集其拔除的健康第三磨牙。在生物安全柜中,取得牙髓组织,剪碎,冲洗,消化。消化后分离得到的细胞培养在生长培养基(α-MEM+体积分数为10%胎牛血清+1%青链霉素)中。部分原代细胞冻存于液氮中备用,部分原代细胞培养后进行干性鉴定(细胞分离培养步骤及干性鉴定结果详见前期文章[16])。在此次实验中,冻存的原代细胞复苏后继续培养,选取第1代细胞用于基因转导。
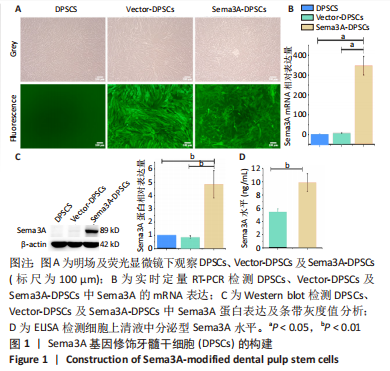
1.4.2 慢病毒转导Sema3A基因 将第1代DPSCs接种在6孔板中(2.5×105个/孔),当细胞密度达到70%时,将旧培养基换为含有4 μg/mL聚凝胺的新鲜培养基。对于转导Sema3A的细胞(Sema3A-DPSCs),将40 μL过表达Sema3A慢病毒载体(EX-G0547-Lv233)加入培养基中;对于对照细胞(Vector-DPSCs),将10 μL对照慢病毒载体(LPP-EGFP-Lv233-100)加入培养基中。孵育12 h后,换为正常培养基。使用1.5 μg/mL的嘌呤霉素筛选稳定转导细胞。通过观察绿色荧光表达,Sema3A mRNA及蛋白表达水平及上清液中分泌型Sema3A水平来检测转导效率。
1.4.3 使用SEMA3A试剂盒采用ELISA法检测分泌型Sema3A水平 将稳定转导的第4代DPSCs及其对照细胞,以2.5×105个/孔的密度接种于6孔板中,种板24 h后收集细胞上清液,1 000×g离心20 min去除沉淀;将100 μL标准品、空白对照及样品分别加入微孔板中37 ℃孵育1 h;其次,加入检测抗体37 ℃继续孵育1 h;然后,加入HRP结合的链霉亲和素37 ℃孵育30 min;最后,每孔加入90 μL底物溶液37 ℃孵育10-20 min后终止反应;酶标仪检测450 nm波长下每孔的吸光度值。
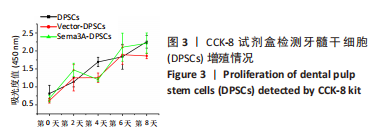
1.4.4 细胞增殖实验 将稳定转导Sema3A的第4代DPSCs(Sema3A-DPSCs)、转导对照病毒的第4代DPSCs(Vector-DPSCs)及第4代未转导的DPSCs以5 000个/孔的密度分别接种于96孔板中,分别在第0,2,4,6,8天检测活细胞数量。在每个检测时间点,将旧培养基换为100 μL含有10% CCK-8溶液的α-MEM,在37 ℃下孵育1 h,酶标仪检测450 nm波长下每孔吸光度值。
1.4.5 Sema3A-DPSCs与前成骨细胞共培养 将小鼠成骨细胞样细胞MC3T3-E1(Vicmed公司)与Sema3A-DPSCs或Vector-DPSCs以1∶1或1∶3的比例混合后,直接接触共培养。
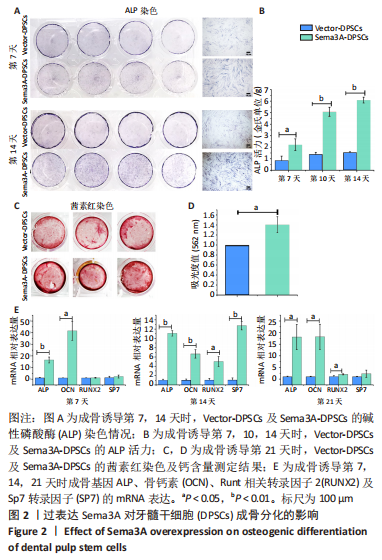
1.4.6 成骨诱导 为检测DPSCs或MC3T3-E1的成骨分化能力,将单独培养的Sema3A-DPSCs、Vector-DPSCs或其与MC3T3-E1直接共培养的混合细胞接种于孔板中,24 h后将普通培养基换为成骨诱导培养基(含有10 mmol/L β-甘油磷酸钠、50 μg/mL 抗坏血酸、10 nmol/L地塞米松的生长培养基)。通过碱性磷酸酶染色、茜素红染色及实时定量RT-PCR检测成骨基因转录情况评价细胞成骨分化能力。
1.4.7 碱性磷酸酶染色及碱性磷酸酶定量 当单独培养的Sema3A-DPSCs、Vector-DPSCs成骨诱导7,14 d时,以及Sema3A-DPSCs或Vector-DPSCs与MC3T3-E1直接共培养后成骨诱导7 d时,用40 g/L多聚甲醛固定,加入BCIP/NBT碱性磷酸酯酶显色溶液孵育1 h进行碱性磷酸酶染色。使用碱性磷酸酶(ALP/AKP)测定试剂盒对细胞中碱性磷酸酶活力进行测定。首先,使用RIPA裂解细胞并提取细胞蛋白;其次,按说明书要求,分别在空白孔、标准孔、测定孔中加入30 μL双蒸水、酚标准液或待测样本,并加入50 μL缓冲液和基质液,充分混匀后37 ℃水浴15 min;最后,加入150 μL显色剂后,测定520 nm波长下的吸光度值。按下列公式计算细胞中碱性磷酸酶活力:
细胞样本碱性磷酸酶活力(金氏单位/g)=[(A测定-A空白)/(A标准-A空白)]× C标准 ÷ Cpr。
C标准:酚标准液质量浓度,0.1 mg/mL;Cpr:样本蛋白质量浓度,g/mL。
1.4.8 茜素红染色及钙含量测定 当单独培养的Sema3A-DPSCs、Vector-DPSCs成骨诱导21 d时,以及Sema3A-DPSCs或Vector-DPSCs与MC3T3-E1直接共培养后成骨诱导21 d时,用40 g/L多聚甲醛固定,加入2%茜素红染色液(pH 4.2)孵育30 min,染色后弃净孔内去离子水,每孔加入10%十六烷基氯化吡啶300 μL,读取562 nm波长的吸光度值。
1.4.9 实时定量RT-PCR 当单独培养的Sema3A-DPSCs、Vector-DPSCs成骨诱导7,14,21 d时,以及Sema3A-DPSCs或Vector-DPSCs与MC3T3-E1直接共培养后成骨诱导21 d时,使用TRIzol分离提取细胞总RNA,并用超微量分光光度计测定RNA含量,使用反转录试剂盒PrimeScript RT Master Mix将mRNA反转录为cDNA,然后进行实时荧光定量RT-PCR反应,在微孔板中配置每孔20 μL的反应体系:2 μL cDNA、100 nmol/L正向及反向引物、10 μL 1× UltraSYBR Mixture及超纯水。使用罗氏LightCycler 480 II进行上机检测。以内参GAPDH为对照,计算目的基因的相对表达量。
1.4.10 Western blot 将Sema3A-DPSCs、Vector-DPSCs及未转染DPSCs接种于6孔板中,24 h后用RIPA裂解液(含1%蛋白酶抑制剂)裂解细胞,提取蛋白;使用BCA蛋白浓度测定试剂盒测量蛋白浓度。吸取一定量的蛋白样品与蛋白上样缓冲液混合,100 ℃加热5 min,制备成上样样品;上样样品在10%聚丙烯酰胺凝胶中进行电泳分离,随后转移至NC膜上;使用5%奶粉对NC膜进行封闭,随后将NC膜浸泡在抗Sema3A抗体(1∶1 000)或抗β-actin抗体(1∶10 000)中,4 ℃过夜;将NC膜孵育在辣根过氧化物酶结合的二抗中;最后,使用超敏ECL化学发光试剂盒使条带化学发光,并用全自动化学发光图像处理系统观察条带发光情况,使用Image J对条带灰度值进行定量分析。
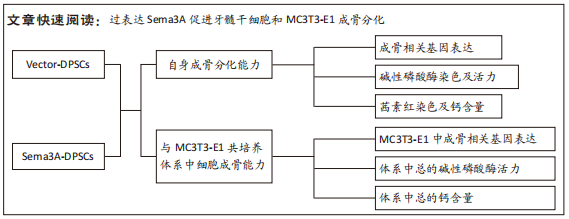
1.5 主要观察指标 ①利用慢病毒载体构建过表达Sema3A的DPSCs,并检测其Sema3A表达及分泌水平;②Sema3A-DPSCs的成骨分化能力(包括成骨基因的转录水平、碱性磷酸酶活力及矿化结节形成情况)及增殖情况;③MC3T3-E1与Sema3A-DPSCs以不同比例共培养后,MC3T3-E1中成骨基因的转录情况,以及共培养体系中碱性磷酸酶活力和矿化结节形成情况。
1.6 统计学分析 所有实验均独立进行了3次。使用SPSS 19.0进行统计分析。数据以x±s表示,使用独立样本t检验比较两组间差异,使用One-way ANOVA比较多组间差异。
P < 0.05为差异有显著性意义。文章统计学方法已经通过徐州医科大学生物统计学专家审核