中国组织工程研究 ›› 2024, Vol. 28 ›› Issue (1): 26-31.doi: 10.12307/2023.772
• 骨髓干细胞 bone marrow stem cells • 上一篇 下一篇
鸢尾素缓解棕榈酸对骨髓间充质干细胞的成骨抑制
张元澍1,2,何 旭1,薛 源2,金叶盛2,汪 凯1,施 勤1,芮永军2
- 1苏州大学苏州医学院,江苏省苏州市 215000;2苏州大学附属无锡九院,江苏省无锡市 214000
Irisin alleviates palmitic acid-induced osteogenic inhibition in bone marrow mesenchymal stem cells
Zhang Yuanshu1, 2, He Xu1, Xue Yuan2, Jin Yesheng2, Wang Kai1, Shi Qin1, Rui Yongjun2
- 1Suzhou Medical College of Soochow University, Suzhou 215000, Jiangsu Province, China; 2Wuxi Ninth People’s Hospital Affiliated to Soochow University, Wuxi 214000, Jiangsu Province, China
摘要:
文题释义:
鸢尾素:是一种在骨骼肌细胞内发现的由FNDC5基因编码的蛋白,鸢尾素的生理作用主要有减轻氧化应激、神经保护作用、抗炎症特性和相关的抗转移作用,因其具有激活各种信号通路的抗炎特性被认为能对肥胖相关疾病发挥潜在保护作用,但具体机制还未被阐明。棕榈酸:脂肪细胞会产生大量的饱和脂肪酸,饱和脂肪酸过量时可能会导致脂毒性,而棕榈酸是脂肪组织中最丰富的饱和脂肪酸之一,常被用于模拟脂毒性细胞模型,这里使用该模型探究鸢尾素对棕榈酸带来脂毒性的保护作用。
目的:探究鸢尾素对棕榈酸诱导的骨髓间充质干细胞成骨能力的影响及作用机制。
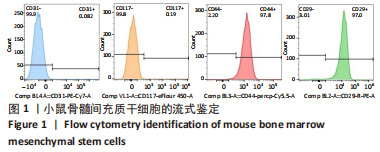
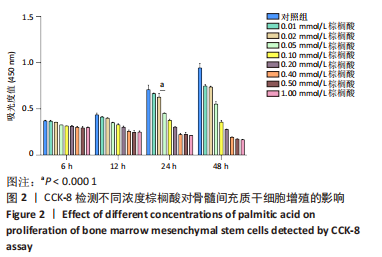
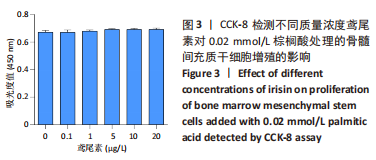
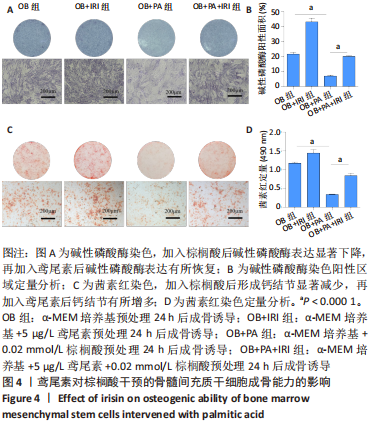
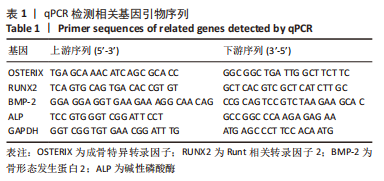
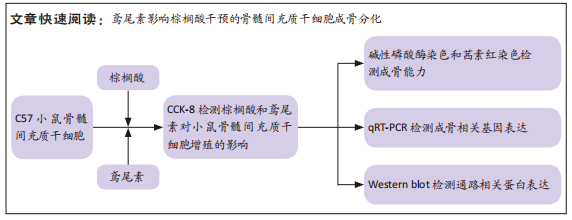
方法:CCK-8检测不同浓度棕榈酸对小鼠骨髓间充质干细胞增殖的影响,以及鸢尾素对棕榈酸存在条件下骨髓间充质干细胞增殖的影响;鸢尾素和棕榈酸预处理24 h后,对小鼠骨髓间充质干细胞成骨诱导分化,在成骨诱导培养第7天进行碱性磷酸酶染色,qRT-PCR检测成骨相关基因的表达,Western blot检测AMPK/BMP2/SMAD信号通路相关蛋白的表达,第21天进行茜素红染色,检测成骨差异。
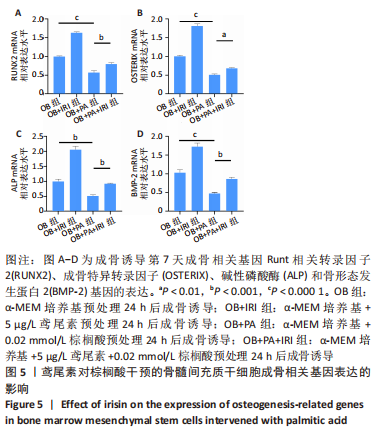
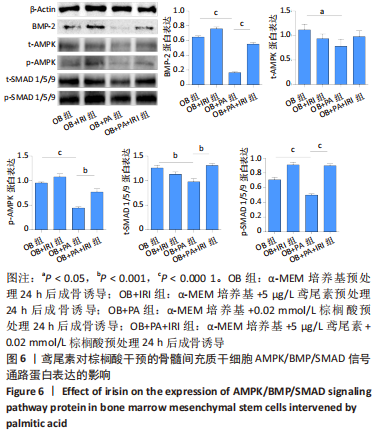
结果与结论:①CCK-8结果提示骨髓间充质干细胞的扩增与棕榈酸的浓度呈反比,但在0.02 mmol/L 浓度时,棕榈酸对骨髓间充质干细胞扩增无显著影响,鸢尾素质量浓度在0.1-20 μg/L范围内时,不影响骨髓间充质干细胞增殖;②碱性磷酸酶染色及茜素红染色结果显示,棕榈酸抑制骨髓间充质干细胞成骨分化能力,鸢尾素能改善棕榈酸诱导的骨髓间充质干细胞成骨抑制,qRT-PCR结果显示,棕榈酸可以引起成骨相关基因下调,而鸢尾素可以抑制这一趋势;③Western bolt结果显示,相较于单纯棕榈酸干预组,鸢尾素处理后增强了骨髓间充质干细胞中AMPK/BMP2/SMAD信号通路传导。该研究发现了鸢尾素能够改善棕榈酸预处理骨髓间充质干细胞的成骨分化能力并提出了具体的机制可能是由AMPK/BMP/SMAD信号通路介导的。
https://orcid.org/0000-0001-7982-7593(张元澍)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: