中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (34): 5430-5435.doi: 10.12307/2023.542
• 组织工程骨材料 tissue-engineered bone • 上一篇 下一篇
氧化石墨烯/壳聚糖复合涂层影响成骨细胞的生物学行为
黄 倩1,2,郝丽英3,贺龙龙1,2,杜良智1,2
- 1西安交通大学口腔医院,陕西省颅颌面精准医学研究重点实验室,陕西省西安市 710004;2西安交通大学口腔医院种植科,陕西省西安市 710004;3四川大学华西口腔医院口腔疾病研究国家重点实验室,四川省成都市 610044
Graphene oxide-chitosan composite coating affects the biological behavior of osteoblasts
Huang Qian1, 2, Hao Liying3, He Longlong1, 2, Du Liangzhi1, 2
- 1Key Laboratory of Shaanxi Province for Craniofacial Precision Medicine Research, College of Stomatology, Xi’an Jiaotong University, Xi’an 710004, Shaanxi Province, China; 2Department of Implant Dentistry, College of Stomatology, Xi’an Jiaotong University, Xi’an 710004, Shaanxi Province, China; 3State Key Laboratory of Oral Diseases Research, West China Hospital of Stomatology, Sichuan University, Chengdu 610044, Sichuan Province, China
摘要:
文题释义:
氧化石墨烯:是一种独特的二维材料,可以看作是石墨的单个单分子层,具有各种含氧官能团,如环氧化物、羰基、羧基和羟基,亲水性好,比表面积大,强度高,易修饰,并且具有良好的生物相容性,在医用材料领域具有广阔的应用前景,并且可以作为添加剂提高材料的机械性能和生物相容性。壳聚糖:是一种氨基多糖,由甲壳类动物和昆虫中的几丁质脱乙酰化而成,具有天然抗菌性、促组织生长能力以及优异的成膜性和生物相容性,可以作为医用金属表面的涂层以有效改善材料生物学性能。
背景:壳聚糖作为医用金属表面的涂层材料可以有效改善其生物学性能,但单纯壳聚糖存在自身生物活性与成骨诱导能力不足的问题;氧化石墨烯能够提高多种聚合物材料的机械性能和生物相容性,并具有促进成骨分化的作用,将两者结合得到的涂层材料可能具有更好的生物性能和成骨活性。
目的:构建氧化石墨烯改性的壳聚糖复合涂层材料,分析涂层材料的表面形貌、化学组成和物理性质,并进一步分析涂层材料对成骨细胞增殖、黏附和成骨分化行为的影响。
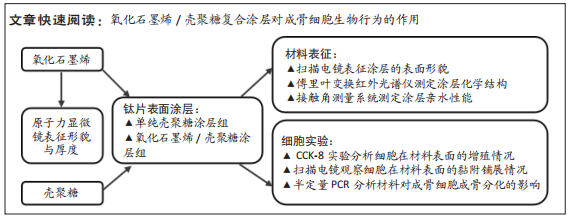
方法:使用3-氨丙基三乙氧基硅烷对钛片表面进行处理,在钛片表面形成硅烷基团,然后利用戊二醛使壳聚糖与硅烷基团形成交联,分别制备单纯壳聚糖涂层与氧化石墨烯/壳聚糖复合涂层。通过原子力显微镜、扫描电镜、傅里叶变换红外光谱仪、接触角测量系统表征涂层的表面形貌、化学结构及亲水性能。将大鼠成骨细胞直接接种于两种涂层材料表面,通过CCK-8实验、扫描电镜和半定量PCR分析材料对大鼠成骨细胞增殖、细胞铺展与成骨分化的影响。
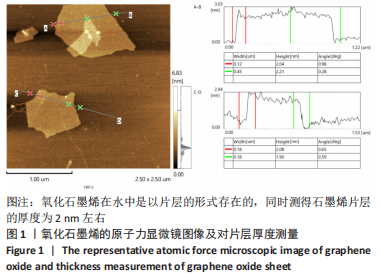
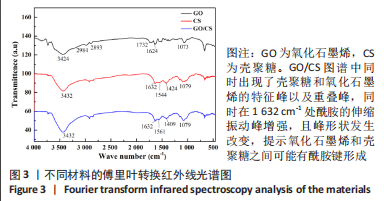
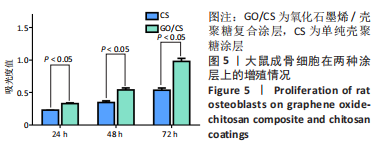
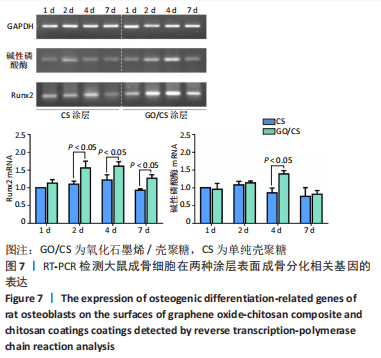
结果与结论:①通过原子力显微镜测得氧化石墨烯片层的厚度为2 nm左右;扫描电镜下可见,两种涂层表面均光滑致密,其中壳聚糖分子紧密排列,氧化石墨烯能够均匀分布于壳聚糖中,同时由于石墨烯的加入,壳聚糖表面出现褶皱样形貌;氧化石墨烯-壳聚糖复合涂层的接触角小于单纯壳聚糖涂层(P < 0.05);②CCK-8实验结果显示,相较于单纯壳聚糖涂层,氧化石墨烯/壳聚糖复合涂层可促进成骨细胞的增殖;③扫描电镜下可见,单纯壳聚糖涂层表面的成骨细胞铺展性较差,氧化石墨烯/壳聚糖复合涂层表面的成骨细胞表现出更好的铺展状态;④半定量PCR检测显示,氧化石墨烯/壳聚糖复合涂层组碱性磷酸酶、Runx2 mRNA表达量多于单纯壳聚糖涂层组(P < 0.05);⑤结果表明,氧化石墨烯/壳聚糖复合涂层具有良好的理化性能、生物相容性和成骨诱导性能。
https://orcid.org/0000-0001-5602-9767(黄倩)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料;口腔生物材料;纳米材料;缓释材料;材料相容性;组织工程
中图分类号: