1.1 设计 体外细胞学实验,多组间比较采用单因素方差分析。
1.2 时间及地点 实验于2021年3月至2022年6月在苏州大学骨科研究所内完成。
1.3 材料
1.3.1 实验动物 雄性6-8周龄C57BL/6小鼠购自上海灵畅生物科技有限公司,体质量18-25 g,实验动物许可证号SCXK(沪)2018-0003。实验方案经苏州大学伦理委员会批准,批准号:SUDA20210324A03。实验过程遵循了国际兽医学编辑协会《关于动物伦理与福利的作者指南共识》和本地及国家法规。
1.3.2 主要试剂与仪器 α-MEM培养基(上海源培生物科技股份有限公司),胎牛血清(美国Gibco-BRL公司),青霉素-链霉素混合液(P/S)(苏州新赛美生物科技有限公司),IWP-2(美国MCE公司),巨噬细胞集落刺激因子(美国PeproTech公司),RANKL(北京索莱宝科技有限公司),RIPA裂解液、BCA蛋白定量试剂盒(上海碧云天生物技术有限公司),GAPDH抗体(武汉赛维尔生物科技有限公司),Non-phospho (Active) β-catenin抗体(美国Cell Signaling Technology公司),HRP山羊抗兔二抗(中国BBI生命科学有限公司),CCK-8检测试剂盒(美国APE × BIO公司),抗酒石酸酸性磷酸酶染色试剂盒(苏州必中生物科技有限公司),RNA isolater、反转录试剂盒、实时荧光定量PCR试剂盒(南京诺唯赞生物科技有限公司)等;超速离心机、PCR仪、NanoDrop 2000C超微量分光光度计(美国Thermo Fisher公司),实时荧光定量PCR仪、ChemiDoc™ Touch化学发光成像系统(美国Bio-Rad公司),全波长自动酶标仪(美国Bio-Tek公司),倒置荧光显微镜(德国Carl Zeiss公司)等。
1.4 方法
1.4.1 BMMs的提取及培养 取6-8周龄雄性C57BL/6小鼠,腹腔注射2%戊巴比妥钠(40 mg/kg),脱颈处死后用体积分数75%乙醇喷洒小鼠身体表面进行消毒,剪开并剥离小鼠后肢的皮肤,取出股骨、胫骨后充分去除表面的肌肉及筋膜等结缔组织。剪去胫骨远端和股骨近端的一小部分骨组织,将骨髓腔中的细胞离心至1.5 mL离心管。用含1% P/S和体积分数10% 胎牛血清的α-MEM培养基培养1 d后收集上清,离心后用含1% P/S、体积分数10%胎牛血清和15 μg/L 巨噬细胞集落刺激因子的α-MEM培养基重悬,置于37 ℃、体积分数5%的CO2培养箱中培养,隔天换液,培养3 d,获得BMMs。在光学显微镜下进行形态学观察,并通过破骨诱导分化和抗酒石酸酸性磷酸酶染色验证BMMs是否能分化为胞体较大、细胞形态不规则、边缘不规整的抗酒石酸酸性磷酸酶阳性多核成熟破骨细胞。

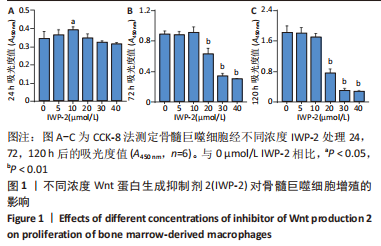
1.4.2 CCK-8检测细胞增殖 将BMMs以5×103/孔的密度种于3块96孔培养板中,分为对照组和IWP-2处理组(浓度分别为5,10,20,30,40 μmol/L),每个浓度设置6个重复孔。对照组用含1% P/S、体积分数10% 胎牛血清、15 μg/L 巨噬细胞集落刺激因子和40 μmol/L IWP-2处理组等体积溶剂DMSO的α-MEM培养基培养;IWP-2处理组用含1% P/S、10% 胎牛血清、15 μg/L 巨噬细胞集落刺激因子和不同浓度IWP-2(5,10,20,30,40 μmol/L)的α-MEM培养基培养,培养24,72,120 h,隔天换液。在每孔中加入10 μL CCK-8检测液后37 ℃孵育2 h,使用全波长酶标仪测定波长450 nm处的吸光度值(A450 nm)。
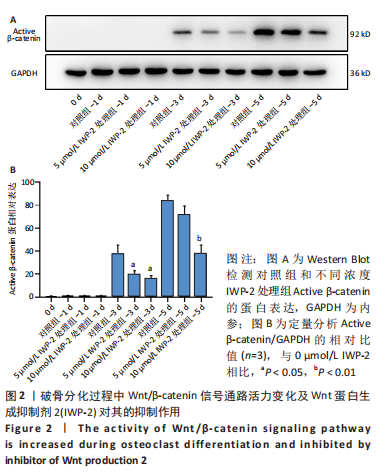
1.4.3 Western blot检测Active β-catenin的蛋白表达水平 将BMMs以4×105/孔的密度种于6孔培养板中,分为对照组和IWP-2处理组(浓度分别为5,10 μmol/L)。对照组用含1% P/S、体积分数10% 胎牛血清、15 μg/L 巨噬细胞集落刺激因子、100 μg/L RANKL和10 μmol/L IWP-2处理组等体积溶剂DMSO的α-MEM培养基培养;IWP-2处理组用含1% P/S、体积分数10% 胎牛血清、15 μg/L 巨噬细胞集落刺激因子、100 μg/L RANKL和不同浓度IWP-2(5 μmol/L和10 μmol/L)的α-MEM培养基培养,隔天换液。分别在0,1,3,5 d用RIPA裂解液收集蛋白,冰上静置20 min,13 000 r/min,4 ℃离心20 min后收集上清,然后用BCA试剂盒测定总蛋白浓度并计算每个蛋白样品20 μg上样量所需蛋白裂解液体积,100 ℃金属浴使蛋白变性。经SDS-PAGE凝胶电泳(电泳参数:浓缩胶90 V,30 min;分离胶120 V)分离蛋白后转移到NC膜上进行转膜(转膜参数:恒压90 V,2 h),转膜结束后将膜取出,用5%脱脂奶粉封闭液室温封闭1 h,然后用1 × TBST缓冲液洗膜后加入GAPDH抗体(1∶2 000稀释)和Active β-catenin抗体(1∶1 000稀释),4 ℃孵育过夜。第2天用1×TBST缓冲液洗膜后加入HRP山羊抗兔二抗,室温孵育1 h后,再用1×TBST缓冲液洗膜,随后将NC膜正面朝上置于化学发光凝胶成像仪中,滴加适量的化学发光液后测定目标蛋白的表达,并以GAPDH为内参,使用Image J软件定量分析目的蛋白的相对表达水平。
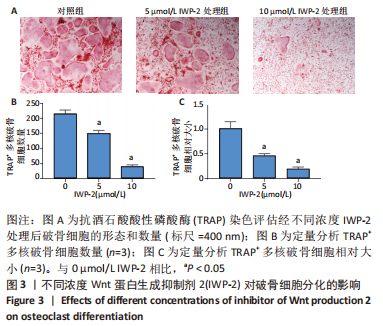
1.4.4 抗酒石酸酸性磷酸酶染色 将BMMs以4×105/孔的密度种于6孔培养板中,分为对照组和IWP-2处理组(浓度分别为5,10 μmol/L)。对照组用含1% P/S、体积分数10%胎牛血清、
15 μg/L 巨噬细胞集落刺激因子、100 μg/L RANKL和10 μmol/L IWP-2处理组等体积溶剂DMSO的α-MEM培养基培养,IWP-2处理组用含1% P/S、体积分数10%胎牛血清、15 μg/L 巨噬细胞集落刺激因子、100 μg/L RANKL和不同浓度IWP-2(5,10 μmol/L)的α-MEM培养基培养至第6天,隔天换液。吸去培养基,用PBS洗1遍后,每孔加入500 μL 4% PFA溶液固定20 min。固定结束后用PBS洗1遍,然后参照抗酒石酸酸性磷酸酶染色试剂盒的说明进行染色。在倒置荧光显微镜下观察采集图像,并使用Image J软件定量分析抗酒石酸酸性磷酸酶阳性且细胞核数量3个以上的破骨细胞数量和相对大小。
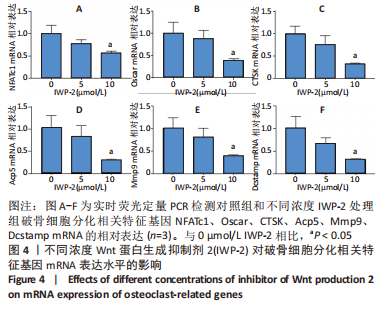
1.4.5 实时荧光定量PCR检测NFATc1、Oscar、CTSK、Acp5、Mmp9、Dcstamp的mRNA表达水平 将BMMs以4×105/孔的密度种于6孔培养板中,分为对照组和IWP-2处理组(浓度分别为5,10 μmol/L)。对照组用含1% P/S、体积分数10%胎牛血清、15 μg/L 巨噬细胞集落刺激因子、100 μg/L RANKL和10 μmol/L IWP-2处理组等体积溶剂DMSO的α-MEM培养基培养;IWP-2处理组用含1% P/S、体积分数10% 胎牛血清、15 μg/L 巨噬细胞集落刺激因子、100 μg/L RANKL和不同浓度IWP-2(5 μmol/L和10 μmol/L)的α-MEM培养基培养至第6天,隔天换液。用RNA isolater提取细胞总RNA并测定浓度,经反转录合成cDNA。选用20 μL反应体系(SYBR Green Master Mix 10 μL,ddH2O 7.5 μL,正向引物0.25 μL,反向引物0.25 μL,cDNA 2 μL),反应条件为95 ℃,5 min;95 ℃,10 s和60 ℃,30 s(40个循环);65 ℃到95 ℃,每步升高0.5 ℃,反应5 s。用以下引物检测特异性基因表达:
Rn18s:上游,5’-CGG CTA CCA CAT CCA AGG AA-3’;下游,5’-GCT GGA ATT ACC GCG GCT-3’;
NFATc1:上游,5’- CAA CGC CCT GAC CAC CGA TAG -3’;下游,5’- GGC TGC CTT CCG TCT CAT AGT -3’;
Oscar:上游,5’- CTG CTG GTA ACG GAT CAG CTC CCC AGA -3’;下游,5’- CCA AGG AGC CAG AAC CTT CGA AAC T -3’;
CTSK:上游,5’- ACG GAG GCA TTG ACT CTG AAG ATG -3’;下游,5’- GGA AGC ACC AAC GAG AGG AGA AAT -3’;
Acp5:上游,5’- TGT GGC CAT CTT TAT GCT -3’;下游,5’- GTC ATT TCT TTG GGG CTT -3’;
Mmp9:上游,5’- GAT CCC CAG AGC GTC ATT C -3’;下游,5’- CCA CCT TGT TCA CCT CAT TTT G -3’;
Dcstamp:上游,5’- TCC TCC ATG AAC AAA CAG TTC CAA -3’;下游,5’- AGA CGT GGT TTA GGA ATG CAG CTC -3’。
以Rn18s为内参,使用2-ΔΔCt法计算目的基因相对表达量。
1.5 主要观察指标 ①CCK-8法检测经不同浓度IWP-2处理24,72,120 h后BMMs的增殖情况;②Western blot检测破骨分化过程中Wnt/β-catenin信号通路活力变化及IWP-2对其的抑制作用;③ 抗酒石酸酸性磷酸酶染色检测不同浓度IWP-2对破骨细胞分化的影响;④实时荧光定量PCR检测经不同浓度IWP-2处理后破骨细胞分化相关特征基因NFATc1、Oscar、CTSK、Acp5、Mmp9、Dcstamp mRNA的表达水平。
1.6 统计学分析 使用GraphPad Prism 8.0软件进行数据分析处理及构图,多组间比较采用单因素方差分析,P < 0.05为差异有显著性意义。文章统计学方法已经苏州大学生物统计学专家审核。