1.1 设计 动物实验和细胞实验,对于正态分布数据采用方差分析和 t 检验,率的显著性比较采用χ2检验。
1.2 时间及地点 实验于2020年5月至2022年5月在新疆医科大学第一附属医院科技楼实验室完成。
1.3 材料
1.3.1 实验动物 3月龄SPF级雌性SD大鼠10只,体质量180-220 g,购买自新疆医科大学动物实验室,此次实验严格遵守中华人民共和国科技部[2006]398 号文件《关于善待实验动物的指导性意见》要求。实验方案经新疆医科大学第一附属医院动物实验医学伦理委员会批准,伦理批号:K202005-18。
1.3.2 主要试剂及仪器 CD29抗体(Affinity AF5379);CD90抗体(Affinity DF6849);CD45抗体(Affinity DF6839);Goat anti-rabbit cy3(Proteintech SA00009-2);无外泌体血清(Umibio);Trizol (Invitrogen);SYBRGreen PCR试剂盒(Thermo F-415XL);反转录试剂盒(Thermo #K1622);荧光定量 PCR中的引物由上海生工公司合成;外泌体提取纯化试剂盒(Umibio UR52121);BRL大鼠肝细胞(CTCC);醋胺酚(索莱宝 IA0030);TUNEL检测试剂盒(索莱宝,#T2190);293T细胞(CTCC);Lipofectamine 2000(Invitrogen);双荧光检测试剂盒(Promega E1910);miR-21-5p NC、miR-21-5p inhibitor、miR-21-5p mimics、质粒(汉恒生物);LY294002(MCE公司);DMEM低糖培养基、RPMI 1640培养基、胎牛血清(Hyclone);红细胞裂解液(天津灏洋生物)。
细胞培养箱(Thermo Scientific 8000);细胞培养皿及孔板(NEST);光学显微镜(XDS-1A);倒置拍照显微镜(OLYMPUS,IX71);低速离心机(上海卢湘仪,TDZ4B-WS);超净工作台(苏州安泰科技有限公司);低温冷冻离心机(德国Eppendorf公司);Real-time检测仪(ABI-7500);超高速离心机(HITACHI,Japan);透射电镜(日本HITACHI);酶标检测仪(Thermo,MK3型);摇床(Qilinbeier,TS-1000);脱色摇床(海门市其林贝尔,TS200A);发光检测仪(Molecular Devices,SpectraMax®i3 )。
1.4 实验方法
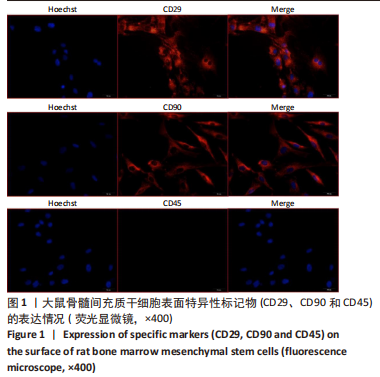
1.4.1 大鼠骨髓间充质干细胞的分离与培养 无菌条件下取出大鼠双侧股骨和胫骨,剪开干骺端,抽取无血清DMEM低糖培养基反复冲洗骨髓腔4次,过滤,1 200 r/min离心5 min,加入红细胞裂解液裂解5 min,1 000 r/min离心5 min,弃上清,洗涤2次后用8 mL含体积分数为10%胎牛血清的DMEM低糖培养基重悬细胞,于37 ℃、体积分数为5%CO2培养箱静置培养3 d,移除不贴壁的细胞;每48 h换液或传代后,进行爬片处理,经过一抗、二抗孵育后,荧光显微镜下观察CD29、CD90以及CD45的阳性表达。

1.4.2 大鼠骨髓间充质干细胞中转染 miR-21-5p 抑制物 制备转染复合物:①用500 μL DMEM低糖基础培养基稀释miR-21-5p NC或miR-21-5p inhibitor;②用460 μL DMEM 低糖基础培养基稀释40 μL Lipofectamine 2000,室温孵育5 min;③将①、②的液体混匀,室温孵育20 min,即为转染复合物。
miR-21-5p inhibitor序列为:UCA ACA UCA GUC UGA UAA GCU A;NC序列为:CAG UAC UUU UGU GUA GUA CAA。
选取第3代骨髓间充质干细胞,调整细胞浓度为1×108 L-1,接种于10 cm细胞培养皿,37 ℃、体积分数为5%CO2培养箱内培养24 h,观察细胞80%融后开始转染,将转染的细胞在37 ℃,体积分数为5%CO2培养箱内培养4-6 h后,加入8 mL含体积分数为10%无外泌体血清的DMEM低糖完全培养基培养48 h。显微镜下观察细胞状态并拍照,分别收取上清液及细胞样本进行后续实验。
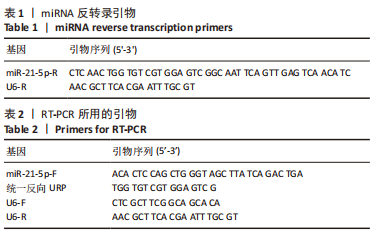
1.4.3 RT-PCR检测目的基因表达变化 使用TRIzol法提取1.4.2转染后细胞的总 RNA,反转录为 cDNA,miRNA反转录引物见表1,RT-qPCR检测miR-21-5p表达,所使用的引物由上海生工公司Primer Premier 5.0软件设计、合成,以U6为内参。引物序列见表2。反应体系:cDNA 1 μL,PCR上下游引物(10 μmol/L)1 μL,Ultra SYBR混合物10 μL和DEPC水7 μL;扩增条件:94 ℃ 10 min,(94 ℃ 20 s、55 ℃ 20 s、72 ℃ 20 s) 40个循环。待测基因表达水平用2-ΔΔCt表示。
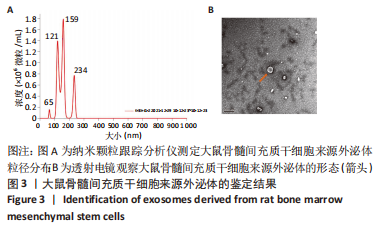
1.4.4 外泌体提取及鉴定 将转染后细胞培养上清液以3 000×g离心10 min去除细胞碎片,2 000×g离心10 min以去除死细胞,4 ℃以10 000×g离心60 min,弃上清,用PBS均匀吹打,4 ℃以12 000×g离心2 min,保留上清液,该上清液中富含外泌体颗粒。将收获的外泌体颗粒粗品转入Exosome Purification Filter (EPF柱)上室中,于4 ℃以3 000×g离心10 min,离心后收集纯化后的外泌体颗粒。
透射电镜观察外泌体形态:将上述外泌体纯化通风处理后,采用漂浮法用醋酸双氧铀负染,通过透射电镜观察外泌体形态以及大小。
BCA 法测蛋白含量:按 BCA 试剂盒步骤测定蛋白浓度,并根据所得浓度调整外泌体稀释倍数,以保证测量的准确性。
纳米颗粒跟踪分析仪检测外泌体浓度以及粒径:将上述外泌体混悬液稀释1 000 倍,充分混匀,用 ParticleMetrix纳米颗粒跟踪分析仪测量外泌体浓度(囊泡数/mL)和粒径分布范围。
外泌体的保存:纯化后的外泌体分装保存于-80 ℃低温冰箱中。
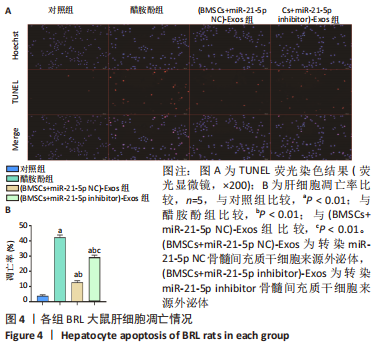
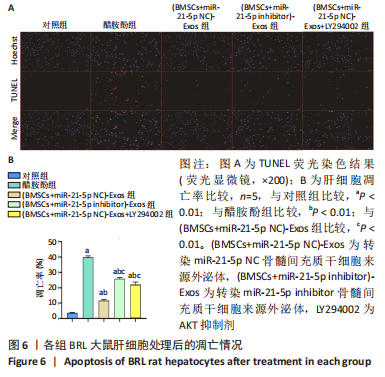
1.4.5 外泌体对BRL大鼠肝细胞凋亡的影响 将BRL细胞接种于96孔培养板,每孔2×102个细胞,培养24 h,对细胞进行分组处理:①对照组:BRL细胞;②醋胺酚组:BRL细胞+醋胺酚(1 μL),制备肝细胞损伤模型;③(BMSCs+miR-21-5p NC)-Exos组:BRL细胞+醋胺酚(1 μL)+(BMSCs+miR-21-5p NC)-Exos(39 μL);④(BMSCs+miR-21-5p inhibitor)-Exos 组:BRL细胞+醋胺酚(1 μL)+(BMSCs+miR-21-5p inhibitor)-Exos(25 μL)。用1640完全培养基稀释醋胺酚母液,使终浓度为5 mmol/L;稀释外泌体至终浓度为100 μg/mL;将BRL细胞放置于37 ℃,体积分数为5%CO2培养箱内培养72 h,通过末端脱氧核苷酸转移酶dUTP缺口末端标记(TUNEL)染色检测细胞凋亡情况,荧光显微镜计数载玻片5个随机选择区域中的TUNEL阳性细胞。
1.4.6 双荧光素酶检测 构建双荧光素酶报告载体,将正常的3’-UTR 序列(WT)和靶序列结合位点突变的3’-UTR序列(MUT)分别插入到PmirGLO载体携带的海肾荧光素酶(human codon optimized-Renilla luciferase,hRluc)的3’-UTR区域,构建表达目标基因的载体(PmirGLO-PIK3R1 3’UTR-wt和PmirGLO-PIK3R1 3’UTR-mutant)。
将293T细胞接种于24孔培养板(每孔2×103个细胞)培养24 h,待细胞80%融合时对细胞进行分组处理:①对照组:293T+miR-21-5p NC+PmirGLO-control;②PI3KR1野生型载体组:293T+miR-21-5p NC+PmirGLO-PIK3R1 3’UTR WT;③PIK3R1突变型载体组:293T+miR-21-5p NC+PmirGLO-PIK3R1 3’UTR MUT;④miR-21-5p mimics组:293T+miR-21-5p mimics+PmirGLO-control;⑤miR-21-5p mimics联合PI3KR1野生型载体组:293T+miR-21-5p mimics+PmirGLO-PIK3R1 3’UTR WT;⑥miR-21-5p mimics联合PI3KR1突变型载体组:293T+ miR-21-5p mimics+PmirGLO-PIK3R1 3’UTR MUT。用15 μL无血清1640培养基稀释双荧光素酶报告基因载体;用10 μL无血清1640培养基稀释miRNA mimics;用25 μL无血清1640培养基稀释0.5 μL Lipofectamine 2000,室温孵育5 min。每孔分别加入50 μL 1640培养基,再分别加入50 μL上述混合液,mimics转染浓度为50 nmol/L,miR-21-5p mimics合成序列见表3。质粒浓度为100 ng/孔,每组设置3个复孔,培养4-
6 h后加入500 μL 1640完全培养基,培养48 h后进行双荧光素酶报告基因检测。

1.4.7 外泌体中miR-21-5p直接靶向PI3K/AKT信号通路对大鼠肝细胞凋亡影响的检测 在6孔板中扩增BRL细胞至第2代,待细胞达到50%融合时对细胞进行分组处理:①对照组:BRL细胞;②醋胺酚组:BRL细胞+醋胺酚(20 μL),制备肝细胞损伤模型;③(BMSCs+miR-21-5p NC)-Exos组:BRL细胞+醋胺酚(20 μL)+(BMSCs+miR-21-5p NC)-Exos(781.25 μL);④(BMSCs+miR-21-5p inhibitor)-Exos组:BRL细胞+醋胺酚(20 μL)+(BMSCs+miR-21-5p inhibitor)-Exos(504 μL);⑤(BMSCs+miR-21-5p NC)-Exos+LY294002组:BRL细胞+醋胺酚(20 μL)+(BMSCs+miR-21-5p NC)-Exos(781.25 μL)+LY294002(10 μL)。用1640完全培养基稀释,醋胺酚母液终浓度为5 mmol/L;外泌体终浓度为100 μg/mL;LY294002母液终浓度为50 μmol/L;培养48 h后弃去培养基,根据组别再次用1640完全培养基稀释醋胺酚、外泌体,继续培养24 h,使总培养时间为72 h;显微镜下观察细胞状态并拍照,通过TUNEL染色检测细胞凋亡情况。
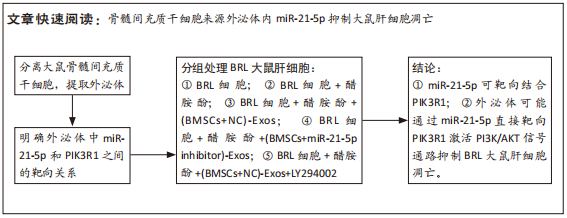
1.5 主要观察指标 ①抑制miR-21-5p表达的骨髓间充质干细胞来源外泌体对大鼠肝细胞凋亡的影响;②双荧光素酶报告基因检测验证miR-21-5p和PIK3R1之间的靶向关系;③外泌体中miR-21-5p直接靶向PIK3R1激活PI3K/AKT信号通路对BRL大鼠肝细胞凋亡的影响。
1.6 统计学分析 使用 SPSS 26.0统计软件进行统计分析,计量资料以x±s表示,采用配对t 检验,P < 0.01为差异有显著性意义。计数资料采用χ2 检验,用率(%)表示;检验水准:α=0.05,P < 0.01为差异有显著性意义。文章统计学方法已经新疆医科大学生物统计学专家审核。