中国组织工程研究 ›› 2022, Vol. 26 ›› Issue (4): 553-559.doi: 10.12307/2022.091
• 材料生物相容性 material biocompatibility • 上一篇 下一篇
聚丙烯酸/琼脂糖三维培养构建细胞球的方法
何云影1,李玲婕2,3,4,张舒淇2,李雨舟2,3,4,杨 生2,3,4,季 平2,3,4
- 1重庆医科大学口腔医学院,重庆市 401147;2重庆医科大学附属口腔医院,重庆市 401147;3口腔疾病与生物医学重庆市重点实验室,重庆市 401147;4重庆市高校市级口腔生物医学工程重点实验室,重庆市 401147
Method of constructing cell spheroids based on agarose and polyacrylic molds
He Yunying1, Li Lingjie2, 3, 4, Zhang Shuqi2, Li Yuzhou2, 3, 4, Yang Sheng2, 3, 4, Ji Ping2, 3, 4
- 1College of Stomatology, Chongqing Medical University, Chongqing 401147, China; 2Stomatological Hospital of Chongqing Medical University, Chongqing 401147, China; 3Chongqing Key Laboratory of Oral Diseases and Biomedical Sciences, Chongqing 401147, China; 4Chongqing Municipal Key Laboratory of Oral Biomedical Engineering of Higher Education, Chongqing 401147, China
摘要:
文题释义:
细胞球:是一种简单且被广泛应用的多细胞三维培养模型,细胞在隔绝与基底的黏附作用后,由于聚集倾向而相互靠拢形成细胞球。这种立体结构促进了细胞与周围细胞在空间上的交流,符合体内细胞的生长状态,一定程度上还原了细胞在体内的生存环境,生理学相关性强。
琼脂糖:是一种提取自藻类的多糖,可溶解在沸腾的溶液中,冷却后形成凝胶。琼脂糖凝胶无细胞毒性,且不携带细胞黏附位点,因此人和动物的细胞不能附着在该水凝胶之上。
背景:细胞球三维培养模型在组织工程领域应用前景广泛,但使用商品化超低吸附培养板进行细胞球培养的实验成本较高,因此需探寻一种细胞球成形的替代策略,推动细胞球在相关研究领域的应用。
目的:采用琼脂糖和聚丙烯酸模具,并利用层层自组装技术构建细胞球三维培养模型,部分模拟细胞体内生存的微环境。
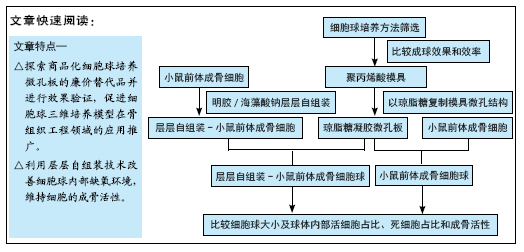
方法:体外培养小鼠前体成骨细胞,依次使用明胶与海藻酸钠对小鼠前体成骨细胞进行层层自组装处理(层层自组装-小鼠前体成骨细胞),同时分别制备明胶包裹与海藻酸钠包裹的小鼠前体成骨细胞。分别制备琼脂糖凝胶涂层培养板与琼脂糖凝胶微孔板,观察上述不同处理的细胞在两种培养板中的成球效果,采用Live/Dead染色法检测细胞球的活性,采用碱性磷酸酶染色法、RT-PCR 实验检测细胞球的成骨能力。
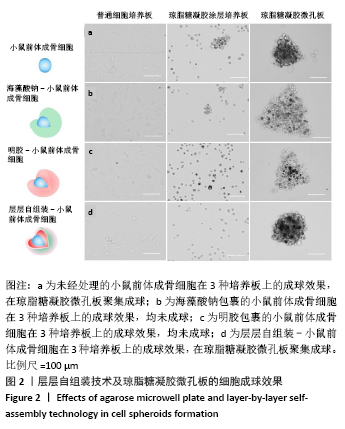
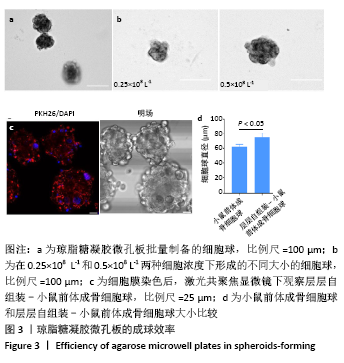
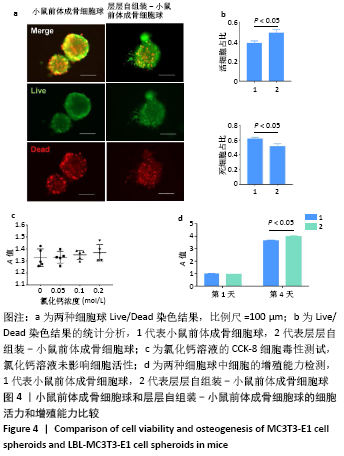
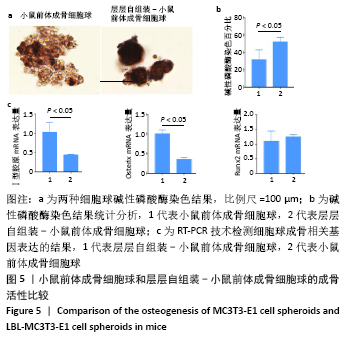
结果与结论:①光学显微镜下可见,在琼脂糖凝胶涂层孔板中,未经处理与经3种涂层处理的小鼠前体成骨细胞均未成球;在琼脂糖凝胶微孔板中,未经处理与层层自组装处理的小鼠前体成骨细胞形成了理想的细胞球,其中层层自组装-小鼠前体成骨细胞球的直径大于未经处理小鼠前体成骨细胞球(P < 0.05);②Live/Dead染色显示,层层自组装-小鼠前体成骨细胞球内的细胞活性高于未经处理小鼠前体成骨细胞球(P < 0.05);③层层自组装-小鼠前体成骨细胞球的碱性磷酸酶活性高于未经处理小鼠前体成骨细胞球(P < 0.05),Ⅰ型胶原和Osterix基因表达高于未经处理小鼠前体成骨细胞球(P < 0.05),两组Runx2基因表达比较差异无显著性意义(P > 0.05);④结果表明,采用琼脂糖凝胶结合层层自组装技术成功建立了细胞球三维培养模型,此方法便捷、经济、高效且细胞活性良好,保留了细胞成骨分化能力,在骨组织工程和再生医学领域具有潜在应用价值。
https://orcid.org/0000-0003-4820-7468 (何云影)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料; 口腔生物材料; 纳米材料; 缓释材料; 材料相容性;组织工程
中图分类号:
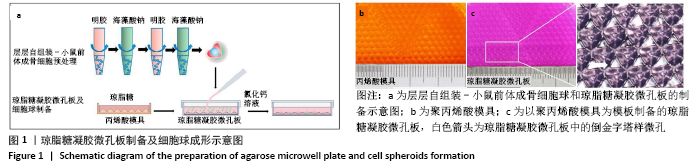

 在琼脂糖凝胶微孔板的辅助下细胞聚集成球,恢复了生理条件下的空间结构,但这也只是在宏观层面上对细胞的生存环境进行了重塑,还原了宏观环境,而细胞所处的细胞外基质也可以在微观层面上影响其命运,调节其功能[21]。因此为了恢复细胞外微观环境,实验中采取了层层自组装技术,利用明胶和海藻酸钠进行细胞表面修饰[4]。明胶是一类生物安全性良好的胶原水解产物,与生理性细胞外基质相
在琼脂糖凝胶微孔板的辅助下细胞聚集成球,恢复了生理条件下的空间结构,但这也只是在宏观层面上对细胞的生存环境进行了重塑,还原了宏观环境,而细胞所处的细胞外基质也可以在微观层面上影响其命运,调节其功能[21]。因此为了恢复细胞外微观环境,实验中采取了层层自组装技术,利用明胶和海藻酸钠进行细胞表面修饰[4]。明胶是一类生物安全性良好的胶原水解产物,与生理性细胞外基质相