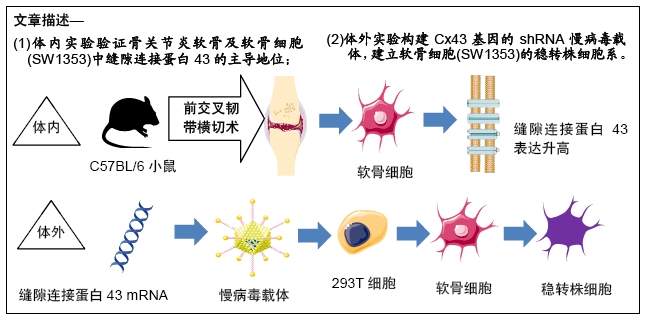
1.1 设计 小鼠自身对照、体外细胞实验。
1.2 时间及地点 于2017年4月至2019年6月在首都医科大学北京口腔医学研究所进行。
1.3 材料
1.3.1 实验动物 实验选取6只10周龄的SPF级C57BL/6小鼠,体质量平均(20±3)g,动物来源:国家啮齿类实验动物种子中心上海分中心,许可证号:SCXK(川)2015-030。
1.3.2 软骨细胞(SW1353)细胞株 由亚太恒信生物科技(北京)有限公司提供。
1.3.3 主要实验仪器和试剂 Leica石蜡包埋机;CO2培养箱(Panasonic SANYO MCO-15AC);离心机(瑞江 RT-TDL-40B);显微镜(COIC XDS-1B);MEM Alpha、胰酶、嘌呤霉素(Puromycin)(均为Gibco);胎牛血清(康源生物);DMSO(Sigma);10 cm Cell Culture Dish,6/24/96 Well Cell Culture Plate(均为NEST);冻存管(AXYGEN);293T细胞(上海生博生物医药科技有限公司);Vectastain Elite ABC试剂盒和DAB过氧化物酶底物试剂盒(均为Vector Labs;Burlingame,CA);兔抗Cx43抗体(1∶1 000)(sigma,Cat. Number C6219, St Louis, MO);兔IgG(Cat. Number 31235, Thermo Scientific, Waltham, MA)。
1.4 实验方法
1.4.1 实验动物及分组 实验选用C57BL/6小鼠6只,采取自身对照,以小鼠右侧后肢为实验侧手术诱导骨关节炎,左侧后肢为对照侧行假手术,术后4周收样。
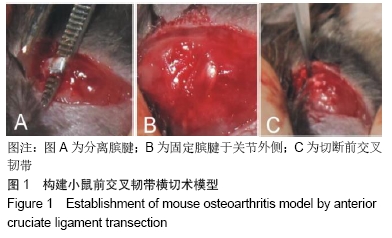
1.4.2 建立小鼠膝骨关节炎模型 使用前交叉韧带横切术(anterior cruciate ligament transection,ACLT)构建小鼠关节不稳定模型[9]。具体方法如下:水合氯醛腹腔注射麻醉后消毒双侧后肢,备皮,于双侧膝关节前方的皮肤处作约3 mm长的纵行切口后行膝关节内侧切口。直视下分离膑腱(见图1A),将膑腱轻柔拨向外侧(见图1B),用手术刀尖划断实验侧前交叉韧带(见图1C)。经抽屉试验确认前交叉韧带完全切断后缝合关节腔软组织和皮肤。对照侧仅做膝关节内侧切口,不予切断前交叉韧带,直接缝合关节腔软组织和皮肤。术后给予正常饮食。建模后4周麻醉后处死小鼠,取双侧膝关节及相应的股骨及胫骨,固定于40 g/L多聚甲醛溶液中过夜后放入5 g/L多聚甲醛溶液中继续保存。

1.4.3 标本及切片制备 双蒸水冲洗12个样本后置入400 mL 10%EDTA溶液中脱钙,每日更换脱钙液,脱钙共计20 d。脱钙完成后使用双蒸水冲洗,之后进行梯度脱水,依次使用体积分数70%,80%,90%,95%,100%的乙醇使组织脱水,每个梯度8 h。将标本置入二甲苯进行透明,直至组织块不漂浮于二甲苯上。组织块浸入融化状态的石蜡液体中,30 min后进行包埋。制备石蜡切片并编号,调整方向使刀片与膝关节的冠状面平行,并作连续切片,每张切片厚4 μm,切片以实验分组的顺序进行编号并作相应标记。切片完成后放入50 ℃烤箱中过夜。
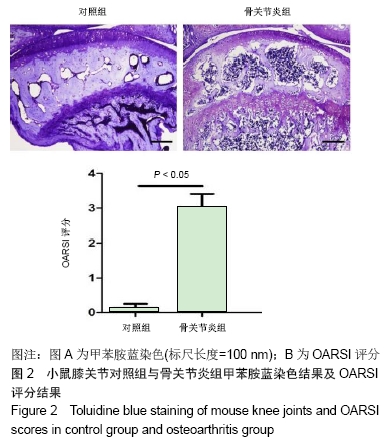
1.4.4 甲苯胺蓝染色 ①脱蜡:将干燥切片放入氢氧化钾的无水乙醇饱和溶液中浸泡10-15 min,无水乙醇清洗3次;②水化:体积分数100%,95%,90%,80%,70%乙醇梯度水化;自来水冲洗3次,每次5 min;浸染于甲苯胺蓝染液中10 min;自来水清洗去多余染液;体积分数70%,80%,90%,95%,100%乙醇梯度脱水;二甲苯透明,中性树胶封固后置于显微镜下观察。
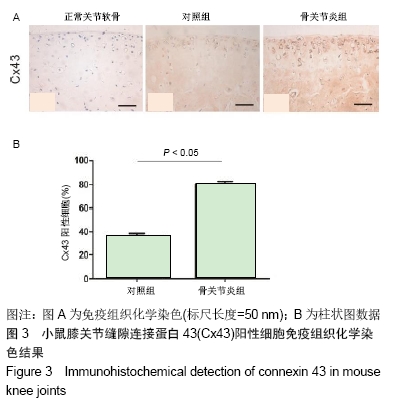
1.4.5 免疫组织化学染色 标本及切片制备同前,用Vectastain Elite ABC试剂盒和DAB过氧化物酶底物试剂盒在石蜡包埋的小鼠膝关节冠状切片上进行免疫组织化学染色,加入兔抗Cx43抗体(1∶1 000)检测小鼠膝关节Cx43的表达;以未免疫兔IgG作阴性对照。
1.4.6 SW1353细胞培养 从液氮中取出SW1353冻存细胞,置37 ℃水浴中振摇使细胞快速融化;细胞冻存液加入10 mL无血清DMEM培养基,1 000 r/min离心5 min后吸弃上清;用新鲜的完全培养液悬浮细胞后,传至培养皿中培养,待细胞长满后传代。细胞长至单层后倾去培养液;用温的1×PBS洗3次;加入适量胰酶,转动培养皿,使胰酶能浸润全部皿底;显微镜下观察,细胞间的胞间连丝蛋白被消化脱落,细胞呈类圆形,加入含血清培养基终止消化;将细胞吹落,收集进10 mL离心管,600 r/min,5 min离心,弃上清,重悬细胞;传代培养。第3代细胞用于实验。
1.4.7 SW1353细胞对嘌呤霉素耐药浓度的筛选 制备SW1353细胞悬液,血球计数板计数;铺板:5 000个细胞/24孔,共10个24孔,37 ℃、CO2培养箱培养过夜;当细胞汇合度达到30%-40%时,配置如下质量浓度的嘌呤霉素:0,0.5,1,1.5,2,3,4,5,6,7 mg/L;每个24孔加入1 mL上述各质量浓度的嘌呤霉素,37 ℃、CO2培养箱培养3 d左右,全部细胞死亡的最低质量浓度作为该细胞对嘌呤霉素的最佳耐药质量浓度。
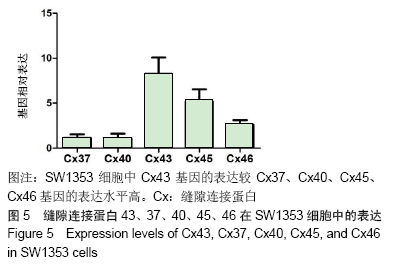
1.4.8 RT-PCR检测SW1353细胞中Cx43、Cx37、Cx40、Cx45、Cx46的mRNA表达 用TRIzol试剂从细胞中提取总RNA并合成cDNA。使用SYBR Green Realtime
PCR Master Mix试剂盒进行实时荧光定量PCR (qRT-PCR)分析。qRT-PCR反应在PTC-220实时荧光定量PCR仪上进行。分别设计Cx43、Cx37、Cx40、Cx45及Cx46的引物序列进行实验。Cx43上游引物为5'-TTT GAT GGA CCT
GGA GGA AAT C-3',下游引物为5'-TGA GCA
TCC CCT CCA ATA CC-3';Cx37上游引物:5'-ATT AAG GAG CAT
GGC GAC TTC T -3',下游引物:5'-CCC AGG
AGG AAA AGC ATG AG-3';Cx40上游引物:5'-ACA CCA CCC CCC
GAC TTT A-3',下游引物:5'-TTA TTG
CTG AAG GGA TTG AAG AAT T-3';Cx45上游引物:5'-AAT GCT AAG ATC
GCC TAC AAG CA-3',下游引物: 5'-CTC
CTC ATG GCT GCC ATA CTG-3';Cx46上游引物:5'-CAA CAC GGT GGA
CTG CTT CA-3',下游引物 5'-AGG
CCA CCG CCA GCA T-3'。并设计相应的GAPDH上游引物和下游引物,以GAPDH为内参,并用2-∆∆Ct方法计算。
1.4.9 构建Cx43 shRNA慢病毒载体
依据Gene Bank小鼠Cx43基因序列(NC_000076.6),按照RNA干扰序列设计原则,设计4个shRNA干扰靶点Cx43-shRNA-1,Cx43-shRNA-2,Cx43-shRNA-3,Cx43-shRNA-4,并同时设计阴性对照序列。再按照shRNA结构特点,shRNA模板中的loop结构选用了CTCGAG以避免形成终止信号,正义链模板的5'端添加了CCGG,与AgeⅠ酶切后形成的粘端互补;反义链模板的5'端添加了AATT,与EcoR I酶切后形成的粘端互补,设计对应shRNA的DNA正反义链。取相应的正义链和反义链寡核苷酸,在PCR仪上按照如下程序进行退火处理:95 ℃ 5 min;85 ℃ 5 min;75 ℃ 5 min;70 ℃ 5 min;4 ℃保存。退火处理后得到浓度为10 mol/L的shRNA模板。将所得模板溶液稀释50倍,终浓度为200 μmol/L,用于连接反应。将处理好的的目的片段通过T4连接酶将其与AgeⅠ和EcoR I双酶切后的载体Pglv2-U6-Puro链接,4 ℃过夜。连接细菌感受态细胞,涂到含50 mg/L Ampicillin LB平板上培养16 h。从每块平板上挑取5个菌落,接种到含50 mg/L Ampicillin的LB培养基中,37 ℃培养16 h。使用碱裂解法抽提质粒,对抽提好的质粒用EcoR I进行单酶切鉴定后送测序。通过测序对比,挑选序列正确的克隆即为成功构建的Cx43-shRNA重组慢病毒载体。
从液氮中取出冻存的293T细胞,置37 ℃水浴中振摇使细胞快速融化;细胞冻存液加入5-10 mL无血清DMEM培养基,1 000 r/min离心5 min后吸弃上清;用新鲜的完全培养液悬浮细胞后,传至培养皿中培养,待细胞长满后传代;细胞长至单层后倾去培养液;用温的1xPBS洗3次;加入适量胰酶,转动培养皿,使胰酶能浸润全部皿底;显微镜下观察,细胞间的胞间连丝蛋白被消化脱落,细胞呈类圆形,加入含血清培养基终止消化;将细胞吹落,收集进10 mL离心管,600 r/min,5 min离心,弃上清,用新的含血清培养基重悬细胞;按适当比例传代培养。经消化、终止、离心后收集的细胞沉淀,用适量冻存液悬起,1 mL/管分装入冻存管;放入细胞冻存盒中于-80 ℃静置过夜,然后迅速移入液氮中长期保存。
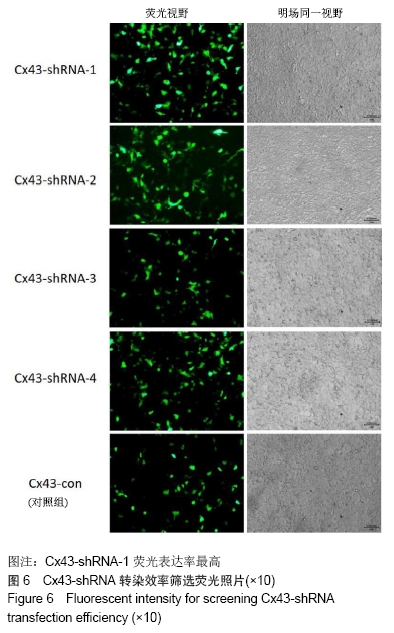
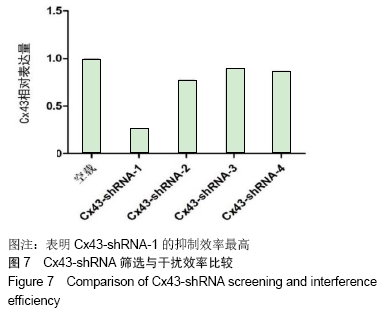
293T细胞感染慢病毒H6373/H145,并筛选稳定表达细胞株。制备293T细胞悬液,血球计数板计数;5 000个细胞/ 24孔,共10个24孔,37 ℃、CO2培养箱培养过夜;当细胞汇合度达到70%时,从-20 ℃冰箱取出Cx43-shRNA质粒(4种)于冰上融化;分别吸取0.8 μg质粒溶于250 μL无抗无血清DMEM,室温放置5 min;吸取20 μL lipo2000溶于2.5 mL无抗无血清DMEM,室温放置5 min;抽取250 μL的lipo2000稀释液加入质粒稀释液中,室温放置30 min;将24孔板中的293T细胞用无抗无血清DMEM 3次;将lipo2000与质粒稀释液加入细胞中,500 μL/孔,37 ℃、CO2培养箱培养4-6 h;换成完全培养基(体积分数10%FBS+DMEM),37 ℃、CO2培养箱培养36 h;荧光显微镜下观察感染效率并拍照,筛选出转染效率高且荧光强的质粒。
将上一步构建出的4段干扰质粒中最有效的shRNA重组到慢病毒表达载体中,进行慢病毒包装。取对数生长期的293T细胞,按照每个10 cm的细胞培养皿5×106细胞接种于细胞培养皿中,于37 ℃、体积分数5% CO2的培养箱中培养过夜。转染前2 h,将细胞培养基更换为Opti-MEM 5 mL。取25 μL Lenti-Easy Packaging Mix加入1 455 μL Opti-MEM (37 ℃预热)中,取60 μL
LipofectAMINETM2000 加入1440 μL
Opti-MEM中,轻轻混匀,室温放置5 min。制备质粒和LipofectAMINETM2000混合物,于37 ℃、体积分数5%CO2的培养箱中孵育。将3 mL质粒脂质体复合物加入到细胞培养皿中,轻轻混匀,于37 ℃、体积分数5%CO2的培养箱中孵育6 h后,将培养基更换为5 mL含50 μL丁酸钠 (110 g/L)的完全培养基,继续于培养箱中孵育6 h后,将培养基更换为10 mL正常完全培养基,继续于培养箱中孵育48 h后,荧光显微镜下观察并拍照,收集细胞培养上清液,离心半径10 cm,1 000 r/min离心5 min,去除细胞残余,留取上清液过滤后,置于-80 ℃保存备用。
选取细胞生长状态良好的293T细胞进行慢病毒滴度测定。病毒稀释用培养基为含有6 mg/L聚酰胺的体积分数10%胎牛血清的细胞培养基。按照每孔5×103细胞接种96孔板,培养至30%-50%的融合密度。转染时用含有体积分数10%胎牛血清的细胞培养基进行梯度稀释,从1×10-1稀释到1×10-7。吸去培养基,混匀各管慢病毒稀释液,各取100 μL加入每孔细胞中,于37 ℃、体积分数5%CO2的培养箱中过夜培养。72 h后,在荧光显微镜下观察各孔中荧光细胞数量,用SYBR Green
I Real Time PCR方法检测人细胞样本中目的基因mRNA转录水平的变化情况。病毒滴度为表达荧光的细胞数乘以相应稀释倍数。
1.4.10 Cx43
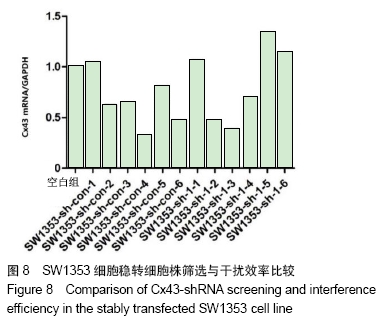
shRNA慢病毒载体转染SW1353细胞并筛选稳转株 制备SW1353细胞悬液,血球计数板计数;细胞铺板:2次分别铺96孔5 000个细胞/孔,24孔15 000个细胞/孔,37 ℃、CO2培养箱培养过夜;当细胞汇合度达到50%时,从-80 ℃冰箱取出转染效率最高的病毒于冰上融化;用无抗无血DMEM以1∶10,1∶100,1∶1 000分别稀释以上病毒,每个96孔分别加入各稀释度的病毒100 μL,每个24孔分别加入各稀释度的病毒500 μL,于37 ℃、CO2培养箱培养过夜后用体积分数10%FBS+DMEM+双抗换液;换液48 h后于荧光显微镜下观察感染效率,选择感染效率高且荧光强的孔,胰酶消化后终止,制备的单细胞悬液600 r/min,离心5 min;配置体积分数10%FBS+DMEM+双抗+嘌呤霉素培养基,用该培养基悬浮细胞沉淀,然后感染96孔的细胞铺96孔板,每个孔的细胞铺半板96孔;感染24孔的细胞铺24孔,每个24孔的细胞铺6个24孔,3-5 d更换新鲜的上述培养基(整个病毒操作过程严格遵照慢病毒操作手册)。挑选荧光强的单克隆孔,胰酶消化,血清终止后,用体积分数10%FBS+DMEM+双抗+嘌呤霉素培养基扩培,直至10 cm培养皿长满,1/3细胞冻存,收1/3细胞沉淀用于Western Blot检测,收1/3细胞沉淀加1 mL trizol混均用于RT-PCR检测,选取检测结果良好的稳转株进行复苏冻存备份。
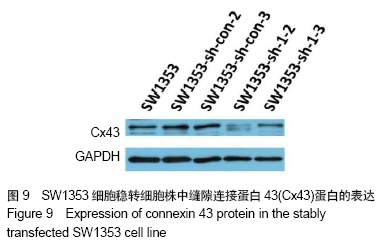
1.4.11 Western Blot检测SW1353细胞稳转细胞株中Cx43蛋白的表达 根据RT-PCR结果,对筛选出的稳转株细胞进行Western
Blot实验。分别收集转染前和转染后的SW1353细胞,并以同代SW1353细胞为空白组,采用BCA protein assay kit试剂盒,分别提取总蛋白。上样,进行SDS-PAGE电泳,电泳结束行电转移,一抗孵育:用3%BSA-TBST稀释一抗(Connexin 43兔多抗,abcam,ab11370,1∶5 000),室温孵育10 min,放4 ℃过夜。二抗孵育:用5%脱脂奶粉-TBST稀释二抗,山羊抗兔IgG(H+L) HRP, 山羊抗小鼠IgG(H+L) HRP,1∶10 000,室温轻摇40 min。胶片曝光:10 s-5 min,显影2 min,定影。孵育内参:加GAPDH鼠单抗,用3%BSA-TBST稀释抗体,1∶20 000稀释,室温孵育2 h。二抗孵育:用5%脱脂奶粉-TBST稀释二抗,山羊抗小鼠IgG(H+L) HRP,室温轻摇40 min。TBST洗膜6次,每次3 min。ECL加到膜上后反应3-5 min,胶片曝光:10 s-5 min,显影2 min,定影。曝光后的胶片直接扫描,软件Image J转变图片格式JPEG为Tif,TotalLab Quant读取条带的积分吸光度(IA)值。
1.5 主要观察指标 ①骨关节炎动物模型中实验侧关节较对照侧关节有更高的国际骨关节炎协会(OARSI)病理学评分;②Cx43在小鼠骨关节炎软骨组织中的表达;③SW1353细胞的培养及嘌呤霉素耐药浓度的筛选;④Cx43、Cx37、Cx40、Cx45、Cx46在SW1353细胞中的表达;⑤Cx43、Cx37、Cx40、Cx45、Cx46在SW1353细胞中的表达;⑥Cx43-shRNA慢病毒载体构建结果;⑦SW1353细胞稳转细胞株的筛选及鉴定结果。
1.6 统计学分析 采用SPSS 17.0软件进行统计分析,两组间比较采用t 检验,多组间比较采用单因素方差分析,P < 0.05为差异有显著性意义。