中国组织工程研究 ›› 2020, Vol. 24 ›› Issue (8): 1149-1154.doi: 10.3969/j.issn.2095-4344.2486
• 软骨组织构建 cartilage tissue construction • 下一篇
原儿茶酸可减轻退变软骨细胞的损伤
占 龙1,孟农钦1,农桔安2,李小峰3,杨 渊4,余 雪5
- 1广西中医药大学,广西壮族自治区南宁市 530000;2南宁市第二人民医院,广西壮族自治区南宁市 530031;3广西骨伤医院,广西壮族自治区南宁市 530012;4广西医科大学附属琅东医院,广西壮族自治区南宁市 530021;5桂林市人民医院,广西壮族自治区桂林市 541000
Protocatechuic acid alleviates degeneration of chondrocytes
Zhan Long1, Meng Nongqin1, Nong Juan2, Li Xiaofeng3, Yang Yuan4, Yu Xue5
- 1Guangxi University of Chinese Medicine; 2the Second Nanning People’s Hospital; 3Guangxi Orthopaedic and Traumatology Hospital; 4Langdong Hospital of Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China; 5Guilin People’s Hospital, Guilin 541000, Guangxi Zhuang Autonomous Region, China
摘要:
文题释义:
原儿茶酸:来源于鳞始蕨科植物乌蕨的叶和冬青科植物冬青的叶,具有抗血小板凝集、降低心肌耗氧量、抑菌、镇痛等多方面药理活性,是一种重要的天然活性物质。近年来的研究发现了其具有抗氧化、抗癌及介导肿瘤细胞凋亡等许多新的药理作用。
软骨细胞:埋藏在软骨间质内的小腔,俗称软骨陷窝。是软骨组织中惟一存在的细胞,在软骨组织分泌蛋白多糖、Ⅱ型胶原的细胞外基质形成致密的结构。其在维持软骨组织的形态和功能上起到重要的作用。
背景:已有研究表明多种抗氧化剂由于对炎性因子存在抑制作用而表现出抗关节炎作用,但是原儿茶酸虽具有抗氧化和抗炎作用,但其是否也对骨关节炎有治疗作用,尚无相关报道。
目的:探讨原儿茶酸在体外对白细胞介素1β诱导炎症的软骨细胞的生物学包括表型和细胞代谢的影响,为骨关节炎疾病提供一种潜在的药物保护手段。
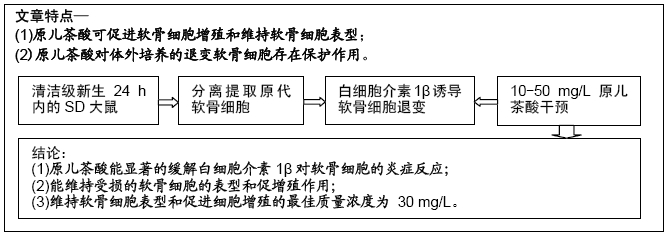
方法:收集乳鼠股骨软骨细胞,以10 mg/L的白细胞介素 1β干预建立退变模型,以10,30和50 mg/L原儿茶酸对细胞进行治疗。实验于2017年10月经广西医科大学动物实验伦理委员会批准,批准号201710008。
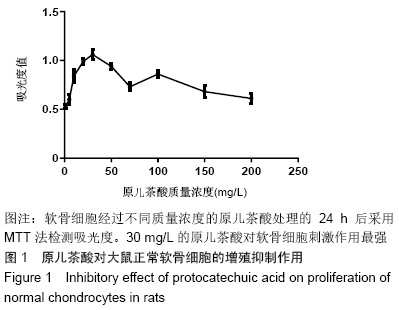
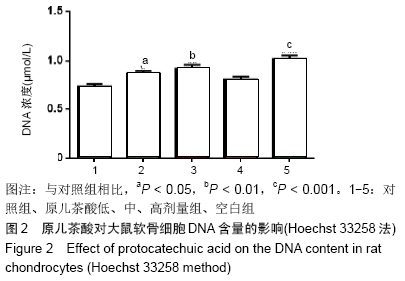
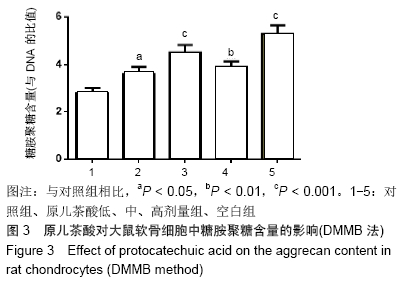
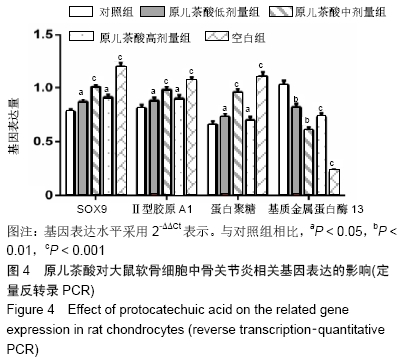
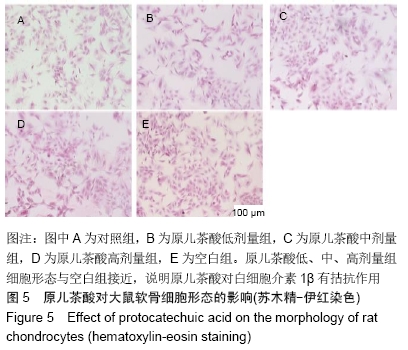
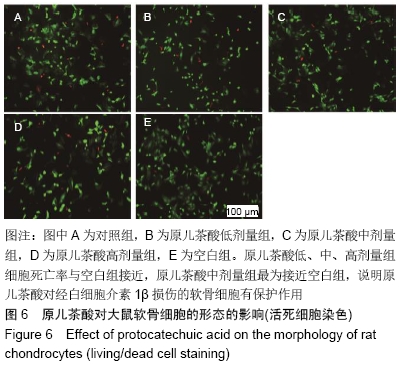
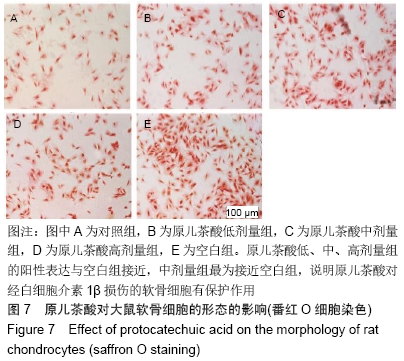
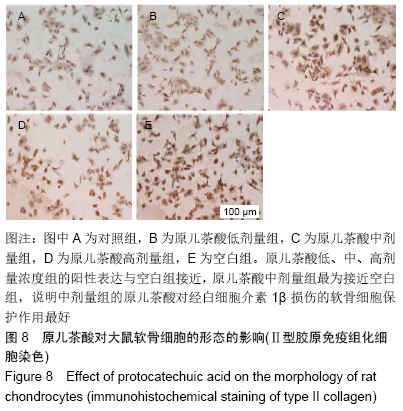
结果与结论:10-50 mg/L原儿茶酸可促进软骨细胞的增殖,其中30 mg/L原儿茶酸对关节软骨细胞的保护作用最强,对退变的关节软骨细胞具有促进增殖的作用,同时原儿茶酸有效促进软骨细胞生长,细胞外基质的合成和聚集蛋白聚糖、Ⅱ型胶原和Sox9的mRNA表达,同时下调炎症相关基因基质金属蛋白酶13的表达。表明原儿茶酸可促进软骨细胞增殖和维持软骨细胞表型,为进一步研究其在体内进行骨关节炎治疗和关节软骨退变损伤修复提供依据。
ORCID: 0000-0002-1075-7969(占龙)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程中图分类号: