中国组织工程研究 ›› 2017, Vol. 21 ›› Issue (4): 551-558.doi: 10.3969/j.issn.2095-4344.2017.04.010
• 口腔组织构建 oral tissue construction • 上一篇 下一篇
人牙周膜成纤维细胞凋亡与体外高糖环境和脂多糖的交互作用
荆 冉1,郭大伟2,廖奕翔3,任伟伟4,仇 静2,陈书兰2
- 1潍坊医学院口腔医学院,山东省潍坊市 261000;2青岛市市立医院口腔科,山东省青岛市 266071;3青岛大学医学院附属青岛市市立医院口腔医学中心,山东省青岛市 266071;4湖北医药学院附属东风口腔医院预防保健科,湖北省十堰市 442000
Interaction of high glucose and lipopolysaccharide on the apoptosis of human periodontal ligament fibroblasts in vitro
Jing Ran1, Guo Da-wei2, Liao Yi-xiang3, Ren Wei-wei4, Qiu Jing2, Chen Shu-lan2
- 1School of Stomatology, Weifang Medical University, Weifang 261000, Shandong Province, China; 2Department of Stomatology, Qingdao Municipal Hospital, Qingdao 266071, Shandong Province, China; 3Center of Stomatology, Qingdao Municipal Hospital Affiliated to Qingdao University Medical College, Qingdao 266071, Shandong Province, China; 4Department of Prevention Dentistry, Dongfeng Stomatological Hospital, Hubei University of Medicine, Shiyan 442000, Hubei Province, China
摘要:
文章快速阅读:
.jpg) 文题释义:
细胞凋亡:也称为程序性的细胞死亡,是机体为了清除损伤的或者不需要的细胞而产生的一种细胞自杀式程序,是最常见的细胞生理性活动,在维持多细胞生物内环境稳定方面有着不可替代的重要作用。在牙周组织正常的新陈代谢过程中,细胞凋亡能够清除受损的或者正在受损的细胞,对保持牙周组织的健康具有非常重要的作用。
交互作用:是指当两种或几种影响因素水平同时作用时的效果较单一水平的影响因素作用效果加强或者减弱的作用。当交互作用存在时,单纯研究某个影响因素的作用是没有意义的,必须分另一个影响因素的不同水平研究该影响因素作用大小。交互作用的分析对于多因素疾病的临床研究具有重要意义。
文题释义:
细胞凋亡:也称为程序性的细胞死亡,是机体为了清除损伤的或者不需要的细胞而产生的一种细胞自杀式程序,是最常见的细胞生理性活动,在维持多细胞生物内环境稳定方面有着不可替代的重要作用。在牙周组织正常的新陈代谢过程中,细胞凋亡能够清除受损的或者正在受损的细胞,对保持牙周组织的健康具有非常重要的作用。
交互作用:是指当两种或几种影响因素水平同时作用时的效果较单一水平的影响因素作用效果加强或者减弱的作用。当交互作用存在时,单纯研究某个影响因素的作用是没有意义的,必须分另一个影响因素的不同水平研究该影响因素作用大小。交互作用的分析对于多因素疾病的临床研究具有重要意义。
.jpg) 文题释义:
细胞凋亡:也称为程序性的细胞死亡,是机体为了清除损伤的或者不需要的细胞而产生的一种细胞自杀式程序,是最常见的细胞生理性活动,在维持多细胞生物内环境稳定方面有着不可替代的重要作用。在牙周组织正常的新陈代谢过程中,细胞凋亡能够清除受损的或者正在受损的细胞,对保持牙周组织的健康具有非常重要的作用。
交互作用:是指当两种或几种影响因素水平同时作用时的效果较单一水平的影响因素作用效果加强或者减弱的作用。当交互作用存在时,单纯研究某个影响因素的作用是没有意义的,必须分另一个影响因素的不同水平研究该影响因素作用大小。交互作用的分析对于多因素疾病的临床研究具有重要意义。
文题释义:
细胞凋亡:也称为程序性的细胞死亡,是机体为了清除损伤的或者不需要的细胞而产生的一种细胞自杀式程序,是最常见的细胞生理性活动,在维持多细胞生物内环境稳定方面有着不可替代的重要作用。在牙周组织正常的新陈代谢过程中,细胞凋亡能够清除受损的或者正在受损的细胞,对保持牙周组织的健康具有非常重要的作用。
交互作用:是指当两种或几种影响因素水平同时作用时的效果较单一水平的影响因素作用效果加强或者减弱的作用。当交互作用存在时,单纯研究某个影响因素的作用是没有意义的,必须分另一个影响因素的不同水平研究该影响因素作用大小。交互作用的分析对于多因素疾病的临床研究具有重要意义。摘要
背景:已有研究表明,高糖和脂多糖在单独作用下都能够促进人牙周膜成纤维细胞的凋亡,但体外培养的人牙周膜成纤维细胞在高糖和脂多糖共同作用下的凋亡行为尚未有相关报道。
目的:通过不同浓度脂多糖影响高糖环境下人牙周膜成纤维细胞,观察细胞增殖、凋亡以及凋亡相关基因Bax和Bcl-2表达的变化。
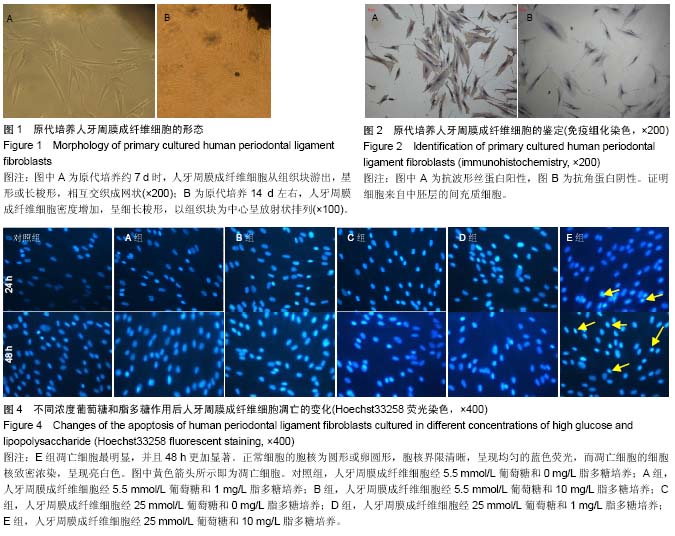
方法:原代培养并鉴定人牙周膜成纤维细胞,5-8代用于后继实验。分别用葡萄糖(5.5,25 mmol/L)和脂多糖(0,1,10 mg/L)作用于细胞24 h及48 h。
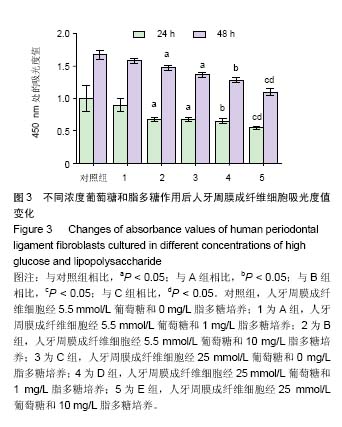
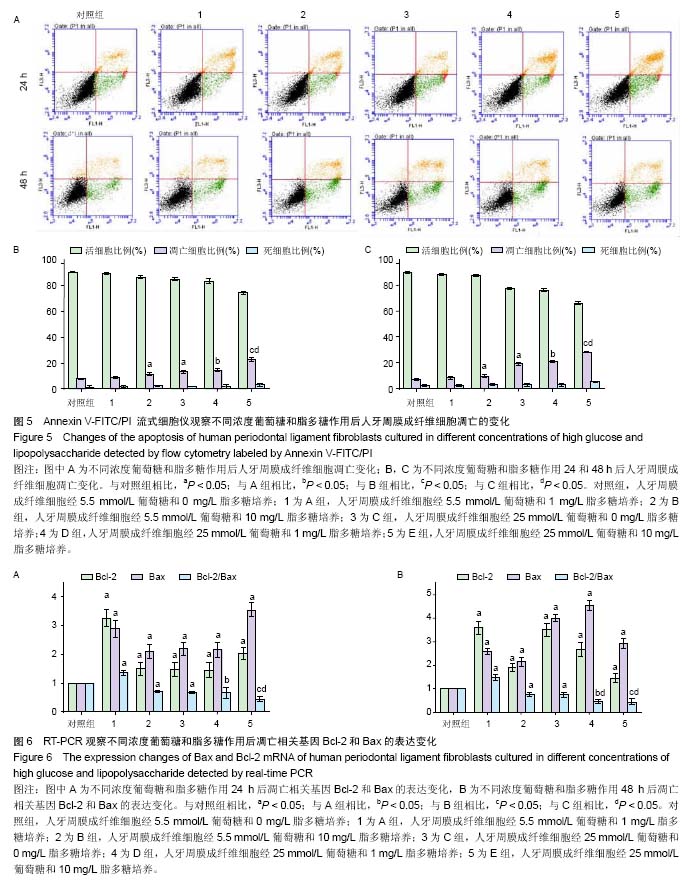
结果与结论:①在正常的葡萄糖浓度(5.5 mmol/L)下,质量浓度为10 mg/L的脂多糖能够显著抑制细胞的增殖(P < 0.05),促进细胞的凋亡(P < 0.05),Bax和Bcl-2 mRNA表达增强(P < 0.05),Bcl-2/Bax的比值显著降低(P < 0.05);②在高糖浓度(25 mmol/L)下,脂多糖诱导的细胞增殖的抑制、细胞凋亡、Bax和Bcl-2 mRNA的表达以及Bcl-2/Bax比值的降低都显著增强(P < 0.05);③方差分析结果显示,高糖和脂多糖在诱导细胞凋亡方面有显著的交互作用(P < 0.05);④结果说明,脂多糖在高糖环境下介导的人牙周膜成纤维细胞增殖的抑制、凋亡及凋亡相关基因Bax和Bcl-2的表达显著增强,脂多糖和高糖在细胞凋亡方面有显著的交互作用。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID: 0000-0003-4977-0695(陈书兰)
中图分类号:
.jpg) 文题释义:
细胞凋亡:也称为程序性的细胞死亡,是机体为了清除损伤的或者不需要的细胞而产生的一种细胞自杀式程序,是最常见的细胞生理性活动,在维持多细胞生物内环境稳定方面有着不可替代的重要作用。在牙周组织正常的新陈代谢过程中,细胞凋亡能够清除受损的或者正在受损的细胞,对保持牙周组织的健康具有非常重要的作用。
交互作用:是指当两种或几种影响因素水平同时作用时的效果较单一水平的影响因素作用效果加强或者减弱的作用。当交互作用存在时,单纯研究某个影响因素的作用是没有意义的,必须分另一个影响因素的不同水平研究该影响因素作用大小。交互作用的分析对于多因素疾病的临床研究具有重要意义。
文题释义:
细胞凋亡:也称为程序性的细胞死亡,是机体为了清除损伤的或者不需要的细胞而产生的一种细胞自杀式程序,是最常见的细胞生理性活动,在维持多细胞生物内环境稳定方面有着不可替代的重要作用。在牙周组织正常的新陈代谢过程中,细胞凋亡能够清除受损的或者正在受损的细胞,对保持牙周组织的健康具有非常重要的作用。
交互作用:是指当两种或几种影响因素水平同时作用时的效果较单一水平的影响因素作用效果加强或者减弱的作用。当交互作用存在时,单纯研究某个影响因素的作用是没有意义的,必须分另一个影响因素的不同水平研究该影响因素作用大小。交互作用的分析对于多因素疾病的临床研究具有重要意义。