中国组织工程研究 ›› 2017, Vol. 21 ›› Issue (4): 559-563.doi: 10.3969/j.issn.2095-4344.2017.04.011
• 口腔组织构建 oral tissue construction • 上一篇 下一篇
正畸牙移动中热休克蛋白70在牙周组织中的表达
聂 晶1,姜 涵2,李泽慧2,潘 旭1,李春霞1
- 新疆医科大学第一附属医院,1口腔正畸科,2牙周粘膜科,新疆维吾尔自治区乌鲁木齐市 830054
Expression of heat shock protein 70 in periodontium during orthodontic tooth movement
Nie Jing1, Jiang Han2, Li Ze-hui2, Pan Xu1, Li Chun-xia1
- 1Department of Orthodontics; 2Department of Periodontics, the First Affiliated Hospital of Xinjiang Medical University, Urumqi 830054, Xinjiang Uygur Autonomous Region, China
摘要:
文章快速阅读:
.jpg) 文题释义:
热休克蛋白:又称应激蛋白,是机体细胞在一些理化因素刺激后高效表达的一组蛋白质,因最先发现于果蝇唾液腺的热应激反应中而得名,广泛存在于人、动物、微生物和植物的细胞中,是一类在遗传上高度保守的分子,能保护细胞并促进细胞对各种刺激所造成的损伤进行自身修复,具有重要的生物学功能。
正畸治疗:主要通过各种矫正装置来调整面部骨骼、牙齿及颌面部的神经及肌肉之间的协调性,也就是调整上下颌骨之间,上下牙齿之间、牙齿与颌骨之间和联系它们的神经及肌肉之间不正常的关系,其最终矫治目标是达到口颌系统的平衡、稳定和美观。
文题释义:
热休克蛋白:又称应激蛋白,是机体细胞在一些理化因素刺激后高效表达的一组蛋白质,因最先发现于果蝇唾液腺的热应激反应中而得名,广泛存在于人、动物、微生物和植物的细胞中,是一类在遗传上高度保守的分子,能保护细胞并促进细胞对各种刺激所造成的损伤进行自身修复,具有重要的生物学功能。
正畸治疗:主要通过各种矫正装置来调整面部骨骼、牙齿及颌面部的神经及肌肉之间的协调性,也就是调整上下颌骨之间,上下牙齿之间、牙齿与颌骨之间和联系它们的神经及肌肉之间不正常的关系,其最终矫治目标是达到口颌系统的平衡、稳定和美观。
.jpg) 文题释义:
热休克蛋白:又称应激蛋白,是机体细胞在一些理化因素刺激后高效表达的一组蛋白质,因最先发现于果蝇唾液腺的热应激反应中而得名,广泛存在于人、动物、微生物和植物的细胞中,是一类在遗传上高度保守的分子,能保护细胞并促进细胞对各种刺激所造成的损伤进行自身修复,具有重要的生物学功能。
正畸治疗:主要通过各种矫正装置来调整面部骨骼、牙齿及颌面部的神经及肌肉之间的协调性,也就是调整上下颌骨之间,上下牙齿之间、牙齿与颌骨之间和联系它们的神经及肌肉之间不正常的关系,其最终矫治目标是达到口颌系统的平衡、稳定和美观。
文题释义:
热休克蛋白:又称应激蛋白,是机体细胞在一些理化因素刺激后高效表达的一组蛋白质,因最先发现于果蝇唾液腺的热应激反应中而得名,广泛存在于人、动物、微生物和植物的细胞中,是一类在遗传上高度保守的分子,能保护细胞并促进细胞对各种刺激所造成的损伤进行自身修复,具有重要的生物学功能。
正畸治疗:主要通过各种矫正装置来调整面部骨骼、牙齿及颌面部的神经及肌肉之间的协调性,也就是调整上下颌骨之间,上下牙齿之间、牙齿与颌骨之间和联系它们的神经及肌肉之间不正常的关系,其最终矫治目标是达到口颌系统的平衡、稳定和美观。摘要
背景:学者们对正畸力作用下牙周组织的改建做了大量的研究,但对于在大鼠牙齿移动过程中热休克蛋白70在牙周组织中表达的研究尚未涉及。
目的:观察在正畸牙移动过程中大鼠牙周组织热休克蛋白70的表达。
方法:采用NiTi拉簧建立大鼠正畸牙移动模型,力值50 g。分别于加力后1,3,5,7,10,14 d检测正畸牙周组织热休克蛋白70的表达。
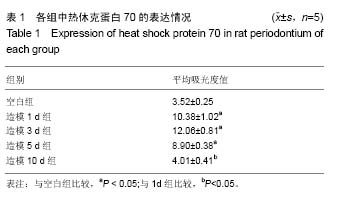
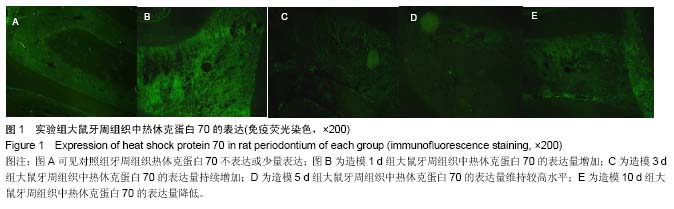
结果与结论:①免疫荧光染色显示,正畸加力1 d,牙周组织中热休克蛋白70的表达量增强,至加力后5 d时表达量最大,之后逐渐降低,第14天时回落至初始水平;②结果说明,正畸力可以刺激牙周组织中热休克蛋白70的表达,热休克蛋白70可能参与了牙周组织的改建。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID: 0000-0001-8173-3430(聂晶)
中图分类号:
.jpg) 文题释义:
热休克蛋白:又称应激蛋白,是机体细胞在一些理化因素刺激后高效表达的一组蛋白质,因最先发现于果蝇唾液腺的热应激反应中而得名,广泛存在于人、动物、微生物和植物的细胞中,是一类在遗传上高度保守的分子,能保护细胞并促进细胞对各种刺激所造成的损伤进行自身修复,具有重要的生物学功能。
正畸治疗:主要通过各种矫正装置来调整面部骨骼、牙齿及颌面部的神经及肌肉之间的协调性,也就是调整上下颌骨之间,上下牙齿之间、牙齿与颌骨之间和联系它们的神经及肌肉之间不正常的关系,其最终矫治目标是达到口颌系统的平衡、稳定和美观。
文题释义:
热休克蛋白:又称应激蛋白,是机体细胞在一些理化因素刺激后高效表达的一组蛋白质,因最先发现于果蝇唾液腺的热应激反应中而得名,广泛存在于人、动物、微生物和植物的细胞中,是一类在遗传上高度保守的分子,能保护细胞并促进细胞对各种刺激所造成的损伤进行自身修复,具有重要的生物学功能。
正畸治疗:主要通过各种矫正装置来调整面部骨骼、牙齿及颌面部的神经及肌肉之间的协调性,也就是调整上下颌骨之间,上下牙齿之间、牙齿与颌骨之间和联系它们的神经及肌肉之间不正常的关系,其最终矫治目标是达到口颌系统的平衡、稳定和美观。