中国组织工程研究 ›› 2016, Vol. 20 ›› Issue (40): 5973-5978.doi: 10.3969/j.issn.2095-4344.2016.40.007
• 脑及脊髓损伤动物模型 Animal models of brain and spinal cord injuries • 上一篇 下一篇
急性马尾神经压迫模型的脊髓组织病理变化
王 展1,李浩鹏2,贺西京2,郝定均3,张 堃1,陈明霞4,雷 霆5
- 西安交通大学医学院附属红会医院,1创伤骨科,3脊柱科,陕西省西安市 710054;2西安交通大学第二临床学院骨二科,陕西省西安市 710003;西安交通大学医学部,4电镜室,5病理教研室,陕西省西安市 710061
Pathological changes in the spinal cord of a model of acute cauda equina compression
Wang Zhan1, Li Hao-peng2, He Xi-jing2, Hao Ding-jun3, Zhang Kun1, Chen Ming-xia4, Lei Ting5
- 1Department of Orthopedic Trauma, 3Department of Spine, Xi’an Honghui Hospital, Health Science Center, Xi’an Jiaotong University, Xi’an 710054, Shaanxi Province, China; 2Second Department of Orthopedics, the Second Clinical College of Xi’an Jiaotong University, Xi’an 710003, Shaanxi Province, China; 4Room of Electron Microscope, 5Department of Pathology, Health Science Center, Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China
摘要:
文章快速阅读:
.jpg) 文题释义:
文题释义:
马尾神经:在脊髓圆锥以下的腰骶神经根称为马尾,由L2-5、S1-5及尾节发出的共10对神经根组成。
马尾神经综合征:由腰骶部骨性结构改变或/和软组织压迫等因素引起,表现为膝关节平面肢体运动、感觉、痛觉、知觉、温度功能障碍,如神经缺血时间过长或并发继发水肿麻痹加重,会导致截瘫。
摘要
背景:动物实验发现,压迫马尾神经可导致腰骶段脊髓前角运动神经元发生凋亡。
目的:观察急性马尾神经压迫后家犬相应脊髓节段组织的病理变化。
方法:将27只犬随机分为9组,每组3组,其中1组为正常对照,7个实验组在L6椎板下硬膜外脂肪上方置入空水囊,进行注水压迫,压迫时间分别设置为4,8,12,24,48,72,168 h;假手术组只置入空水囊,不进行注水压迫。达到压迫时间后,取马尾神经发出段脊髓及相邻头端脊髓,进行组织病理学检查。
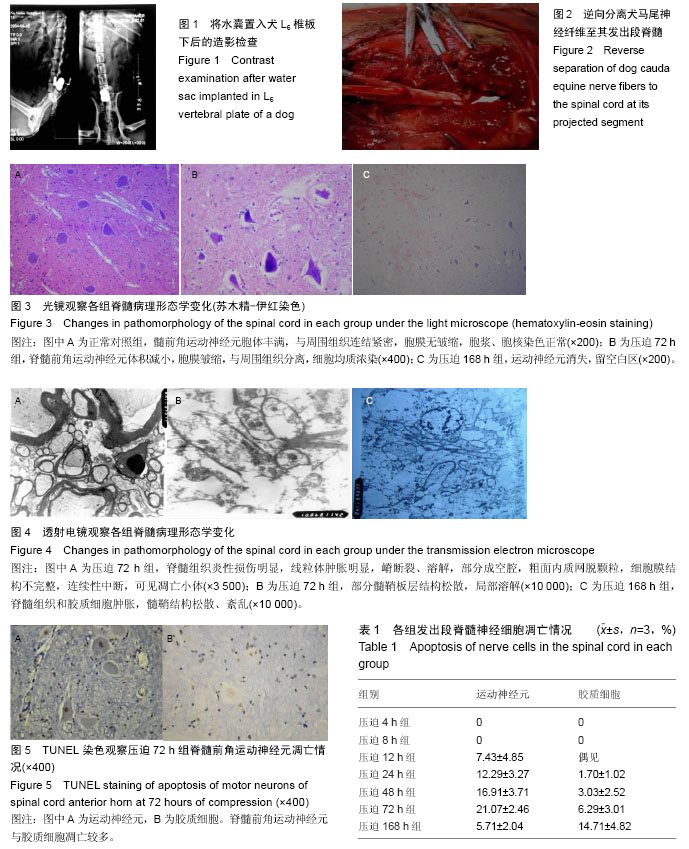
结果与结论:①光镜观察结果:压迫4-48 h,脊髓前角前运动神经元未见明显改变;压迫72 h后,观察到运动神经元体积减小,细胞膜皱缩,与周围组织分离,细胞均质浓染;压迫168 h可见运动神经元消失,但相邻头端脊髓切片未见脊髓前角运动神经元形态异常;②电镜观察结果:压迫12 h,脊髓组织开始肿胀,随压迫时间的延长,脊髓组织肿胀加重,胶质细胞肿胀明显,至168 h时髓鞘板层结构溶解,轴突空泡化,轴浆外溢,有炎性损伤特征样改变;③前角运动神经元凋亡检测结果:压迫12 h开始出现凋亡,随后逐渐增多,至168 h仍呈增高趋势。
中国组织工程研究杂志出版内容重点:肾移植;肝移植;移植;心脏移植;组织移植;皮肤移植;皮瓣移植;血管移植;器官移植;组织工程
ORCID:0000-0002-8010-455X(王展)
中图分类号:
.jpg) 文题释义:
文题释义: