设计:细胞学体外观察实验。
时间及地点:于2013年10月至2014年12月在广州医科大学附属第三医院广东省产科重大疾病重点实验室完成。
材料:
实验动物:雌性免疫缺陷性(severe combined immune deficiency,SCID)小鼠5只,SPF级,8周龄,体质量25-35 g,由北京维通利华实验动物技术有限公司提供。
细胞来源:皮肤成纤维细胞来自广州医科大学附属第三医院基因诊断患者在知情同意条件下自愿捐赠的皮肤组织(已签组织捐赠知情同意书)。正常人的诱导多能干细胞(NHF)和胚胎干细胞(ES-10)由广州医科大学附属第三医院广东省产科重大疾病重点实验室和广东省普通高校生殖与遗传重点实验室干细胞库提供。293T细胞购自中科院上海细胞库。
|
SCA3型诱导多能干细胞系建立和神经分化实验用主要试剂和仪器:
|
|
试剂和仪器
|
来源
|
|
含高糖的DMEM培养基、Knockout-DMEM培养基、血清替代物、谷氨酰胺、β-巯基乙醇、非必需氨基酸、DMEM/F12、Advanced DMEM/F12、胎牛血清、PSC神经诱导培养基
|
Gibco公司
|
|
Matrigel、碱性成纤维生长因子、流式抗体
|
BD公司
|
|
秋水仙素(Colcemid)、吉姆萨染液(Giemsa)、Trizol regent、B27、N2、Accutase、poly-L-ornithine、laminin、Alexa Fluor系列荧光染料标记的二抗
|
Invitrogen公司
|
|
丝裂霉素(mitomycinC)、Triton X-100、一抗
|
Sigma公司
|
|
重编程中使用的反转录病毒:人OKSM质粒
|
美国Stemgent 公司
|
|
Vigofect
|
威格拉斯生物技术有限公司
|
|
DAPI
|
Roche公司
|
|
碱性磷酸酶染色液
|
武汉博士德生物工程有限公司
|
|
光学倒置显微镜、荧光倒置显微镜、共聚焦显微镜
|
Nikon
|
实验方法:
患者皮肤成纤维细胞获取:复苏皮肤成纤维细胞,接种到100 mm培养皿中培养。第2天见细胞贴壁,呈梭形,隔天换液,培养两三天细胞密度达90%以上,可进行传代。
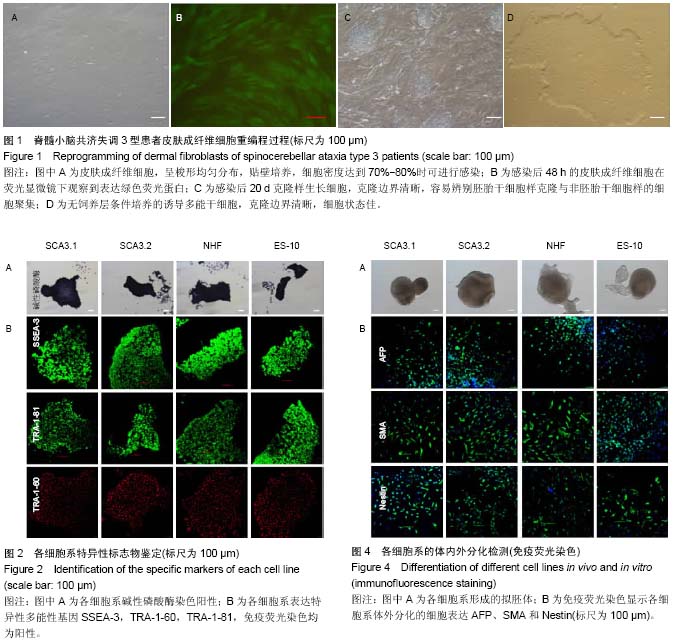
诱导多能干细胞建系:用Vigofect转染试剂盒通过反转录病毒转染系统将转录因子pMx-hOct4、hSox2、hKlf4、hc-Myc转入SCA3患者成纤维细胞中,在人胚胎干细胞培养条件下培养至类似人胚胎干细胞集落形成,感染后21-28 d以形态标准为基础隔离这些克隆。待克隆长大后以物理切割的方式将其传代扩增,将传至第7代的克隆以物理切割的方式铺到matrigel覆盖的无菌培养皿中,用mTeSRTM1继续培养,待克隆长大后以酶消化的方法传代扩增,以后每隔3-5 d传代1次。
碱性磷酸酶检测:第10代诱导性多能干细胞用40 g/L多聚甲醛固定20 min,PBS冲洗3次,加入碱性磷酸酶染色液,避光,室温孵育30 min,光镜下观察结果。
RT-PCR检测Oct4和Nanog基因表达:使用Trizol提取第10代细胞总RNA,反转录成cDNA,RT-PCR检测诱导性多能干细胞中胚胎干细胞标志性基因Oct4和Nanog的表达情况。PCR反应程序:94 ℃预变性5 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸1 min,循环扩增35次,最后72 ℃延伸5 min,PCR产物进行1%琼脂糖凝胶电泳。引物序列:Oct4:5’-GAC AGG GGG AGG GGA GGA GCT AGG-3’,5’-CTT CCC TCC AAC CAG TTG CCC CAA AC-3’;Nanog:5’-CAG CCC CGA TTC TTC CAC CAG TCC-3’,5’-CGG AAG ATT CCC AGT CGG GTT CAC C-3’。
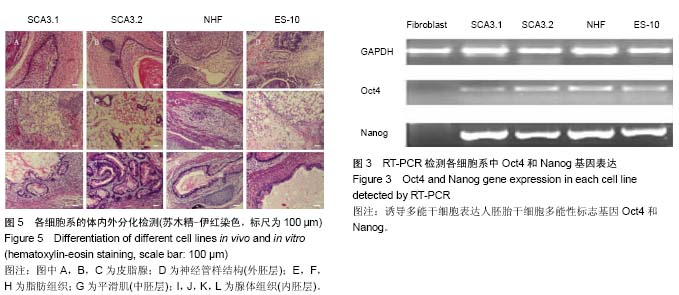
畸胎瘤形成实验检测诱导性多能干细胞的体内分化潜能:当培养在matrigel覆盖的无菌培养皿上SCA3诱导性多能干细胞、正常人的诱导多能干细胞(NHF)和胚胎干细胞(ES-10)至70%密度时,用dispase消化 5-7 min,将细胞团吹下,用DMEM/F12和Matrigel混合液(2∶1)重悬细胞,分别注射到SCID小鼠的后侧大腿内侧皮下(每只小鼠约注射106个细胞),每个细胞系注射1只小鼠。8-10周后,当小鼠腿部的肿块直径超过2 cm时处死小鼠,分离肿块将其置于甲醛溶液中固定,石蜡包埋切片,苏木精-伊红染色 , NikonTi显微镜下观察3个胚层的形成情况。
免疫细胞化学实验:第10代各个细胞系先用40 g/L多聚甲醛固定20 min,然后用PBS洗涤2次,0.1%Triton X-100破膜30 min,用体积分数为1%山羊血清在室温下封闭30 min,PBS洗涤细胞及稀释抗体。细胞在4 ℃下与一抗SSEA-3(1∶1 000)、TRA-1-60(1∶1 000)和TRA-1-81 (1∶1 000)孵育过夜后,用PBS清洗3遍,再与相应二抗在37 ℃下避光孵育120 min,用PBS清洗3遍后,1 g/mL DAPI染细胞核,共聚焦显微镜进行荧光照相。
诱导性多能干细胞拟胚体形成实验:第15代诱导性多能干细胞经1 g/L的dispase消化成细胞团块后,用拟胚体分化液重悬,铺在低吸附的培养皿中,放置在37 ℃,体积分数为5%CO2培养箱内进行培养,隔天更换新鲜培养基,拟胚体分化液为撤去碱性成纤维生长因子的人类胚胎干细胞完全培养基。培养7 d后光学倒置显微镜下观察(×10),然后将拟胚体转换至明胶包被的4孔板内贴壁培养7 d,免疫荧光染色观察三胚层分化情况。
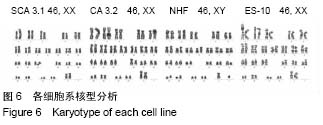
G-带核型分析:第20代诱导性多能干细胞培养第3天,处于对数生长期时,用0.25 g/mL秋水酰胺处理2 h,胰酶消化和离心后,细胞使用低渗液0.075 mol/L KCl 重悬并在37 ℃处理15-30 min,300×g低速离心5 min后,用固定液(冰醋酸∶甲醇=1∶3)轻轻重悬和静置10 min固定,再重复2遍,最后用200 μL固定液重悬细胞沉淀,滴在预冷且干燥的载玻片上,然后70 ℃干燥1 h,G带显示时使用37 ℃预热的0.01%胰酶消化30-60 s,生理盐水清洗后,10%吉姆萨染液染5 min,水洗后风干,对染色体进行分析。
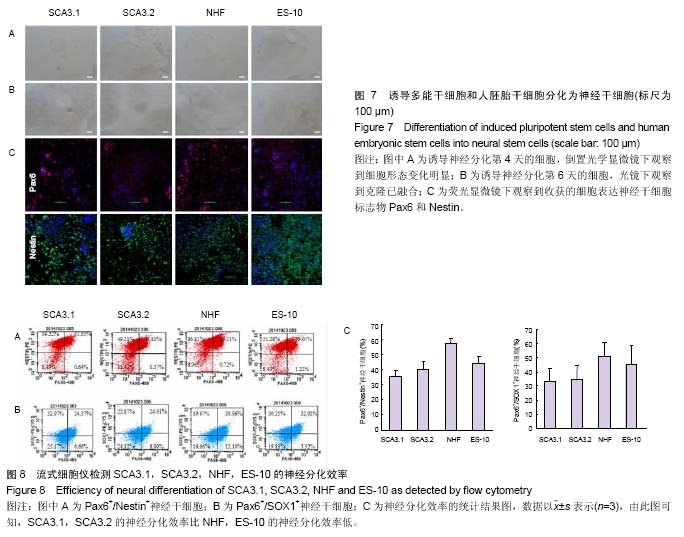
神经干细胞分化:根据诱导性多能干细胞神经诱导的说明书进行,各株细胞(第30代)培养至第4天,克隆密度达70%时,用1 g/L的dispase消化,取3×105个诱导性多能干细胞铺到matrigel覆盖的6孔板里,加入适量的神经干细胞诱导培养基,每孔2.5 mL,隔天换液,第7天收获细胞。
神经元的获得:使用accutase细胞消化液消化第3代的神经干细胞,使用N2培养基重悬细胞,取100 000个细胞铺到多聚鸟氨酸/层粘连蛋白覆盖的6孔板上,第2天换成含有10 μg/L碱性成纤维生长因子的按1︰1比例配制的N2培养基和B27培养基的混合液,隔两三天换液,培养21 d。
流式细胞术分析PAX-NESTIN和PAX-SOX1双阳性细胞比例:用accutase细胞消化液将准备好的第2代神经干细胞消化成单细胞,加入含体积分数为2%胎牛血清的PBS终止消化。离心,弃上清,向离心管加入1×Fix/Perm Buffer在2-8 ℃中避光孵育 40-50 min。用1×Perm/Wash Buffer洗涤2次,离心,弃上清。用1×Perm/Wash Buffer稀释抗体,加到相应的管中,漩涡振荡10 s,在 2-8 ℃中避光孵育40-50 min。用1×Perm/Wash Buffer洗涤2次,离心,弃上清。加入350 μL stain buffer到每个流式管中重悬细胞,上机分析。
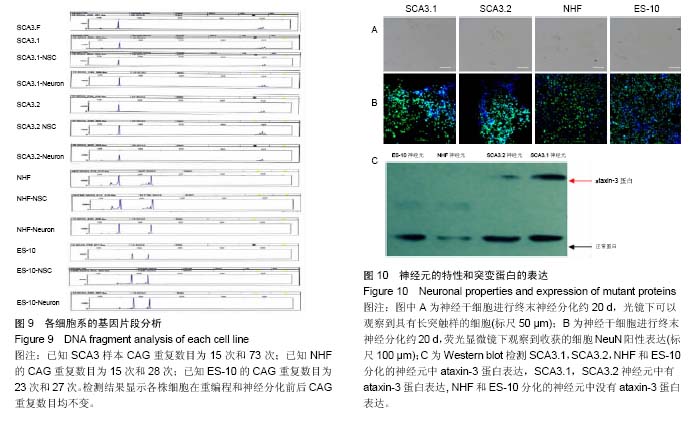
聚合酶链反应检测SCA3/ATXN3基因CAG重复数目:分别提取捐赠者皮肤成纤维细胞、诱导多能干细胞、神经干细胞和神经元的基因组DNA,运用聚合酶链反应及毛细管电泳片段分析,对各个样本进行ATXN3基因CAG重复数检测。
Western blot检测ataxin-3蛋白表达:收集分化第21天的神经元于1.5 mL离心管,用预冷的DPBS洗2次,加含1%PMSF的1×细胞裂解液,冰上裂解30 min,然后离心,收集上清用于测定蛋白浓度和电泳。Western blot分析的实验操作参考标准程序[18],检测ataxin-3蛋白的表达情况。
主要观察指标:①诱导多能干细胞神经分化效率。②诱导多能干细胞神经分化前后CAG拷贝数变化。