中国组织工程研究 ›› 2015, Vol. 19 ›› Issue (19): 3074-3082.doi: 10.3969/j.issn.2095-4344.2015.19.021
• 干细胞综述 stem cell review • 上一篇 下一篇
卵母细胞深低温保存的策略分析
王沛涛,邵翠华,刘海宁
- 青岛大学附属医院,山东省青岛市 266003
-
出版日期:2015-05-06发布日期:2015-05-06 -
通讯作者:王沛涛,博士,教授,主任医师,青岛大学附属医院,山东省青岛市 266003 -
作者简介:王沛涛,男,1965年生,山东省章丘市人,汉族,2005年中国科学技术大学毕业,博士,教授,主任医师,主要从事低温医学、生殖医学研究。 -
基金资助:山东省自然科学基金项目(ZR2010OHMO74):“热休克蛋白超表达在小鼠卵母细胞深低温保存中的作用”
Strategic thinking of human oocyte cryopreservation
Wang Pei-tao, Shao Cui-hua, Liu Hai-ning
- Affiliated Hospital of Qingdao University, Qingdao 266003, Shandong Province, China
-
Online:2015-05-06Published:2015-05-06 -
Contact:Wang Pei-tao, Affiliated Hospital of Qingdao University, Qingdao 266003, Shandong Province, China -
About author:Wang Pei-tao, M.D., Professor, Chief phyhsician, Affiliated Hospital of Qingdao University, Qingdao 266003, Shandong Province, China -
Supported by:the Natural Science Foundation of Shandong Province, No. ZR2010OHMO74
摘要:
背景:卵母细胞具有特殊而复杂的低温生物学性质,致使卵母细胞在深低温保存中易受到多因素的损伤而影响复温后的存活率、受精率和受精后发育潜能。 目的:综述卵母细胞深低温保存技术的研究进展,阐明存在的技术缺陷以及解决问题的思路与研究路线。 方法:以“卵母细胞,深低温保存/慢速冷冻,玻璃化”为中文捡索词,以“oocyte, cryopreservation/slow freezing, vitrification”为英文检索词,在中国知网(CNKI)期刊全文数据库和PubMed数据库检索2004 年1月至2014年10月有关卵母细胞深低温保存文献,排除陈旧性、重复性研究,最终纳入41篇文献进行综述。 结果与结论:慢速冷冻、玻璃化方法深低温保存卵母细胞得到较好的临床应用,但复温存活率、受精能力、发育能力损伤等仍困扰医生们。卵母细胞深低温保存技术的进一步完善或突破在于对深低温保存技术环节的细化、卵母细胞低温生物学特性的研究以及相关技术的创新,如深低温保护剂选择、冷冻载体的改进、卵母细胞时相选择、卵母细胞体外成熟技术、卵巢组织保存与移植等。
中图分类号:
引用本文
王沛涛,邵翠华,刘海宁. 卵母细胞深低温保存的策略分析 [J]. 中国组织工程研究, 2015, 19(19): 3074-3082.
Wang Pei-tao, Shao Cui-hua, Liu Hai-ning. Strategic thinking of human oocyte cryopreservation[J]. Chinese Journal of Tissue Engineering Research, 2015, 19(19): 3074-3082.
2.1 卵母细胞低温生物学特性 卵母细胞具有完全不同于其他体细胞的特征,如体积、细胞核状态和细胞膜成分等;同时,处于不同发育时期的卵母细胞也具有明显不同的生物学特性。卵母细胞这些独特、可变的生物学特性,直接影响到深低温冷冻保存策略的决定,进而影响复温后卵母细胞的存活率和功能[3-4]。一般认为,这些突出的特性包括:卵母细胞体积-表面积比例、膜特性和渗透性能、纺锤体和卵母细胞透明带等。任何致力于提高卵母细胞深低温保存效率和功能的方案,都必须基于对这些细胞特征的全面考虑和评价,才有可能达到理想的保存效果,最大限度地提高卵母细胞存活率和受精发育能力,以及胚胎发育潜能。
2.1.1 卵母细胞的成熟过程 卵母细胞的发育成熟过程较为复杂而漫长,各有不同。根据卵泡的形态和功能可以分为以下时期:始基卵泡(primordial follicles)、初级卵泡(窦前卵泡,preantral follicles)、次级卵泡(窦状卵泡,antral follicles)、囊状卵泡(Graafian follicles)或排前卵泡(preovulatory follicles)。 卵母细胞共经历两次减数分裂过程,即第1次减数分裂(meiosis Ⅰ,MⅠ期)和第2次减数分裂(meiosis Ⅱ,MⅡ期)。减数分裂与卵泡发育同步。第1次减数分裂分为5个时期:细线期(leptotene stage)、偶线期(zygotene stage)、粗线期(pachytene stage)、双线期(diplotene stage)、终变期(diakinesis stage)。第1次减数分裂停留于双线期,也就是休眠期MⅠ前期卵母细胞,也就是囊泡完整卵母细胞(GV-完整的);到女性生殖期时,受促性腺激素的影响,重新开始减数分裂,核膜融解,然后进展为MⅠ期、后Ⅰ期、末期(有丝分裂)、MⅡ期。
2.1.2 卵母细胞低温生物学特点
细胞骨架与纺锤体:基于临床需要,MⅡ期卵母细胞是深低温保存的最早研究对象。此时期卵母细胞的减数分裂纺锤体对染色体重组的保真性、胚胎非整倍体至关重要。纺锤体可以促进MⅡ期细胞染色体的分离和聚集。
减数分裂纺锤体是一个微管蛋白和相关蛋白的动态聚合体,微管/蛋白质解聚合和重聚合过程处于一个持续的流动状态。微管形成一个横跨整个细胞浆的三维纤维网络,当卵泡囊泡破裂时,微管网变得更具活力,并与染色体连接,染色体压缩,形成一个皮质下MⅠ期纺锤体。这一结构辅助第一次减数分离时的染色体分离,促进卵周间隙内第一极体的形成。在成熟MⅡ期,染色体平稳地排列于MⅡ纺锤体的赤道板。这是一个动力结构,其微管发生迅速循环的聚合与解聚,激动蛋白微丝也发挥重要作用,为卵母细胞皮质下减数分裂纺锤体的锚定提供底物。同样,第一极体的凸出,MⅡ纺锤体皮质下的定位保证了精子穿透后的高度非对称性的第二次减数分裂,限制对胚胎发育至关重要的细胞器和分子的丢失。
不是所有时期的卵母细胞具有构架明显的减数分裂纺锤体,其对温度敏感性也大不相同。特殊条件下,纺锤体纤维能够在复温后去极化和重极化,重建与染色体的物理性连接,使其重新定位于赤道板,因此,细胞骨架具有一定的可复性。未成熟卵母细胞的微管不是构建在MⅡ纺锤体内,GV-完整卵母细胞缺乏一个明显的减数分裂纺锤体。研究表明,MⅡ期卵母细胞减数分裂纺锤体对于温度变化极敏感,难以耐受深低温保存中的温度变化而保持结构和功能的完整性。因此,原则上深低温保存未成熟的GV期卵母细胞绕过了染色质发生异常的风险,因为此期的染色质是非压缩的,受到核膜的保护;但是,研究结果提示,保存人类的GV-完整卵母细胞存在困难,成功率低,可能存在其他因素,如细胞膜成分等[1,5]。动物实验研究显示,4 ℃环境下,与MⅠ和MⅡ期卵母细胞相比,分裂终末期小鼠卵母细胞的纺锤体更加稳定;同时,研究观察到,相对于温度的降低,一定的温度提高有利于卵母细胞完成正常的纺锤体重聚合作用,温度的降低可能会打乱这种平衡态,导致部分纺锤体成分解聚合。特征性的深低温损伤是皮质下肌动蛋白网的打破、微管的去极化、纺锤体构架异常和染色体分散。研究证实,降温、低温保护剂、冷冻等可引起纺锤体微管的去极化和破坏。所有这些都会极大改变卵母细胞结构和功能,引起卵母细胞胞浆移动异常,不能正常发育[6]。
只有卵母细胞的细胞骨架结构和功能正常,才能保证染色体正常分离、纺锤体旋转、细胞激酶和前核形成。纺锤体是卵母细胞主要的微管结构,负责减数分裂中卵母细胞空间结构和染色体迁移。目前的相关研究热点是不同减数分裂时期的纺锤体低温生物学特性是否存在差异,如果存在,其微管去极化和再极化的能力如何?除对卵母细胞纺锤体的损伤和破坏,深低温冷冻诱导的损伤还涉及到聚合肌动蛋白组成的卵母细胞微丝和细胞器,如核糖体、高尔基体、线粒体等。微丝调节纺锤体旋转、极体突出、原核迁徙、细胞内分子转运、细胞器和细胞因子的转运等。低温、玻璃化、保护剂等并不改变微丝的极化。有趣的一个现象是,慢速冷冻或玻璃化的微丝损伤可能导致线粒体的分布不正常。深低温保存后卵母细胞的线粒体肿胀能否恢复,或其结果如何尚不清楚。动物实验中观察到,线粒体的非致命性损伤可能会遗传到胚胎,并导致移植后胚胎发育异常,如不能着床、流产、低体质量儿等。一些关注卵母细胞超微结构的精细研究证实,玻璃化后,卵母细胞发生非典型的、细微的线粒体滑面内质网聚集,而慢速冷冻后则正常[7]。
卵细胞膜:细胞膜与细胞的生物学特性直接相关,保持细胞结构与功能完整。细胞膜主要成分是磷脂,还有相关的功能蛋白等。磷脂内的双键数量和位置强烈影响膜特性,这对于细胞的低温生物学特性至关重要。其中胆固醇和聚合不饱和脂肪酸浓度越高,细胞膜更容易保持液态,对降温损伤的敏感性也越低,或者说对低温的耐受能力越强。降温过程中,热能消失,膜脂质双层中的分子运动减弱,相邻脂质分子相互作用,发生膜磷脂的液晶相转变,其特点是脂质分子的高度旋转和侧向运动性,然后高度固体化为晶体胶相,脂质分子的运动被限制,此时的温度称为“转变温度”(Tm),细胞膜含有多种磷脂、聚合不饱和脂肪酸影响转变温度[8]。
在卵母细胞的成熟过程中,其细胞膜成分组成发生快速而明显的变化。从GV到MⅡ期的卵母细胞成熟中,膜成分发生了一定变化,受精后变化更大[9]。合子与处于不同发育期的卵母细胞膜的转变温度值不同,说明它们的组成成分有显著差异。研究发现,成熟人卵母细胞主要含饱和脂肪酸(79.22%),聚合不饱和脂肪酸只有6.5%。Ghetler等研究发现,合子和卵母细胞(不同发育期)的相变温度显著不同。脂质相变(LPT)温度:合子(受精卵)为(10.0±1.2) ℃,成熟卵母细胞为(16.9±0.9) ℃,未成熟卵母细胞为(24.4±1.6) ℃(P < 0.05)。细胞膜电熔合可提高卵母细胞对降温的耐受性,提示膜成分变化能够改变卵母细胞热力学特性和对降温的抵抗能力[10]。
人合子的转变温度低,说明膜对降温损伤具有好的抵抗性,合子的深低温保存广泛用于体外受精治疗,结果满意。人卵母细胞的转变温度显著低于合子,说明对降温损伤敏感度高,GV卵母细胞敏感度最高。实际临床数据证明,慢速冷冻、快速复温方案,常规应用于人合子的深低温保存,室温条件下添加低温保护剂,并开始冷冻程序。这一方案适合人合子的深低温保存,因为合子的转变温度远低于室温(20 ℃),而成熟卵母细胞的转变温度非常接近于室温,此温度下细胞膜可能就发生了部分降温导致的膜相变。高脂质相变温度至少部分能够解释女性配子深低温保存时存活率偏低的原因。Lim 等证实,牛单细胞合子深低温保存复温存活率和发育能力优于MⅡ卵母细胞;而且,MⅡ卵母细胞的慢速冷冻后的存活率和发育率好于GV卵母细胞。有研究发现,改变细胞膜的脂质成分也可以提高细胞对降温损伤的耐受性,如:向细胞膜内嵌入脂质体。增加母羊饮食中的聚合不饱和脂肪酸能够改变卵母细胞的脂肪酸含量,细胞膜的物理学特性发生变化,转变温度从15 ℃降低到4 ℃,提示对于降温损伤的耐受能力会提高[11]。玻璃化是目前保存MⅡ卵母细胞的最好方法,根据其降温冷冻过程的各项技术参数看,玻璃化绕过由细胞膜相变带来的降温或冷冻损伤,因此才获得比慢速冷冻、快速复温更高的存活率[8]。
卵丘细胞:GV-完整卵母细胞无明显的减数分裂纺锤体,遗传物质被限制在核被膜内,因此,深低温保存此时期的卵母细胞可以无需考虑纺锤体的保护,利于建立高效的卵母细胞深低温保存方法。但是,早期的研究提示,保存人类的GV-完整卵母细胞困难,成功率低,原因就是卵丘细胞的存在。
卵丘细胞包绕卵母细胞,并协同代谢作用。卵丘细胞发出丰富的微丝,并穿过透明带而与卵膜直接连接。在接触部位,卵丘细胞与卵母细胞通过缝隙连接发生交流。缝隙连接似乎对于小体积卵丘细胞因子、代谢物和信号分子的转运至关重要,这些物质是未成熟卵母细胞进行减数分裂,获得充分细胞浆成熟和发育完成所必需的条件。
从GV到MⅡ期,膜成分发生了一定变化,受精后变化更大,这种变化可能由于受精时皮质颗粒细胞的胞吐作用所致。MⅡ期卵母细胞不依赖于周围卵丘细胞的支持,因此,深低温保存中是否能够保证这些细胞的存活力并不影响卵母细胞的结构与功能,可以忽略其存在而仅对卵母细胞进行有效保护即可。相反,GV期卵母细胞的深低温保存则必须考虑如何最大化保护卵丘细胞及其与卵母细胞之间的通信连接功能,确保复温后两种细胞之间仍能通过透明带实现相互作用,这对于卵母细胞成熟是必需的。首先,必需保证卵丘细胞在深低温保存后存活。这是在筛选和优化深低温保存方案时必需考虑的条件,因为卵母细胞和卵丘细胞之间体积差别大,对冷冻保护剂敏感性明显不同;其次,必需保证深低温保存后透明带结构和功能完整性,而透明带对深低温保存敏感性非常高。低温保护剂毒性、保存中温度变化导致的机械应力及渗透压改变等都会损伤或破坏卵母细胞-卵丘细胞连接,直接导致透明带微管和微丝构架的断裂,卵丘细胞与卵母细胞间不能进行正常的信息因子的传递与交流[12-13]。
毫无疑问,未成熟卵母细胞对于低温保护剂的通透性不仅依赖于膜脂质成分和皮质微丝网络,还依赖于其体细胞构成的“外衣”。但是,此方面研究报道不一致。一些报道认为保存卵丘细胞活力,可以使冷冻保护剂在降温中更加平稳渗透,避免复温中冷冻保护剂移出导致的过快的渗透压变化,提高卵母细胞存活率和受精率[8]。另有报道认为,卵丘细胞无保护作用,干扰冷冻保护剂通过卵浆;而且,构建卵丘细胞和卵母细胞间的功能连接,易化卵丘细胞间信息交流的细胞内接触,在冷冻中可能成为启动邻近细胞间冰晶形成的成核点。但是,纵然卵丘细胞不利于GV卵母细胞的深低温保存,但对于其后的体外成熟也是绝对不能缺少的。所有这些考虑都说明在未成熟卵丘卵母细胞复合体深低温保存中维持透明带的重要性。因此,非成熟期卵母细胞的深低温保存方案的设计有更多因素需要考虑,并在技术环节中实现突破[14]。
目前,玻璃化MⅡ卵母细胞效果比较可靠,但GV卵母细胞的存活率为55%-75%。适合卵母细胞存活的深低温方案并不能同时实现对卵丘细胞的有效保护,复温后GV卵丘细胞存活率低,或不能继续发育成熟[1,15]。
2.2 深低温保存卵母细胞现状 依据降温速率的不同,生物活性材料的冷冻保存方法可分为2种:慢速冷冻(亦称程控降温冷冻)和超速冷冻(亦称玻璃化)。综合目前卵母细胞冷冻保存的相关研究结果,玻璃化冷冻较程控降温冷冻更适合于卵母细胞的深低温保存。但无论哪种方法,各有不同的技术优势和缺陷,都会对复温后卵母细胞的结构和功能产生不同层面的影响和损害。
2.2.1 慢速冷冻(程控降温冷冻) 程控降温冷冻是传统细胞与组织深低温保存技术,目前临床多用于精子、各种干细胞、角膜、血管和心瓣膜等的深低温保存。该技术方法较为成熟,保存效果完全可以满足研究与临床治疗的需要。早在1986年,研究人员就报道了采用慢速冷冻-复温方法,成功深低温保存卵母细胞,并获得胚胎和妊娠[7]。
程控降温冷冻方法是通过控制差异性的降温速率,分段完成细胞或组织的降温冷冻过程。通过不同速率的降温步骤,达到水、电解质、低温保护剂的细胞内外移动、平衡的目的,在冷冻体相变及降温冷冻时,最大限度减少冰晶的形成,降低冰晶对细胞或组织的损伤,并最终达到稳定的超低温状态(如-195.8 ℃的液氮),长期贮存,复温后获得良好的细胞和组织活性。这种深低温保存技术的关键在于细胞脱水和降温速率的控制。细胞的脱水是通过对低温保护剂添加的控制来实现的。大体上,根据低温保护剂的保护性能特点,将其分为2大类:渗透性低温保护剂、非渗透性低温保护剂。前者主要包括二甲基亚砜、甘油、乙二醇、丙二醇等,对细胞有极强的渗透性,结合细胞内水分子,抑制冰晶的形成。后者主要包括多种单糖(果糖、葡萄糖)、多糖(蔗糖、海藻糖)、聚合物和胶体(聚乙烯吡咯烷酮)、羟乙基淀粉、血浆、白蛋白等,这些物质不能透过细胞膜,但可以对细胞产生较大渗透压效应,促进细胞内水分的流出,降低降温冷冻中冰晶形成可能性;同时,对于细胞膜稳定性发挥作用,提高其对于低温及其他损伤因子的耐受能力。此两类物质的组合产生不同的深低温保护效应,降低细胞或组织的冷冻损伤,因此,是深低温保存生物活性材料的关键环节。根据低温生物学基本原理,程序控制降温技术中,低温保护剂浓度相对较低,多采用1.0-1.5 mol/L的甘油或二甲基亚砜,其他渗透性保护剂有乙二醇、丙二醇;非渗透性保护剂蔗糖、葡萄糖、果糖等。样本降温到-5至-7 ℃时,冷平衡并种冰,诱导细胞外的冰形成,然后慢速降温到-30 ℃以下,投入液氮中保存。此技术过程关键点是种冰和慢速降温冷冻,使细胞有充分的时间最大限度脱水,避免或减少细胞内损伤性冰晶的形成,而达到一种近似玻璃化的状态[16]。丙二醇的蔗糖混合物低温保护剂用于卵母细胞保存研究中,人们发现,蔗糖浓度由0.1 mol/L提高到0.3 mol/L,卵母细胞的存活率、受精率和分裂率会明显升高,但植入率却会降低。并发现高浓度蔗糖冷冻后,卵母细胞中的空泡现象严重,因而影响了植入率[17]。
世界首例冷冻卵母细胞获得临床妊娠和出生婴儿即采用慢速冷冻方法复温后的卵母细胞,之后得到广泛推广和研究。但目前慢速冷冻技术在临床应用已较少,通过大量研究和临床观察,人们发现慢速冷冻方法保存卵母细胞的冷冻效果不理想,复温后卵母细胞的存活率不高,体外受精率低,受精后的发育率也不满意[18-19]。
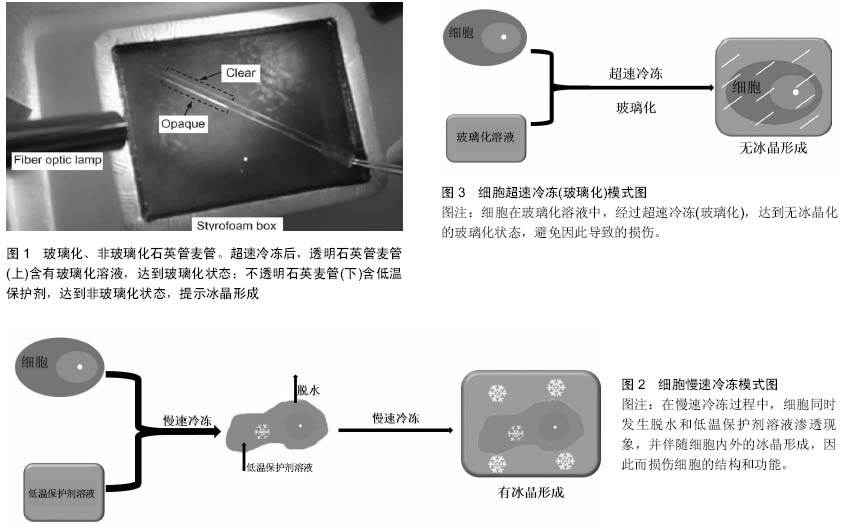
2.2.2 超速冷冻(玻璃化) 超速冷冻即玻璃化。顾名思义,玻璃化是一种均质的、非晶体化状态。玻璃化冷冻体中,生物样本在极高的低温保护剂浓度、超快的降温速率(> 2 000 ℃/min)条件下,瞬间转变为非晶体化的玻璃态,无冰晶形成,因此消除了慢速冷冻技术中主要的损伤因素——冰晶形成;另一方面,在这种极速玻璃化冷冻过程中,细胞内外电解质、水分子等基本不发生流出或流入现象,冷冻后保持了冷冻前的分布状态,避免了由于渗透压、电解质浓度的剧烈变化而导致的渗透性休克的发生,减少了细胞损伤。
玻璃化、慢速冷冻方法比较,见图1-3。
然而,要实现细胞或组织保存的玻璃化冷冻,需要具备特殊的条件:第一,极高浓度的玻璃化溶液;第二,超速降温速率。首先,极高的玻璃化溶液浓度意味着高浓度的低温保护剂,黏度越高,玻璃化倾向越大,越易于实现样本玻璃化,而降低冰晶形成的概率。为此,人们进行了大量的实验研究和观察,已经建立的较为成熟的玻璃化方法中,玻璃化的冷冻保护剂浓度高达 4-6 mol/L,为多种低温保护剂的混合液(如:乙二醇、二甲基亚砜、聚乙二醇等)和非渗透性保护剂(如蔗糖等)。其次,超速降温速率对玻璃化细胞的存活率至关重要,但实现高降温速率途径主要有两种,第一种途径是将生物样品直接投入液氮中(-195.8 ℃),依据样本的大小、包装等,降温速率在数百至数万℃/min;另一种方法是液态氮泥(约-210 ℃),降温速率会明显提高,较液氮提高2-6倍,但实现起来有一定技术难度。第2种途径是缩小样本体积。体积越小,降温过程中的传热、传质越迅速,有利于玻璃化实现,对此,研究人员在玻璃化冷冻载体研制方面进行了大量实验,设计了多种体积小的玻璃化载体。主要的玻璃化载体分为两大类:表面技术和管技术。表面技术包括电镜铜网(EM grid)、微滴胶(minimum drop size,MDS)、冷冻薄膜(Cryotop)、冷冻环(Cryoloop)、半麦管(Hemi-straw)、固体表面玻璃化冷冻(solid surface)、尼龙网(nylon mesh)、冷冻叶片(Cryoleaf)、光纤栓(fiber plug)、冷冻勺(vitrification spatula)、塑料刀片(plastic blade)和玻璃化(Vitri-Inga)。管技术包括塑料麦管(plastic straw)、开放式拉长麦管(OPS)、封闭式拉长麦管(closed pulled straw)、弹性聚酯剥离吸管(flexi pet-denuding pipette)、超细开放式拉长麦管、冷冻尖管(CryoTip)、吸管尖(pipette tip)、高安全性玻璃化装置冷冻(high-security vitrification device)、热封细管(sealed pulled straw)、冷冻细管(Cryopette)和JY麦管(JY Straw)。前者降温、复温速率快,后者具有更高的安全性、易操作性[16]。
目前,应用于卵母细胞玻璃化保存的技术操作相对简单,玻璃化溶液和载体都已经商品化,已经成为胚胎冷冻、卵母细胞冷冻的首选方法。大量研究报道,玻璃化冷冻后的卵母细胞,复温后的卵母细胞受精后发育潜力、妊娠率和优质胚胎率、移植率等主要指标与新鲜卵母细胞无明显差异[20],第1例玻璃化卵母细胞怀孕是在1999年,之后直到2003年玻璃化研究方法取得显著进展,日本研究人员采用特殊的结构装置获得快速冷冻速率,显著降低冷冻损伤效应,并且获得高卵母细胞存活率和受孕率,复温后存活率达91%,胚泡期发育达50%。玻璃化已经成为供卵库常规方法。玻璃化卵母细胞最高存活率报道达96.9%,目前的受精率几乎与新鲜卵母细胞相等(76.3%︰82.2%)。怀孕率据报道达65.2%,植入率40.8%。在西班牙,最大组的前瞻性随机对照研究中,包括600个卵母细胞受体,未证实新鲜的卵母细胞比玻璃化的库存卵母细胞有更大优势[21-24]。
2.2.3 两种保存方法的比较 综合复温后卵母细胞的各项结构与功能指标,玻璃化保存优于慢速冷冻保存方法。结构损伤包括透明带硬化、纺锤体打乱、细胞骨架破坏等;功能指标如复温后卵母细胞存活率、受精率、卵裂率和着床妊娠率等[24]。
一项随机对照研究中,玻璃化48例,慢速冷冻30例,两组卵母细胞的存活率、受精率、临床妊娠率分别为81%︰67%、 84%︰71%、38%︰13%,且玻璃化卵母细胞受精后胚胎发育形态完整性好于慢速冷冻组,两组的流产率相同[25]。Cobo等[26]综合分析了5项研究报道,共有4 282个玻璃化卵母细胞,3 524个新鲜卵母细胞,361个慢速冷冻卵母细胞。结果发现,玻璃化卵母细胞与新鲜卵母细胞的怀孕率、高质量胚胎数、胚胎分裂和受精等无差异;与慢速冷冻相比,玻璃化卵母细胞存活率高(OR=2.46,95%CI 1.82-3.31),受精率高(22.4%︰8%,OR=3.32,95%CI 1.37-8.02),胚胎分裂率高(D2:64.6%∶47.7%,OR=2.00,95%CI 1.33- 3.00;D3: 53%︰33.3%,OR=2.25,95%CI 1.32-3.85)。Luciano等[27]在对猫GV卵母细胞的慢速冷冻和玻璃化冷冻对照研究发现,80%慢速冷冻卵母细胞的微管在胞浆内同质分布,微丝在膜下轻微凝聚;玻璃化则导致细胞骨架分布不均、胞浆内聚集;同时发现,两种方法冷冻后细胞间缝隙连接减少,玻璃化卵母细胞与体细胞间连接破坏更明显,而慢速冷冻卵母细胞较玻璃化卵母细胞的成熟能力更高。这一结果验证了慢速冷冻时冷冻保护剂渗透性平衡作用,抑制了渗透性休克的发生或程度,而玻璃化时的高浓度冷冻保护剂则增加了化学毒性作用。有学者试图从基因水平解释玻璃化冷冻优于慢速冷冻的现象。Monzo等[28]将慢速冷冻和玻璃化冷冻的卵母细胞解冻后,采用基因芯片技术分析复温后卵母细胞的部分基因表达情况,结果显示,慢速冷冻的卵母细胞染色体稳定基因KIF2C和KIF3A及细胞周期蛋白CHEK2和CDKN1B表达水平下调,而这些基因的下调可能损伤卵母细胞的发育潜能;玻璃化冷冻的卵母细胞泛素化特定肽酶和26S酶亚基等泛素化基因表达下调,此类基因的下调有助于维持母体蛋白的稳定,促进卵母细胞的发育。
慢速冷冻方法操作方法复杂、繁琐,其中关键环节是“冷平衡”操作过程;玻璃化方法操作相对简单,无“冷平衡”过程[7]。然而,仅仅从方法学上判定慢速冷冻与玻璃化的差别过于简单化,也是错误的。慢速冷冻中,细胞内水逐渐移到细胞外,种冰后细胞外冷冻,而细胞内发生玻璃化;玻璃化过程中,细胞在高浓度的玻璃化介质中完成脱水后,细胞内外的成分玻璃化。与慢速冷冻需要的复杂的控温设备不同,玻璃化条件简单,甚至可以在野外条件完成,当然玻璃化操作的样本装载或装入需要熟练的专业技术操作才能准确完成[16,29]。
当前,玻璃化技术比较热门,那么是否意味着没有人在做慢速冷冻了呢?答案是否定的,因为,实际卵母细胞深低温保存操作工作中,还要结合各自实验室和程序特殊性。例如:如果需要短时间内完成多个患者,数十个卵母细胞的深低温保存,冷冻速率要求极高的玻璃化操作实现起来会有相当的困难,而程控降温冷冻可能更合适,会有充裕的时间完成卵母细胞清洗、胞浆内单精子注射和其他显微操作等[30]。另一方面,有学者发现,多数比较慢冻与玻璃化的研究中,采用的慢速冷冻中的蔗糖浓度为0.3 mol/L,因为此浓度下有较好的存活率、受精率和卵裂率,但其植入率和临床妊娠率低,因此不能据此认为慢速冷冻方法劣于玻璃化,应该在对慢速冷冻方法进行改进或调整的基础上,进行更多的随机对照研究,才能获得更可靠的对比结果。而且,目前临床缺乏比较两种方法的前瞻性随机研究,因此,需要更严格设计实验研究,才能更全面比较和评价两种技术在人类卵母细胞深低温保存中的优势与不足[17,25]。
2.3 未来展望
2.3.1 深低温保存方案的优化与改良
低温保护剂的选择:低温保护剂的共同特点是高水溶性和毒性,其毒性与浓度和温度正相关。深低温保存中,既要保证细胞脱水充分且适度,又要最大限度降低保护剂浓度,减少毒性[31]。有研究者采用超快速玻璃化冷冻[22],以低浓度的丙二醇(1.5 mol/L)和海藻糖或蔗糖(0.5 mol/L)为冷冻保护剂、石英毛细管为冷冻载体、液氮泥为冷冻剂冷冻鼠卵母细胞,结果冻融卵可以达到超过90%的存活率,受精率和囊胚形成率与新鲜卵母细胞无明显差别,这种新型的冷冻方法为传统玻璃化方案的改进提供了参考。另外,最近有研究报道,在玻璃化冷冻液中添加一种多肽类抗冷冻蛋白(AFP),可以提高卵母细胞存活率、复温后受精率和胚胎发育率,卵母细胞的包膜、纺锤体和染色体形态受到较少破坏[24]。
降温速率控制:冷冻载体的改进以提高冷冻速率为目的,最大限度实现样品的均质化的快速降温或复温,提高保存效果。当前,对于使用何种玻璃化容器最好,何种渗透性和非渗透性低温保护剂的组合最有效地支持卵母细胞深低温保存和长期安全性方面,存在广泛争论。研究表明,所有的玻璃化容器都可以,使用效果高度依赖操作技术。选择满足需要和常规要求的玻璃化容器,并广泛实践,这样就能保证效果。早期玻璃化冷冻常采用开放式拉长麦管或电子显微镜网格作为冷冻载体, 目前常用的玻璃化冷冻载体包括CryoLeaf、CryoTop、CryoLoop 等,CryoTop能产生50 000 ℃/min的降温速率。
深低温保存技术流程:卵母细胞移入、移出低温保护剂,都会导致细胞环境的极大变化,细胞最直接的变化就是随着水、电解质、低温保护剂等成分的出入而发生的收缩与膨胀。细胞骨架空间走向、细胞浆性细胞器发育时期特异性的分布,如线粒体对细胞功能至关重要。相应的问题是:在细胞收缩和膨胀过程中,这些结构与细胞器是否位置发生变化?是否影响胚胎的发育能力?对此,有人设想了一种微液性玻璃化装置:浓度梯度增加式的玻璃化液体流过细胞,而不是细胞通过液体,这样就可以提供一种自动化方法将低温保护剂以一种浓度递增方式传递给细胞;低温保护剂的去除过程与之相反[7]。
2.3.2 卵母细胞的低温生物学特性及修饰
卵母细胞分裂时相与纺锤体:冷冻的卵母细胞多选用MⅡ期卵母细胞,但是成熟卵纺锤体对温度变化很敏感,易造成纺锤体损伤,导致出现异常染色体概率增加。理论上认为冷冻未成熟卵(GV 期、MⅠ)更具有优势。不是所有时期的卵母细胞的纺锤体都具有对温度的相同敏感性。研究显示,与MⅠ和MⅡ期卵母细胞相比,后Ⅰ期小鼠卵母细胞在4 ℃时维持更稳定的纺锤体10 min。据报道,2 h内获得的卵母细胞慢速冷冻后,胚胎质量、怀孕和植入率较2 h后冷冻的卵母细胞高,主要是因为卵母细胞在排卵前获取,它们的最后成熟在体外完成。有丝分裂后期卵母细胞显示一个极体。这些卵母细胞的一部分在获取后2 h内仍处于有丝分裂后Ⅰ期,冷冻是合理可行的。未成熟胚泡卵尚未形成纺锤体,膜通透性高,较MⅡ卵母细胞抵抗深低温保存损伤的能力强。报道的慢速冷冻复温存活率为37%-63%。但是,发现复温后纺锤体异常,说明也存在冷冻损伤[14,21]。
早期的研究提示,保存人类的GV-完整卵母细胞困难,成功率低。卵丘细胞的存在是影响因素之一,因为它们促进卵母细胞成熟,但是适合卵母细胞存活的深低温方案不能有效保护卵丘细胞存活。目前玻璃化GV卵母细胞的存活率在55%-75%之间。当然,有效的体外卵母细胞成熟也是一个GV-卵母细胞深低温保存的前提条件。几项研究检验了几种药学化合物的应用,如紫杉醇,能够影响减数分裂纺锤体的稳定性而提高细胞的低温耐受能力[1,32]。
研究表明,在玻璃化前行体外卵母细胞成熟,然后玻璃化效果可能更好。未成熟卵母细胞应该在体外卵母细胞成熟后的MⅡ期行玻璃化,因为未成熟期卵母细胞玻璃化后的卵母细胞成熟率明显降低。Cao等[33]研究了体外卵母细胞成熟前后人卵母细胞玻璃化的效果,结果显示,GV期和MⅡ期卵母细胞的存活率差异无显著性意义;但是,成熟率有显著性差异,GV期卵母细胞明显低于对照组。有进一步的研究报道,可以从卵巢组织中获取中窦期卵泡,行体外成熟后,玻璃化或慢速冷冻深低温保存,此类卵泡体外成熟后的平均成熟率可达56.3%-79%。卵巢组织冷冻保存与移植取得一定发展,但临床资料有限,同时对于恶性疾病女性的卵巢或卵巢组织移植,可能发生移植复发。因此,对于如血液恶性疾病患者卵巢,只能在排除卵巢转移风险后方可移植,如通过免疫缺陷鼠试验性移植验证,也可采用体外成熟获得成熟卵母细胞。当然,卵巢组织深低温保存技术、成熟卵母细胞体外成熟技术有待突破[21]。
降温过程中,热能的消除降低了膜脂质活动性,相邻脂质分子之间建立了不同的相互作用。在“相变温度”时,膜改变其流动性,从液体状态转变成结晶玻璃态。转变温度值与冷抵抗力相关,转变温度越低,抗冻力越强。Kim等[34]利用傅里叶变换红外分光镜研究体外和未成熟GV卵母细胞人受精卵的转变温度差异发现,人类受精卵的转变温度大约在10 ℃,远低于室温,这就解释了受精卵对抗冷损伤的原因;而未受精卵母细胞的转变温度明显高于此温度,成熟和未成熟卵母细胞转变温度分别为16.9 ℃和24.4 ℃。这可以说明,与受精卵相比,卵母细胞抗冻力低,也就是说容易受到降温冷冻的冲击损伤,复温后的存活率低。
基于这一概念,理想的卵母细胞深低温保存方案可以考虑通过人工加入脂质体的方法改变膜构成,提高对细胞深低温保存忍耐性能力的改进。有研究报道,喂养富有聚合不饱和脂肪酸饲料,可以改变羊卵膜的构成和物理特性,并证实其卵母细胞转变温度明显降低,对冷损伤的耐受力提高[9,35];另外一种方法是,使用某些降温时保护卵母细胞膜完整性的物质,如Isachenko等发现,卵黄在冷冻前和冷冻后都对小鼠卵母细胞和卵丘细胞完整性有积极作用。这一效果尚未得到完全解释,可能因素:第一,卵黄能够作为卵母细胞的外衣,隔离低温保护剂与卵膜的直接接触,降低冷冻时盐溶液导致的卵母细胞的渗透性休克;第二,卵黄的某些成分可能整合进入了卵膜,降低了向胶冻样状态转变的趋势。卵黄是一种自然的非完全性确定的复合混合物:磷脂和抗氧化剂,不能应用于人卵母细胞深低温保存,但是,它仍然是未来发现新脂质产品,并用于帮助保护卵丘复合体冷冻保存研究的一个好的起点[1,36]。
另有报道,与体内成熟卵母细胞相比,体外成熟人卵母细胞的卵膜结合水通道蛋白含量降低。因此,培养条件可能是膜低温保护剂通透能力降低的原因,并增加了体外成熟卵的深低温保存损伤敏感性。通过对玻璃化复温后胚胎发育监测发现,注射水通道3cRNA可以提高鼠卵母细胞膜水通道蛋白3表达,增加水通透性,并帮助改善深低温耐受能力[37-38]。
| [1] Clark NA, Swain JE. Oocyte cryopreservation: searching for novel improvement strategies. J Assist Reprod Genet. 2013; 30(7):865-875.
[2] Noyes N, Boldt J, Nagy ZP. Oocyte cryopreservation: is it time to remove its experimental label. J Assist Reprod Genet. 2010; 27(2-3):69-74.
[3] Ruffing NA, Steponkus PL, Pitt RE, et al. Osmometric behavior, hydraulic conductivity, and incidence of intracellular ice formation in bovine oocytes at different developmental stages. Cryobiology. 1993;30(6):562-580.
[4] Zeron Y, Pearl M, Borochov A, et al. Kinetic and temporal factors influence chilling injury to germinal vesicle and mature bovine oocytes. Cryobiology. 1999;38(1):35-42.
[5] Gomes CM, Silva CA, Acevedo N, et al. Influence of vitrification on mouse metaphase II oocyte spindle dynamics and chromatin alignment. Fertil Steril. 2008;90(4 Suppl): 1396-1404.
[6] Gomes C, Merlini M, Konheim J, et al. Oocyte meiotic-stage- specific differences in spindle depolymerization in response to temperature changes monitored with polarized field microscopy and immunocytochemistry. Fertil Steril. 2012; 97(3): 714-719.
[7] Smith GD, Motta EE, Serafini P. Theoretical and experimental basis of oocyte vitrification. Reprod Biomed Online. 2011; 23(3): 298-306.
[8] Ghetler Y, Yavin S, Shalgi R, et al. The effect of chilling on membrane lipid phase transition in human oocytes and zygotes. Hum Reprod. 2005;20(12):3385-3389.
[9] Zeron Y, Sklan D, Arav A. Effect of polyunsaturated fatty acid supplementation on biophysical parameters and chilling sensitivity of ewe oocytes. Mol Reprod Dev. 2002;61(2): 271-278.
[10] Matorras R, Ruiz JI, Mendoza R, et al. Fatty acid composition of fertilization-failed human oocytes. Hum Reprod. 1998;13(8): 2227-2230.
[11] Lim JM, Fukui Y, Ono H. The post-thaw developmental capacity of frozen bovine oocytes following in vitro maturation and fertilization. Theriogenology. 1991;35:1225-1235.
[12] Vandevoort CA, Shirley CR, Hill DL, et al. Effects of cryoprotectants and cryopreservation on germinal vesicle-stage cumulus-oocyte complexes of rhesus monkeys. Fertil Steril. 2008;90(3):805-816.
[13] Ruppert-Lingham CJ, Paynter SJ, Godfrey J, et al. Developmental potential of murine germinal vesicle stage cumulus-oocyte complexes following exposure to dimethylsulphoxide or cryopreservation: loss of membrane integrity of cumulus cells after thawing. Hum Reprod. 2003; 18(2):392-398.
[14] Brambillasca F, Guglielmo MC, Coticchio G, et al. The current challenges to efficient immature oocyte cryopreservation. J Assist Reprod Genet. 2013;30(12):1531-1539.
[15] Toth TL, Baka SG, Veeck LL, et al. Fertilization and in vitro development of cryopreserved human prophase I oocytes. Fertil Steril. 1994;61(5):891-894.
[16] Saragusty J, Arav A. Current progress in oocyte and embryo cryopreservation by slow freezing and vitrification. Reproduction. 2011;141(1):1-19.
[17] Dovey S. Oocyte cryopreservation: advances and drawbacks. Minerva Ginecol. 2012;64(6):485-500.
[18] 王瑶,狄文. 卵子冷冻技术的应用进展[J].上海交通大学学报:医学版,2013,33(8):1171-1175.
[19] 高明,章志国,曹云霞. 人类卵子冷冻技术的进展[J]. 国际生殖健康/计划生育杂志,2013,32(6):475-477.
[20] Solé M, Santaló J, Boada M, et al. How does vitrification affect oocyte viability in oocyte donation cycles? A prospective study to compare outcomes achieved with fresh versus vitrified sibling oocytes. Hum Reprod. 2013;28(8): 2087-2092.
[21] Rodriguez-Wallberg KA, Oktay K. Recent advances in oocyte and ovarian tissue cryopreservation and transplantation. Best Pract Res Clin Obstet Gynaecol. 2012;26(3):391-405.
[22] Cai LB, Qian XQ, Wang W, et al. Oocyte vitrification technology has made egg-sharing donation easier in China. Reprod Biomed Online. 2012;24(2):186-190.
[23] Siano L, Engmann L, Nulsen J, et al. A prospective pilot study comparing fertilization and embryo development between fresh and vitrified sibling oocytes. Conn Med. 2013;77(4): 211-217.
[24] 陈春华,李萍,宋岳强. 卵子冷冻研究进展[J].生殖与避孕,2014, 34(4):311-316.
[25] Smith GD, Serafini PC, Fioravanti J, et al. Prospective randomized comparison of human oocyte cryopreservation with slow-rate freezing or vitrification. Fertil Steril. 2010; 94(6):2088-2095.
[26] Cobo A, Diaz C. Clinical application of oocyte vitrification: a systematic review and meta-analysis of randomized controlled trials. Fertil Steril. 2011;96(2):277-285.
[27] Luciano AM, Chigioni S, Lodde V, et al. Effect of different cryopreservation protocols on cytoskeleton and gap junction mediated communication integrity in feline germinal vesicle stage oocytes. Cryobiology. 2009;59(1):90-95.
[28] Monzo C, Haouzi D, Roman K, et al. Slow freezing and vitrification differentially modify the gene expression profile of human metaphase II oocytes. Hum Reprod. 2012;27(7): 2160-2168.
[29] Herrero L, Martínez M, Garcia-Velasco JA. Current status of human oocyte and embryo cryopreservation. Curr Opin Obstet Gynecol. 2011;23(4):245-250.
[30] Boldt J. Current results with slow freezing and vitrification of the human oocyte. Reprod Biomed Online. 2011;23(3): 314-322.
[31] Swain JE, Smith GD. Cryoprotectants. In: Cihian RC, Quinn P, editors. Fertility cryopreservation. Cambrige: Cambridge University Press, 2010:24-39.
[32] Morató R, Izquierdo D, Albarracín JL, et al. Effects of pre-treating in vitro-matured bovine oocytes with the cytoskeleton stabilizing agent taxol prior to vitrification. Mol Reprod Dev. 2008;75(1):191-201.
[33] Cao Y, Xing Q, Zhang ZG, et al. Cryopreservation of immature and in-vitro matured human oocytes by vitrification. Reprod Biomed Online. 2009;19(3):369-373.
[34] Kim JY, Kinoshita M, Ohnishi M, et al. Lipid and fatty acid analysis of fresh and frozen-thawed immature and in vitro matured bovine oocytes. Reproduction. 2001;122(1):131-138.
[35] Zeron Y, Tomczak M, Crowe J, et al. The effect of liposomes on thermotropic membrane phase transitions of bovine spermatozoa and oocytes: implications for reducing chilling sensitivity. Cryobiology. 2002;45(2):143-152.
[36] Isachenko EF, Nayudu PL. Vitrification of mouse germinal vesicle oocytes: effect of treatment temperature and egg yolk on chromatin and spindle normality and cumulus integrity. Hum Reprod. 1999;14(2):400-408.
[37] Van den Abbeel E, Schneider U, Liu J, et al. Osmotic responses and tolerance limits to changes in external osmolalities, and oolemma permeability characteristics, of human in vitro matured MII oocytes. Hum Reprod. 2007; 22(7):1959-1972.
[38] Yamaji Y, Seki S, Matsukawa K, et al. Developmental ability of vitrified mouse oocytes expressing water channels. J Reprod Dev. 2011;57(3):403-408.
[39] ACOG: Committee Opinion No. 584: oocyte cryopreservation. Obstet Gynecol. 2014;123(1):221-222.
[40] Borini A, Coticchio G. The efficacy and safety of human oocyte cryopreservation by slow cooling. Semin Reprod Med. 2009;27(6):443-449.
[41] Cil AP, Seli E. Current trends and progress in clinical applications of oocyte cryopreservation. urr Opin Obstet Gynecol. 2013n;25(3):247-254.
|
| [1] | 林清凡, 解一新, 陈婉清, 叶振忠, 陈幼芳. 人胎盘源间充质干细胞条件培养液可上调缺氧状态下BeWo细胞活力和紧密连接因子的表达[J]. 中国组织工程研究, 2021, 25(在线): 4970-4975. |
| [2] | 蒲 锐, 陈子扬, 袁凌燕. 不同细胞来源外泌体保护心脏的特点与效应[J]. 中国组织工程研究, 2021, 25(在线): 1-. |
| [3] | 张秀梅, 翟运开, 赵 杰, 赵 萌. 类器官模型国内外数据库近10年文献研究热点分析[J]. 中国组织工程研究, 2021, 25(8): 1249-1255. |
| [4] | 王正东, 黄 娜, 陈婧娴, 郑作兵, 胡鑫宇, 李 梅, 苏 晓, 苏学森, 颜 南. 丁酸钠抑制氟中毒可诱导小胶质细胞活化及炎症因子表达增多[J]. 中国组织工程研究, 2021, 25(7): 1075-1080. |
| [5] | 汪显耀, 关亚琳, 刘忠山. 提高间充质干细胞治疗难愈性创面的策略[J]. 中国组织工程研究, 2021, 25(7): 1081-1087. |
| [6] | 万 然, 史 旭, 刘京松, 王岩松. 间充质干细胞分泌组治疗脊髓损伤的研究进展[J]. 中国组织工程研究, 2021, 25(7): 1088-1095. |
| [7] | 廖成成, 安家兴, 谭张雪, 王 倩, 刘建国. 口腔鳞状细胞癌干细胞的治疗靶点及应用前景[J]. 中国组织工程研究, 2021, 25(7): 1096-1103. |
| [8] | 谢文佳, 夏天娇, 周卿云, 刘羽佳, 顾小萍. 小胶质细胞介导神经元损伤在神经退行性疾病中的作用[J]. 中国组织工程研究, 2021, 25(7): 1109-1115. |
| [9] | 李珊珊, 郭笑霄, 尤 冉, 杨秀芬, 赵 露, 陈 曦, 王艳玲. 感光细胞替代治疗视网膜变性疾病[J]. 中国组织工程研究, 2021, 25(7): 1116-1121. |
| [10] | 焦 慧, 张一宁, 宋雨晴, 林 宇, 王秀丽. 乳腺癌类器官研究进展及临床应用前景[J]. 中国组织工程研究, 2021, 25(7): 1122-1128. |
| [11] | 王诗琦, 张金生. 中医药调控缺血缺氧微环境对骨髓间充质干细胞增殖、分化及衰老的影响[J]. 中国组织工程研究, 2021, 25(7): 1129-1134. |
| [12] | 曾燕华, 郝延磊. 许旺细胞体外培养及纯化的系统性综述[J]. 中国组织工程研究, 2021, 25(7): 1135-1141. |
| [13] | 孔德胜, 何晶晶, 冯宝峰, 郭瑞云, Asiamah Ernest Amponsah, 吕 飞, 张舒涵, 张晓琳, 马 隽, 崔慧先. 间充质干细胞修复大动物模型脊髓损伤疗效评价的Meta分析[J]. 中国组织工程研究, 2021, 25(7): 1142-1148. |
| [14] | 侯婧瑛, 于萌蕾, 郭天柱, 龙会宝, 吴 浩. 缺氧预处理激活HIF-1α/MALAT1/VEGFA通路促进骨髓间充质干细胞生存和血管再生[J]. 中国组织工程研究, 2021, 25(7): 985-990. |
| [15] | 史洋洋, 秦英飞, 吴福玲, 何 潇, 张雪静. 胎盘间充质干细胞预处理预防小鼠毛细支气管炎[J]. 中国组织工程研究, 2021, 25(7): 991-995. |
最佳的卵母细胞深低温保存程序不应该仅仅局限于经验性的积累,而应该建立在对卵母细胞低温生物学特性与深低温保存技术的系统研究和综合评价基础之上的独有方案[1-2],但目前卵母细胞深低温保存仍然存在许多技术瓶颈,一方面,深低温保存基础研究进展不大,如在低温保护剂、温度控制等方面,近年来无突破性发现和进展;另一方面,卵母细胞深低温保存技术多是以经验性研究为基础而建立的,缺乏系统、科学的研究与认识,因而难以建立有效、稳定的深低温保存技术方案。
本综述分别从卵母细胞低温生物学特性、低温保存技术研究进展两个方面,综合分析与评价相关研究资料,阐述当前卵母细胞深低温保存技术特点,探讨卵母细胞深低温保存技术的策略,提出进一步改进和完善卵母细胞深低温保存技术的研究思路与可行性途径。
1.1 资料来源 由第一作者使用计算机检索截止到2014年12月PubMed数据库及中国知网数据库。英文检索词为“cryopreservaton, vitrification, oocyte”,中文检索词为“深低温保存,玻璃化、卵母细胞”。
1.2 资料筛选及评价
纳入标准:①文章所述内容为卵母细胞深低温保存基础与应用研究文献。②同一领域选择选择近期发表或在权威杂志上发表的文章。
排除标准:与纳入标准无关,陈旧性文献,重复性文献。
1.3 资料提取与文献质量评价 计算机检索得到301篇文献,阅读标题和摘要进行初筛,排除中英文文献重复报道以及与纳入标准无关的文献。查阅全文,最后保留41篇文献做进一步分析。
卵母细胞低温生物学特性和低温生物学技术是卵母细胞深低温保存方法建立的基础,卵母细胞深低温保存方法的评价为保存技术提出改进方向和目标,推动该技术在生殖医学领域的不断进步与创新。一方面,针对卵母细胞生物学特性的低温生物学基础研究有待于进一步探索,包括低温保护剂选择、降温速率控制、冷冻载体的研制等;另一方面,针对卵母细胞本身的选择和修饰方法,可以有效改变卵母细胞的低温生物学特性,提高对低温损伤的耐受性。同时,有关卵母细胞发育的重要机制研究不断发展,研究人员要评价与深低温保存相关的这些细胞功能的常态性,优化技术方法,提高卵母细胞和胚胎深低温成功率[7]。可以肯定,卵母细胞深低温保存技术已经在辅助生殖技术中得到广泛应用,每一种研究尝试都应该避免或减少卵母细胞深低温保存的损伤,提高有效性和安全性[17]。
1此问题的已知信息:卵母细胞深低温保存技术是辅助生殖技术的重要组成,但目前临床采用深低温保存方案差异性较大,也导致了保存结果存在不确定性。 2 文章增加的新信息:从深低温保存基本原理技术和卵母细胞的低温生物学特性两方面,综合国内外相关研究资料,对深低温保存技术进行了系统理论阐述,并针对目前卵母细胞深低温保存中存在的技术缺陷进行分析,提出未来研究的可行途径与思路。 3 临床应用的意义:帮助临床生殖实验室操作人员了解深低温保存基本理论技术原理,结合卵母细胞低温生物学特性,系统开展卵母细胞深低温保存及其他相关技术(如卵巢组织保存等),建立高效、稳定的卵母细胞深低温保存技术方案。
卵母细胞保存技术的关键在于最大限度提高存活率与功能完整性,也是研究与关注的热点。任何该技术环节的突破都具有重要的理论与实践意义。如:低温保护剂类型和/或不同低温保护剂组合、降温与复温速率与方法的调控、细胞低温生物学特性的研究或修饰、冷冻载体发明与使用等。目前,生殖医学科相关技术的发展与突破,极大刺激了对深低温保存技术的需求,但由于两个领域理论与技术的差异,导致发展的不平衡,在两种技术的密切结合性系统研究方面不足,卵母细胞深低温保存技术方案多来自于经验性的积累,限制了卵母细胞深低温保存技术的研究与发展。本文从低温生物学理论技术角度,阐述分析卵母细胞相关低温生物学特性,结合目前卵母细胞深低温技术现状,寻求克服目前保存技术缺陷、提高保存效率的理论支持,提出未来卵母细胞深低温技术的可行突破环节与思考。
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||