2.1 基因治疗的定义 基因治疗是指将外源正常基因导入靶细胞,以纠正或补偿因基因缺陷和异常引起的疾病,以达到治疗目的。也就是将外源基因通过基因转移技术将其插入患者的适当的受体细胞中,使外源基因制造的产物能治疗某种疾病。从广义说,基因治疗还可包括从DNA水平采取的治疗某些疾病的措施和新技术。
基因治疗有广义和狭义之分,广义的基因治疗指把某些遗传物质转移到患者体内,使其在体内表达,最终达到治疗某种疾病的方法;狭义的基因治疗也是通常所说的基因治疗,是指用具有正常功能的基因置换或增补患者体内有缺陷的基因,因而达到治疗疾病的目的,它又可分为体内基因治疗和体外基因治疗。
2.2 基因治疗的分类
2.2.1 按基因操作 一类为基因修正和基因置换,即将缺陷基因的异常序列进行矫正,对缺陷基因精确地原位修复,不涉及基因组的其他任何改变。通过同源重组即基因打靶技术将外源正常的基因在特定的部位进行重组,从而使缺陷基因在原位特异性修复。另一类为基因增强和基因失活,是不去除异常基因,而通过导入外源基因使其表达正常产物,从而补偿缺陷基因等的功能;或特异封闭某些基因的翻译或转录,以达到抑制某些异常基因表达。
2.2.2 按靶细胞 又可分为生殖细胞基因治疗和体细胞基因治疗。广义的生殖细胞基因治疗以精子、卵子和早期胚胎细胞作为治疗对象。由于当前基因治疗技术还不成熟,以及涉及一系列伦理学问题,生殖细胞基因治疗仍属禁区。在现有的条件下,基因治疗仅限于体细胞,包括淋巴细胞类,肿瘤细胞,干细胞,肌细胞,皮肤或纤维细胞等。
2.2.3 按给药途径
活体外途径:指将含外源基因的载体在体外导入人体自身或异体细胞(或异种细胞),经体外细胞扩增后,输回人体。活体外途径基因转移途径比较经典、安全,而且效果较易控制,但是步骤多、技术复杂、难度大,不容易推广。
活体内途径:将外源基因装配于特定的真核细胞表达载体,直接导入体内。这种载体可以是病毒型或非病毒性,甚至是裸DNA。活体内途径基因转移途径操作简便,容易推广,但目前尚未成熟,存在疗效持续时间短,免疫排斥及安全性等一系列问题。
2.3 间充质干细胞的基因治疗
2.3.1 间充质干细胞作为靶细胞基因治疗的优势和缺陷 间充质干细胞是属于中胚层的一类多能干细胞,主要存在于结缔组织和器官间质中,以骨髓组织中含量最为丰富。具有以下特性:①间充质干细胞相对容易获取、易于分离、培养、扩增和纯化,多次传代扩增后仍具有干细胞特性。②间充质干细胞能够像胚胎干细胞一样可分化为三胚层不同类型的细胞。③间充质干细胞在动物体内会有较少的排斥反应[1]。④间充质干细胞体外增殖能力较强,可以多次传代培养。⑤间充质干细胞可以与周围的细胞形成缝隙连接,从而有利于间充质干细胞与周围其他细胞间小分子以及离子的互相渗透[2]。⑥间充质干细胞来源广泛,骨髓、脂肪以及脐带血等中都可以分离获得间充质干细胞,体外扩增性强,具多向分化潜能,外源基因易于植入,并可整合到间充质干细胞的基因组中稳定表达,是细胞治疗和基因治疗的理想靶细胞。⑦间充质干细胞有望成为代替神经干细胞和胚胎干细胞成为理想的组织工程种子细胞,用于干细胞基因治疗[3-4]。⑧目前有许多研究尝试用不同的细胞充当细胞载体,包括免疫细胞,肿瘤细胞和间充质干细胞等[5-8]。由于间充质干细胞具有免疫原性低,且取材方便,容易大量扩增等特点,是一种较理想的病毒细胞载体。⑨间充质干细胞本身低表达甚至不表达主要组织相容性分子和某些共刺激分子从而具有低免疫原性,因此在进入同种异体后不发生排斥反应而容易被宿主接受[9-10],同时间充质干细胞还具有特异性向肿瘤组织迁移的特点。如Khakoo等[11]报道通过尾静脉进入小鼠体内的人骨髓来源的间充质干细胞能够到达皮下形成的卡波西肉瘤组织,Kidd等[12]运用活体内生物发光跟踪技术清晰直观的记录了间充质干细胞向肿瘤组织选择性趋化的特性。⑩2004年,Le Blanc等报道了间充质干细胞治疗移植物抗宿主病不需要严格的配型。此外体内外研究表明,关于间充质干细胞迁移和增殖的具体调控机制目前尚不清楚;干细胞具有不易转染的特性,利用普通质粒表达载体无法达到理想的转染效率,因而无法对干细胞中某种蛋白的功能进行分析研究[13];间充质干细胞的低存活率、移植物植入和分化限制了其临床应用[14];但是在实际应用过程中,间充质干细胞在发挥其自身功能时,往往会受到环境条件的影响[15-16]。
2.3.2 间充质干细胞基因治疗各种疾病及具体操作的差别 最初基因治疗的临床研究是1995年由Lazarus等进行的,他们收集缓解期血液肿瘤患者的自体间充质干细胞,在体外扩增培养4-7周,然后再静脉注射入患者体内,注射后没有观察到毒副作用,提示间充质干细胞用于移植治疗安全可靠[14]。
目前利用间充质干细胞作为基因治疗载体的新策略已经展示了较好的预期效果,如Gao等[17]利用慢病毒包装系统制备的色素上皮衍生因子修饰的骨髓来源间充质干细胞在体内体外实验中均展示了较好的抑制肝癌细胞生长和转移的能力。
Kucerova等[18]联合利用胞嘧啶脱氨酶修饰的脂肪来源间充质干细胞和前体药物5-氟胞嘧啶有效抑制了体内肿瘤模型中大肠癌的发展。
Seo等[19]报道白细胞介素12修饰的间充质干细胞能够明显的激活小鼠体内肿瘤特异性的T淋巴细胞反应和抗肿瘤效应。
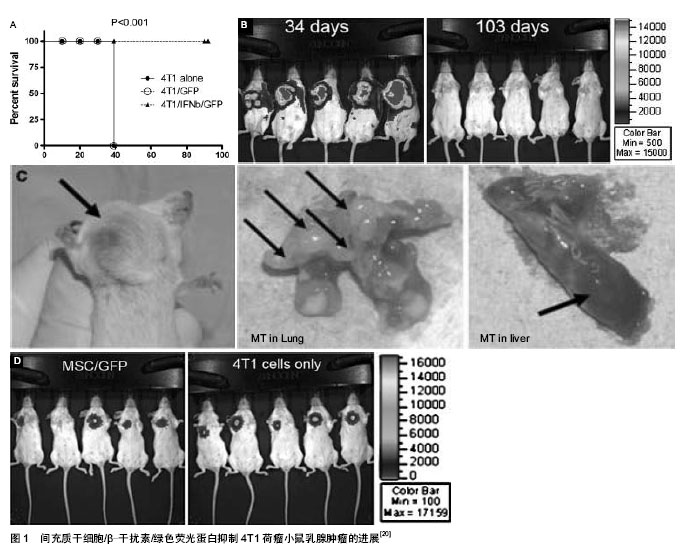
Ling等[20]的结果表明β-干扰素修饰的间充质干细胞能够在具有正常免疫系统的小鼠体内抑制乳腺癌细胞的增殖和转移(图1)。
孟昊等[21]采用基因敲除骨桥蛋白-/-型模式小鼠骨髓间充质干细胞,分子实验技术检测结果显示骨桥蛋白基因在调控间充质干细胞促进糖尿病创面愈合中的作用,为糖尿病慢性创面的临床治疗提供新思路。
Saka等[22]报道使用反转录病毒将绿色荧光蛋白转染至兔自体骨髓间充质干细胞,再移植到兔退变椎间盘中,移植后48周可以通过荧光标记更直观地观察间充质干细胞增殖与分化情况,证实了间充质干细胞移植是一种有效的治疗方法。
随后国内樊守刚[23]、Chen[24]、Miyamoto[25]均在各自的干细胞治疗椎间盘退变的研究中运用此项示踪技术,其意义在于基因与干细胞联合应用明显提升了椎间盘修复能力。
李华壮等[26]利用腺病毒载体在体外对骨髓间充质干细胞进行人转化生长因子β1基因修饰,再移植到兔退变椎间盘中,12周后,X射线结果显示移植组椎间隙狭窄明显抑制,免疫组织化学提示蛋白多糖、Ⅱ型胶原积聚较对照组明显增多。
许运等[27]报道运用慢病毒载体成功使SOX9基因修饰的骨髓间充质干细胞移植到兔退变椎间盘中,并稳定表达治疗基因。
黄爱华等[28]通过慢病毒载体介导的基因修饰方式使脐血间充质干细胞表达NEP1-40,药物筛选方式获得均一表达NEP1-40的脐带血间充质干细胞,控制转染拷贝数调整NEP1-40 mRNA表达水平,为神经系统疾病治疗提出了新的思路。
王斌等[29]通过血管内皮生长因子基因转染间充质干细胞移植能显著促进肺泡发育以及微血管再生,血管内皮生长因子与新生大鼠肺发育有密切关系。
杨晓亚等[30]携带干扰素-β基因的间充质干细胞可以抑制SCID小鼠皮下黑色素瘤细胞的生长,并可以延长动物的生存期。Ryu等[31]改造脐带血来源的脐带血间充质干细胞,使其表达白细胞介素12基因,发现白细胞介素12-脐带血-间充质干细胞能够抑制小鼠颅内胶质瘤的生长。
实验使间充质干细胞表达细胞因子CX3CLl,注射到肺癌小鼠气管内,结果能有效的抑制肺癌转移,延长荷瘤小鼠的生存期,并且没有明显的不良反应[32]。
Tong等[33]用腺病毒载体在体外将小鼠超极化激活的环核苷酸门控离子通道4基因转染导入小鼠骨髓间充质干细胞,膜片钳可检出转染细胞表达类似If电流特性的起搏离子流,甚至可观察到间充质干细胞本身有自发搏动。
Yang等[34]利用慢病毒载体体外转染人超极化激活的环核苷酸门控离子通道4基因至兔骨髓间充质干细胞,同样检出有If电流表达,与心室肌细胞共培养后可明显提高心室肌自发搏动的频率。选择慢病毒载体作为基因运载系统,获得了较高的转染效率,转染的细胞稳定表达目的基因,目前未见有诱发肿瘤的报道[35-37]。
赵成利等[32] 通过构建真核表达载体pLVX-IRES- ZsGreenl加血管内皮生长因子165,运用脂质体介导293T细胞包装慢病毒,并成功感染人骨髓间充质干细胞,感染后人骨髓间充质干细胞的血管内皮生长因子mRNA显著提高,为高表达血管内皮生长因子的骨髓间充质干细胞进一步应用于血管再生和治疗临床创面愈合进行全面的探索,利用病毒实验系统将外源基因转到间充质干细胞中是当今研究的热点,慢病毒载体具有可感染处于分裂期和非分裂期的细胞,可容纳的外源片段大,能实现目的基因的稳定表达及免疫反应小等优点。
Grove等[38]运用骨髓基质细胞诱导骨髓间充质干细胞,利用腺病毒感染骨髓间充质干细胞作为基因治疗载体治疗肺气道和肺泡疾病。通过建立稳定的基因重构间充质干细胞模型研究GATA-4转染骨髓间充质干细胞的特征及鉴定,为GATA-4修饰的间充质干细胞应用于急性心肌梗死等心肌疾病的治疗提供有效的技术手段[39]。
总之,鉴于间充质干细胞的生物学特性、多向分化潜能、独特的自身特点,使其在组织工程、神经系统疾病、肝脏疾病、心血管系统、免疫系统疾病、视网膜疾病、糖尿病、肿瘤疾病等方面的基因治疗具有巨大的优势。
