中国组织工程研究 ›› 2014, Vol. 18 ›› Issue (8): 1244-1249.doi: 10.3969/j.issn.2095-4344.2014.08.016
• 生物材料基础实验 basic experiments of biomaterials • 上一篇 下一篇
KH-550/PPy/PET单丝制备及生物相容性评价
王 莹1,陈 莹2,岳秉飞1,3,唐劲天1, 2,李 莹1,张小娜1
- 1北京中医药大学中药学院生物制药系,北京市 100102;2清华大学工程物理系医学物理与工程研究所,北京市 100084;3中国食品药品检定研究院实验动物资源研究所,北京市 100050
Preparation and biocompatibility of gamma-aminopropyl triethoxysilane/polypyrrole/ polyester monofilament
Wang Ying1, Chen Ying2, Yue Bing-fei1, 3, Tang Jin-tian1, 2, Li Ying1, Zhang Xiao-na1
- 1Department of Biopharmaceutical Sciences, Beijing University of Chinese Medicine, Beijing 100102, China; 2Institute of Medical Physics and Engineering, Department of Engineering Physics, Tsinghua University, Beijing 100084, China; 3Department of Laboratory Animal Quality Testing, National Institutes for Food and Drug Control, Beijing 100050, China
摘要:
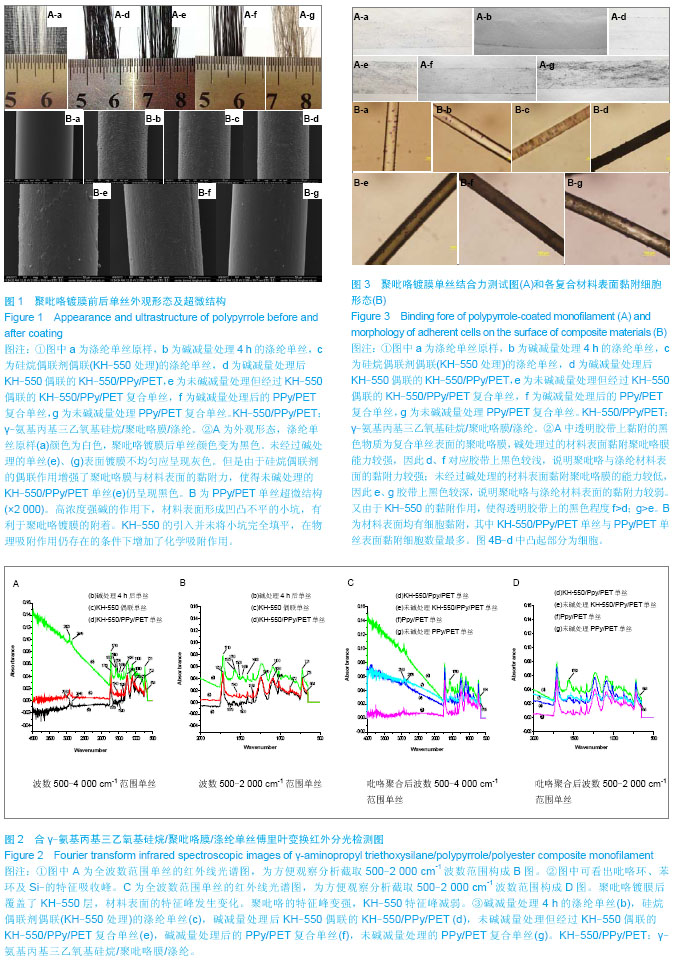
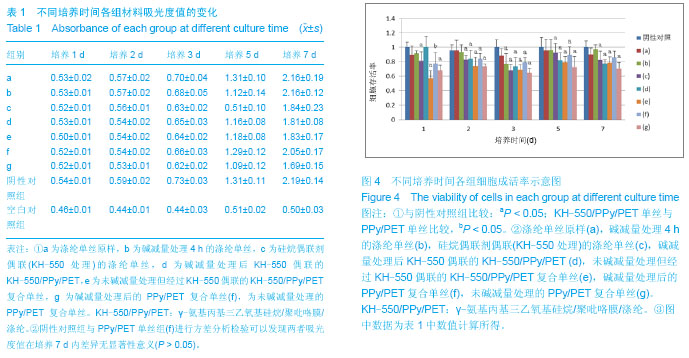
背景:目前关于移植毛发的研究大部分是以患者本身拥有足够的毛发为基础,对于治疗大面积的秃发没有明显的效果,而植入性人造头发可解决这一问题。 目的:制备硅烷偶联剂γ-氨基丙基三乙氧基硅烷/聚吡咯膜/涤纶(KH-550/PPy/PET)单丝复合材料作为植入性人造头发,并对制备效果进行评定,测定复合材料对小鼠成纤维细胞L929的细胞毒性。 方法:涤纶单丝经过去污处理、碱减量处理、硅烷偶联剂处理和聚吡咯镀膜等一系列过程制备成KH-550/PPy/PET复合材料。采用直接接触法,将此复合材料和L929细胞共孵育。采用CCK-8法于培养第1,2,3,5,7天进行细胞毒性检测。 结果与结论:制备所得的复合材料表面光滑,聚吡咯镀膜完整,无断裂,且耐磨性能良好,不易脱落。从扫描电子显微镜、傅里叶变换红外分光检测减量处理后的涤纶单丝表面聚吡咯的镀膜量明显高于未经过碱减量处理的涤纶单丝。复合材料和L929细胞共孵育,培养第1,2,3,5,7天细胞存活率依次为100%,80.37%,73.26%,81.96%,77.50%,细胞毒级为1级。结果表明,硅烷偶联剂γ-氨基丙基三乙氧基硅烷的引入有效地提高了聚吡咯膜与涤纶单丝的结合力,实验所制备的硅烷偶联剂γ-氨基丙基三乙氧基硅烷/聚吡咯膜/涤纶复合材料生物相容性较好,无明显细胞毒性。
中图分类号: