设计:病例对照试验。
时间及地点:于2010年1至6月在解放军广州军区广州总医院医学实验科完成。
对象:采集标本前3个月内未使用过免疫抑制剂的再生障碍性贫血患者20例,男9例,女11例,中位年龄26.9(15-62)岁,其中慢性再生障碍性贫血患者12例,重型再生障碍性贫血患者8例。
诊断标准:符合1987年第四届全国再生障碍性贫血学术会议修订的再生障碍性贫血的诊断标准[2]。
纳入标准:①符合再生障碍性贫血的诊断标准者。②对治疗及试验方案知情同意,且得到医院伦理委员会批准者。
排除标准:采集标本前3个月内使用过免疫抑制剂者。
同期入选18例健康体检者为正常对照组,男7例,女11例,中位年龄28.6(22-46)岁。正常对照组及再生障碍性贫血组在性别、年龄方面经统计学分析差异无显著性意义(P > 0.05)。提供者完全同意将自己的血样或标本用于本实验。
骨髓间充质干细胞对再生障碍性贫血患者T细胞免疫抑制作用实验的主要试剂及仪器:
方法:
T淋巴细胞的提取制备:取再生障碍性贫血患者和正常人的新鲜外周血10 mL,加入Ficoll淋巴细胞分离液(密度1.073 g/mL)中,提取单个核细胞。灭菌的尼龙毛柱垂直固定后放于超净台内,将细胞悬液加入尼龙毛柱内,待流出的培养液基变得不透明,此时其中含有T细胞,收集这一部分培养基。流出非黏附细胞即为T淋巴细胞,离心后重悬于上述培养基中。
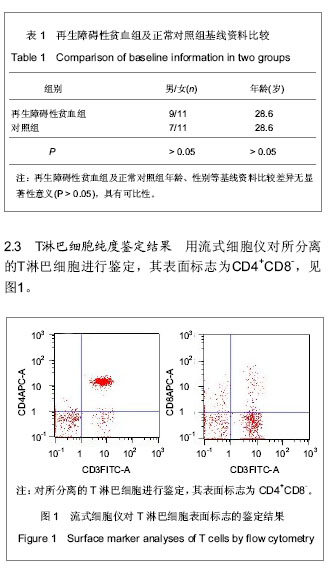
取细胞悬液1 mL,在测定管中加入(CD3-PECY5/ CD4-FITC/CD8-PE)20 μL,每份标本设一同型对照,对照管中加入鼠抗人(IgG1-PECY5/IgG1-FITC/IgG1-PE) 20 μL,混匀,室温避光反应20 min后,上机检测。
骨髓间充质干细胞的分离和培养:在本院健康骨髓捐献者经骨髓穿刺术中所得的5 mL肝素抗凝骨髓中加入Ficoll细胞分离液,密度梯度离心法提取单个核细胞,经低糖DMEM培养液洗涤,重悬后,计数,确认有核细胞数达105个/cm2后进行原代细胞培养接种。培养48 h后进行第1次全量换液,将未贴壁的细胞全部去除,每两三天换液1次。
细胞达到80%以上融合后,按1∶2的比例进行传代接种培养,记作P1,每三四天换液1次。再重复以上操作,实现细胞的有效扩增。传至P3代,留取进行下步实验。细胞培养扩增到第3代时,分别取100 μL细胞与鼠抗人CD105,CD29,CD34,CD44,HLA-DR抗体室温中反应30 min。流式细胞仪鉴定骨髓间充质干细胞表型。
骨髓间充质干细胞作为滋养层与异体T淋巴细胞共孵育:取第3代的骨髓间充质干细胞经鉴定后铺于6孔板内,待细胞生长贴壁90%融合后,为去除其过度增殖、分化能力,对骨髓间充质干细胞进行照射,选取形态及浓度均合适的孔内骨髓间充质干细胞作为滋养层细胞,分如下4组:正常对照组外周血T淋巴细胞、再生障碍性贫血组外周血T淋巴细胞、正常对照组外周血T淋巴细胞与骨髓间充质干细胞共培养后、再生障碍性贫血组外周血T淋巴细胞与骨髓间充质干细胞共培养后。
每组设3个复孔。放置于37 ℃、体积分数5%CO2培养箱培养。三四天添加培养液,第7天取上清1 mL,待测。
ELISA检测白细胞介素2、白细胞介素4、γ-干扰素、白细胞介素10蛋白水平:①样品准备:待测的样品置放于离心机1 000 r/min,离心5 min,取上清液1 mL,冰浴。②分别在相应的反应板孔中加入分别100 μL样品和标准品,稍加混匀30 s,封住板孔,置于37 ℃水浴恒温箱1 h,用洗涤液反复洗涤反应板,去除水滴,甩尽板内液体。③每孔加入100 μL×Biotin。稍加混匀30 s,置于37 ℃水浴恒温箱1 h,用洗涤液反复洗涤反应板,去除水滴,甩尽板内液体。④每孔加入100 μL×HRP,加混匀30 s,置于37 ℃水浴恒温箱1 h,置于37 ℃水浴恒温箱1 h,用洗涤液反复洗涤反应板,去除水滴,甩尽板内液体。⑤每孔加入100 μLTMB显色液,稍加混匀15 s,37 ℃水浴恒温箱暗处温浴20 min。⑥每孔加入100 μL终止液,稍加混匀30 s,在酶标仪492 nm处读吸光度(A)值。⑦绘制标准曲线,以标准浓度为横坐标,A值的半对数为纵坐标,以直线连接各标准品的坐标点,计算标准曲线,根据标准曲线计算样品的白细胞介素2、白细胞介素4、γ-干扰素、白细胞介素10水平。
主要观察指标:正常对照组和再生障碍性贫血组外周血T淋巴细胞与骨髓间充质干细胞共培养前后的白细胞介素2、白细胞介素4、γ-干扰素、白细胞介素10蛋白表达变化。
统计学分析:统计学处理者为张乐琴,数据用SPSS 13.0统计软件处理,数值用x±s表示,组间比较采用t 检验,P < 0.05为差异有显著性意义。

.jpg)