中国组织工程研究 ›› 2018, Vol. 22 ›› Issue (12): 1939-1943.doi: 10.3969/j.issn.2095-4344. 0211
• 神经组织构建 nerve tissue construction • 上一篇 下一篇
原发性干燥综合征周围神经病的神经电生理特点分析:前瞻性病例系列研究方案及预试验结果
王 丹1,李仲铭2,赵明洁1,薛若鸿1,许 虹1,钟莲梅1
- 1昆明医科大学第一附属医院神经内科,云南省昆明市 650032;2昆明医科大学基础医学院,云南省昆明市 650500
Neuroelectrophysiological characteristics of peripheral neuropathy in primary Sjögren’s syndrome: study protocol for a prospective case series and preliminary results
Wang Dan1, Li Zhong-ming2, Zhao Ming-jie1, Xue Ruo-hong1, Xu Hong1, Zhong Lian-mei1
- 1Department of Neurology, First Affiliated Hospital of Kunming Medical University, Kunming 650032, Yunnan Province, China; 2Basic Medical College, Kunming Medical University, Kunming 650500, Yunnan Province, China
摘要:
文章快速阅读:
.jpg)
.jpg)
文题释义:
干燥综合征:是一种累及全身外分泌腺的慢性炎症性自身免疫病,主要侵犯泪腺和唾液腺,表现为口眼鼻干燥及唾液分泌功能障碍。腺体外的系统如呼吸道、消化道、泌尿道肌肉及关节等均可受累,亦称口眼干燥和关节炎综合征。干燥综合征常与类风湿关节炎、系统性红斑狼疮同时存在,表现为支气管腺体的炎症、气道分泌功能降低,导致肺不张或支气管炎和肺炎;也可能发生间质性肺炎、胸膜炎等。
神经传导速度及测量方法:是用于评定周围神经传导功能的一项诊断技术,通常包括运动神经传导速度和感觉神经传导速度。其测量方法如下:①运动神经传导速度:将刺激电极置于神经干,记录电极置于肌腹,参考电极置于肌腱;地线置于刺激电极和记录电极之间。刺激神经干远端和近端,在该神经支配的肌肉上可记录到2次复合肌肉动作电位,测定其不同的潜伏期。神经传导速度(m/s)=两点间距离(cm)×10/两点间潜伏期差(ms);②感觉神经传导速度:将刺激手指或脚趾末端,顺向性地在近端神经干收集,或刺激神经于而逆向地在手指或脚趾末端收集;地线固定于刺激电极和记录电极之间。记录潜伏期和感觉神经动作电位。感觉神经传导速度为刺激电极与记录电极之间的距离除以潜伏期。
摘要
背景:干燥综合征是一种慢性进展性自身免疫性疾病,其中原发性干燥综合征患者发生周围神经系统损害比率为10%-30%。既往研究仅展示了原发性干燥综合征周围神经病患者会出现多种电生理表现,但对其神经电生理特点无统一认识,易与其他病因导致的周围神经病混淆。
目的:观察原发性干燥综合征周围神经病变患者神经电生理特征表现。
方法:此项试验涉及参与患者100例,在中国昆明医科大学第一附属医院神经内科完成,预实验纳入52例符合原发性干燥综合征周围神经病变的患者。主要观察指标为运动神经传导速度异常率,次要观察指标为末端运动潜伏期异常率、复合肌肉动作电位波幅异常率、感觉神经传导速度异常率、感觉神经动作电位波幅异常率、F波异常率及皮肤交感反射异常率。
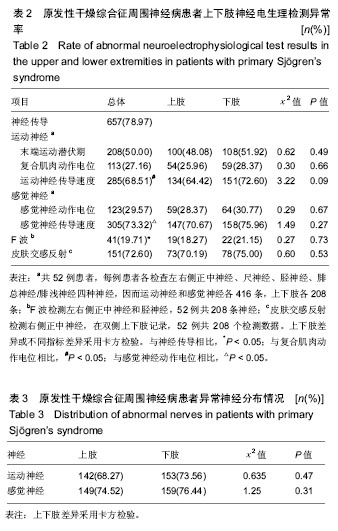
结果与结论:预试验纳入的52例患者的结果是,上、下肢不同电生理检测指标异常率接近,运动神经传导速度异常率远高于复合肌肉动作电位波幅异常率,感觉神经传导速度异常率明显比感觉神经动作电位波幅异常率高,且运动神经传导速度与感觉神经传导速度异常率接近,复合肌肉动作电位与感觉神经动作电位波幅异常率接近,F波异常率明显低于神经传导异常率,皮肤交感反射异常率与神经传导异常率接近。试验结果能够展示原发性干燥综合征周围神经病神经电生理异常情况,为疾病的诊断提供帮助。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID: 0000-0002-1666-3365(王丹)
中图分类号:
.jpg)
.jpg)