1.1 设计 制备负载药物的纳米粒,验证其体外杀伤肿瘤细胞功能及对皮下荷瘤小鼠的治疗效果。两组间数据比较使用t检验分析,两组以上数据比较采用方差分析(ANOVA)。
1.2 时间及地点 实验于2022年2月至2023年2月在苏州大学骨科研究所完成。
1.3 材料
1.3.1 细胞株 人成骨肉瘤细胞系MG-63购自中国科学院细胞库。
1.3.2 主要药品与试剂 EPZ6438(Selleck,美国);牛血清白蛋白、壳聚糖(Sigma-Aldrich,美国);丙酮、乙酸(国药,中国);胎牛血清(Gibco,美国);DMEM高糖培养基(Hyclone,美国);青霉素-链霉素溶液、TUNEL染色试剂盒(碧云天,中国);CCK-8、活死细胞染色试剂盒、细胞凋亡染色试剂盒(同仁化学,日本);OCT冰冻切片包埋剂(樱花,日本)。
1.3.3 主要仪器 实验室微量注射泵(保定兰格,中国);倒置荧光显微镜(蔡司,德国);正置荧光显微镜(蔡司,德国);透射电子显微镜(日本电子,日本);粒度仪(马尔文,英国);紫外分光光度计(岛津,日本);全波长酶标仪(BIOTEK,美国);流式细胞仪(Life,美国)。
1.3.4 实验动物 12只雌性BALB/c-Nude小鼠(裸鼠),SPF级,6周龄,体质量为20 g左右,购自江苏集萃药康生物科技股份有限公司,许可证号:SCXK(苏)2018-0008。小鼠饲养于苏州大学北校区SPF动物房。实验得到苏州大学伦理委员会审批(伦理号:SUDA20230522A04),所有实验操作均全程遵循科学技术部颁发的《关于善待实验动物的指导性意见》。
1.4 实验方法
1.4.1 负载EPZ6438牛血清白蛋白-壳聚糖纳米粒的制备 取5 mL超纯水及50 mg牛血清白蛋白放置于100 mL烧杯中,以2 mL/min的速度泵入20 mL无水乙醇,之后在磁力搅拌器上搅拌过夜。将 0.2 g的1%乙酸溶液加入到19.8 mL超纯水中,并加入20 mg壳聚糖,配置壳聚糖溶液。把壳聚糖溶液以2 mL/min的速度泵入牛血清白蛋白溶液中,之后将20 mL的无水乙醇以0.5 mL/min的速度泵入,搅拌8 h后得到胶体状溶液,12 000 r/min离心20 min,得到的白色沉淀即为牛血清白蛋白-壳聚糖纳米粒(空白纳米粒)。在-80 ℃超低温冰箱中冷冻1 d后经冷冻干燥机冻干备用。
制作负载EPZ6438的牛血清白蛋白-壳聚糖纳米粒(载药纳米粒)时,需要在加入牛血清白蛋白的同时加入EPZ6438,后续步骤与空白纳米粒相同。制作包载率测定用的载药纳米粒时,加入 10 mmol/L的EPZ6438 100 μL(573 μg)。在包载率测定后确定后续实验的相应剂量,制作载药纳米粒时,加入10 mmol/L的 EPZ6438 22.7 μL(130.23 μg)。
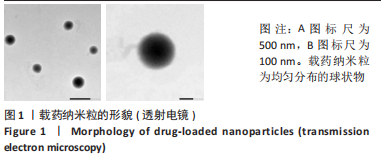
1.4.2 纳米粒的表征 将载药纳米粒置于离心管中,加入适量的无水乙醇,使用超声波清洗仪超声30 min,使纳米粒完全分散。用镊子将铜网从样品盒中取出并置于滤纸制样板,使用移液枪将10 μL均匀分散的纳米粒滴加于滤网上,再滴上1%磷钨酸进行负染色,等待纳米粒自然晾干后放入透射电镜,两次抽真空后在120 kV电压下进行微观结构拍照。
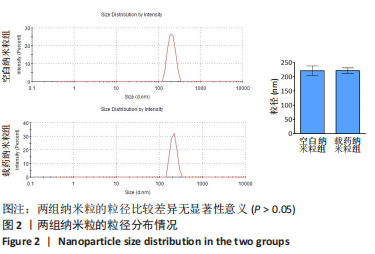
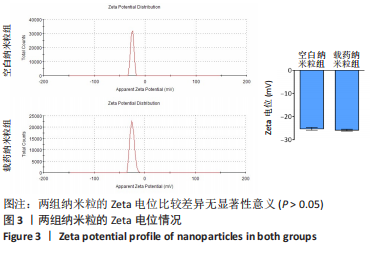
将空白纳米粒与载药纳米粒分别用超纯水重悬,置于石英管中,使用纳米粒度仪测定粒径。将两种纳米粒分别用超纯水重悬,置于马尔文Zeta电位样本池中,使用Zeta电位仪测定Zeta电位。
1.4.3 细胞的培养 取MG-63细胞,加入含体积分数10%胎牛血清、1%青霉素和链霉素的DMEM高糖培养基培养,置于37 ℃、体积分数5%CO2培养箱中,每2 d更换一次培养液。在细胞扩增至T25培养瓶的85%左右时胰蛋白酶消化,然后以1∶4的比例传代培养。
1.4.4 空白纳米粒的生物相容性检测
纳米粒浸提液的制备:将空白纳米粒浸入含体积分数10%胎牛血清、1%青霉素和链霉素的DMEM高糖培养液中,二者的比例为70 mg∶1 mL,37 ℃浸提7 d,经0.22 μm滤膜过滤后即得到空白纳米粒浸提液。
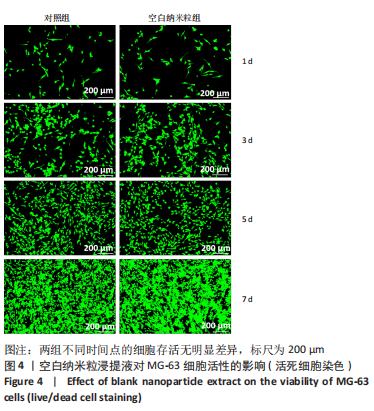
活死细胞染色:将MG-63细胞以104/孔的密度接种于24孔板中,加入200 μL 含体积分数10%胎牛血清、1%青霉素和链霉素的DMEM高糖培养液,待细胞完全贴壁后,吸除原培养液,以PBS冲洗后加入200 μL空白纳米粒浸提液,以加入培养液的孔作为对照。培养1,3,5,7 d时,轻轻吸掉原培养液,每孔加入200 μL活死荧光染液(PBS∶Calcein-AM∶PI=1 000∶2∶3),放入37 ℃、体积分数5%CO2培养箱内避光孵育30 min。孵育完毕后吸除荧光染液,以PBS清洗3次,置于倒置荧光显微镜下观察。
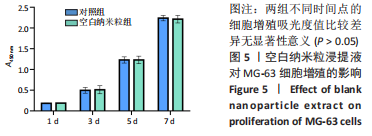
细胞增殖检测:将MG-63细胞以5×103/孔的密度接种于96孔板中,加入100 μL含体积分数10%胎牛血清、1%青霉素和链霉素的DMEM高糖培养液,置于37 ℃、体积分数5%CO2培养箱中培养24 h;待细胞完全贴壁后吸除原培养液,以PBS冲洗后分别加入100 μL的新鲜培养液(对照组)和空白纳米粒浸提液。培养1,3,5,7 d时,轻轻吸掉原培养液,以PBS冲洗,每孔加入110 μL CCK-8工作液(体积比 CCK-8原液∶PBS=1∶10),另外选择空白孔加入等量CCK-8工作液,放入37 ℃、体积分数5%CO2培养箱内避光孵育1 h。孵育完毕后,吸取100 μL反应液加入到新的96孔板中,通过全波长酶标仪检测其在450 nm波长下的吸光度值。
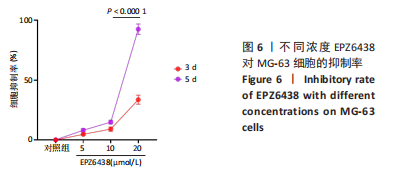
1.4.5 不同浓度EPZ6438对MG-63细胞增殖的影响 将MG-63细胞以5×103/孔的密度接种于96孔板中,加入100 μL含体积分数10%胎牛血清、1%青霉素和链霉素的DMEM高糖培养液,置于37 ℃、体积分数5%CO2培养箱中培养24 h;待细胞完全贴壁后,吸除原培养液,以PBS冲洗后分别加入100 μL含0,5,10,20 μmol/L EPZ6438的培养液。培养3,5 d时,轻轻吸掉原培养液,以PBS冲洗后每孔加入110 μL
CCK-8工作液(体积比 CCK-8原液∶PBS=1∶10),另外选择空白孔(无细胞)加入等量CCK-8工作液,放入37 ℃、体积分数5%CO2培养箱内避光孵育1 h。孵育完毕后,吸取100 μL反应液加入到新的96孔板中,通过全波长酶标仪检测其在450 nm波长下的吸光度值。细胞抑制率=(A不含药物孔-A含药物孔)/(A不含药物孔-A空白孔)×100%。
1.4.6 载药纳米粒的药物释放 取5组载等量药物的载药纳米粒(含EPZ6438 573 μg),分别置于500 μL超纯水中,每组对应一个时间点,分别于24,48,72,120,168 h取出液体,利用紫外分光光度计在280 nm波长处检测其吸收峰,利用标准曲线计算得到相应时间点的EPZ6438的总释放量。进一步计算载药纳米粒的包载率,包载率=总药物释放量/总制备投入量×100%。
1.4.7 载药纳米粒对MG-63细胞凋亡与凋亡基因表达的影响
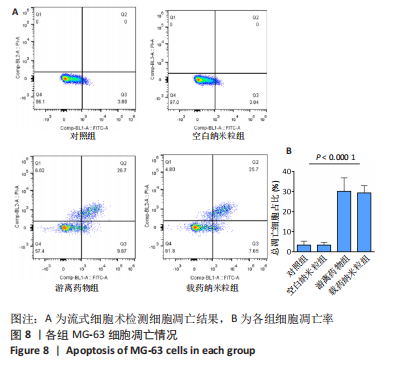
MG-63细胞凋亡检测:将MG-63细胞以105/孔的密度接种到12孔板中,分4组培养,分别加入PBS(对照组)、血清白蛋白-壳聚糖纳米粒浸提液(空白纳米粒组)、EPZ6438溶液(20 μmol/L,游离药物组)及负载EPZ6438的血清白蛋白-壳聚糖纳米粒浸提液(纳米粒中EPZ6438浓度约为19.97 μmol/L,载药纳米粒组),2 mL/孔。培养3 d后,吸取培养板中的上清液丢弃,以PBS清洗细胞3遍;使用胰蛋白酶把细胞消化下来,用含体积分数2%胎牛血清的PBS重悬细胞,800×g离心3 min,用Annexin V Binding Solution重悬细胞,细胞浓度为109 L-1;取100 μL细胞悬液,向其中加入染色工作液(Annexin V-FITC液5 μL,PI液5 μL),37 ℃避光孵育15 min后,利用流式细胞仪检测细胞凋亡,检测完毕后利用Flowjo软件分析数据。
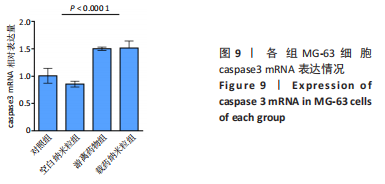
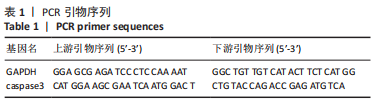
MG-63细胞凋亡基因表达检测:将MG-63细胞以2×105/孔的密度接种到6孔板中,按照如上分组培养。培养3 d后,吸出培养基,以PBS清洗3遍,每孔内加入1 mL Trizol,冰上裂解10 min并充分吹打后转移至EP管;每管内加入200 μL氯仿,并使用旋涡振荡仪振荡使其充分混合,冰上静置15 min;4 ℃下15 000 r/min离心15 min,取400 μL上清转移至新EP管内,加入400 μL异丙醇,上下翻动EP管使其充分混合,冰上静置10 min;4 ℃下15 000 r/min离心15 min,小心去上清,每管内加入1 mL体积分数75%乙醇(DEPC水稀释)用以洗涤RNA沉淀,4 ℃下15 000 r/min离心15 min,小心去上清后风干;EP管完全干燥后,每管内加入20 μL DEPC水,离心EP管后将其置于金属水浴锅中58 ℃水浴8 min,充分溶解RNA。使用NanoDrop 2000测定各组RNA浓度,进行反转录得到cDNA,将cDNA按如下配比配制PCR反应溶液(10 μL体系):SYBR green 5 μL、DEPC水1.5 μL、上下游引物各0.5 μL、cDNA 2.5 μL,将该体系置于96孔PCR板中,离心后于实时荧光定量PCR仪中扩增检测。引物序列见表1。
1.4.8 载药纳米粒的动物体内实验
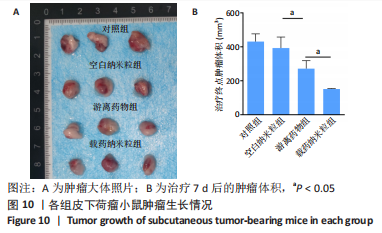
皮下荷瘤小鼠模型的构建与分组干预:在SPF动物房饲养1周后,在12只裸鼠右侧腋下注射100 μL处于对数生长期的MG-63细胞悬液,细胞浓度为1×1010 L-1,每隔1 d观察皮下成瘤情况。使用数显游标卡尺测量肿瘤长径L和短径W,计算公式:肿瘤体积V=0.5×L×W2。待肿瘤体积长至100 mm3左右时,采用随机数字表法分为对照组、空白纳米粒组、游离药物组及载药纳米粒组,每组3只,分别向肿瘤组织内注射生理盐水、空白纳米粒溶液、20 μmol/L的EPZ6438溶液、载药纳米粒(含EPZ6438约19.97 μmol/L)溶液,注射体积为100 μL。纳米粒溶液是将纳米粒重悬于生理盐水中。7 d后,对小鼠实施安乐死,取肿瘤组织,检测肿瘤体积后进行冰冻切片TUNEL染色,检测肿瘤组织的凋亡。
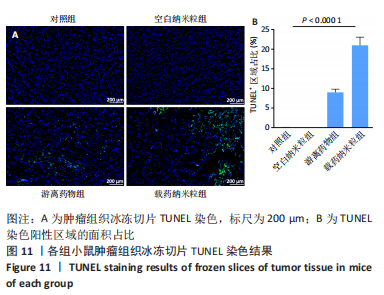
冰冻切片TUNEL染色:将肿瘤标本包埋于OCT中,冻存于-20 ℃冰箱。经冰冻切片机切片,室温平衡30 min,用冷丙酮脱水30 min,随后使用PBS清洗3遍,每次5 min。用组化笔圈定区域,多聚甲醛4 ℃固定1 h,吸去固定液,以PBS清洗3遍,每次5 min。滴加免疫荧光通透液37 ℃孵育10 min,随后使用PBS清洗3遍,每次5 min。配置TUNEL检测工作液(TdT酶∶荧光标记液=1∶9),滴加50 μL至标本表面,湿盒中37 ℃避光孵育1 h,以PBS清洗3遍,每次5 min。染DAPI室温避光15 min,以PBS清洗3遍,每次5 min,置于正置荧光显微镜下观察拍摄。
1.5 主要观察指标 载药纳米粒对MG-63细胞凋亡及凋亡基因表达的影响,以及对皮下荷瘤小鼠肿瘤组织的影响。
1.6 统计学分析 所有数据以x±s新指标,由GraphPad Prism软件进行统计学检验。其中,两组间数据对比采用t检验分析,两组以上数据之间的对比采用方差分析(ANOVA)。P < 0.05认为差异有显著性意义。该文统计学方法已经苏州大学生物统计学专家审核。