中国组织工程研究 ›› 2024, Vol. 28 ›› Issue (5): 682-689.doi: 10.12307/2024.252
• 水凝胶材料Hydrogel materials • 上一篇 下一篇
羟基磷灰石-聚乙烯醇/胶原-壳聚糖-明胶复合水凝胶修复兔骨软骨缺损
王 武1,樊晓磊2,谢 杰3,胡懿郃3,曾 敏4
- 1新疆医科大学第五附属医院骨科,新疆维吾尔自治区乌鲁木齐市 830011;2西安交通大学附属红会医院骨科,陕西省西安市 710054;3浙江大学第一附属医院骨科,浙江省杭州市 315000;4中南大学湘雅医院骨科,湖南省长沙市 410008
Hydroxyapatite-polyvinyl alcohol/collagen-chitosan-gelatin composite hydrogel for repairing rabbit osteochondral defect
Wang Wu1, Fan Xiaolei2, Xie Jie3, Hu Yihe3, Zeng Min4
- 1Department of Orthopedics, Fifth Affiliated Hospital of Xinjiang Medical University, Urumqi 830011, Xinjiang Uygur Autonomous Region, China; 2Department of Orthopedics, Honghui Hospital Affiliated to Xi’an Jiaotong University, Xi’an 710054, Shaanxi Province, China; 3Department of Orthopedics, First Affiliated Hospital of Zhejiang University, Hangzhou 315000, Zhejiang Province, China; 4Department of Orthopedics, Xiangya Hospital, Central South University, Changsha 410008, Hunan Province, China
摘要:
文题释义:
3D打印技术:又称快速成型技术或增材制造技术,是指在计算机控制下精准、快速地实现材料复杂宏观结构和精细微观结构的一体化构建,在控制材料孔隙结构及力学性能等方面具有独特优势,可精确制造个性化的组织工程支架。目前应用较多的有光固化立体印刷技术、熔融沉积成型技术、选择性激光烧结技术及3D 生物打印技术等,而聚乳酸和聚乙烯醇是目前熔融沉积成型技术中最常用的打印原材料。水凝胶:是水溶性或亲水性的高分子,通过化学或物理交联方式形成的一种具有三维网状结构的凝胶,它可以在水中迅速溶胀并能在此状态下饱含大量水分而不溶解。其根据材料不同可分为天然水凝胶和合成水凝胶两大类,聚乙烯醇水凝胶是经过冷冻融化处理后得到的一种常温下状态稳定的合成水凝胶。
背景:关节骨软骨缺损是目前骨科医生面临的难题,传统修复方法难以取得满意疗效,以羟基磷灰石-聚乙烯醇为基础的复合水凝胶材料是目前研究的一个方向。
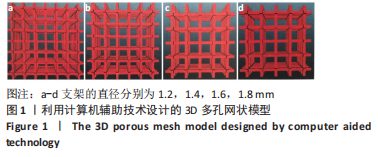
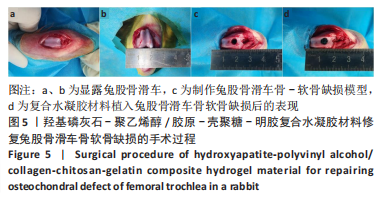
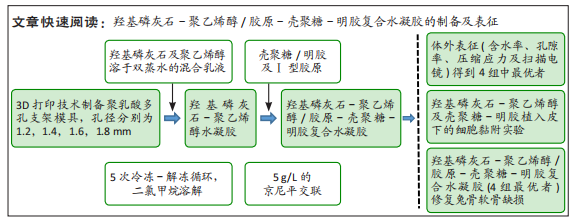
目的:制备羟基磷灰石-聚乙烯醇/胶原-壳聚糖-明胶复合水凝胶,表征其物理学特征,验证其植入体内后的组织相容性及细胞黏附增殖能力,探讨其对兔骨软骨缺损的修复效果。方法:利用3D打印技术制备圆柱状多孔聚乳酸支架(孔径分别为1.2,1.4,1.6,1.8 mm),再将聚乙烯醇及羟基磷灰石混合乳液灌入聚乳酸支架中,经过冻融及二氯甲烷溶解后制成羟基磷灰石-聚乙烯醇水凝胶。然后将胶原-壳聚糖-明胶混合液灌入羟基磷灰石-聚乙烯醇水凝胶中,利用京尼平进行交联,最后经乙醇清洗及冷冻干燥制成羟基磷灰石-聚乙烯醇/胶原-壳聚糖-明胶复合水凝胶,表征4组水凝胶的物理学特征,筛选性能最优的水凝胶进行后续实验。将羟基磷灰石-聚乙烯醇水凝胶、胶原-壳聚糖-明胶复合水凝胶分别植入SD大鼠皮下,苏木精-伊红与Masson染色观察材料表面的细胞黏附生长状况。在15只兔双侧膝关节股骨滑车制作骨软骨缺损(直径5 mm、深6 mm)模型,左侧植入复合水凝胶(实验组),右侧未植入任何材料(对照组),Micro-CT及组织学检测来评估其对骨软骨缺损的修复效果。
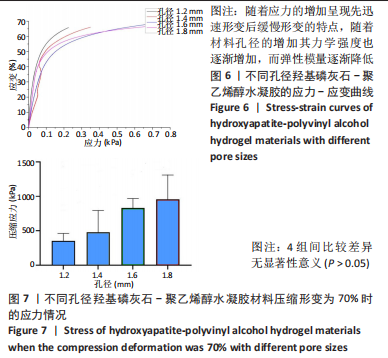
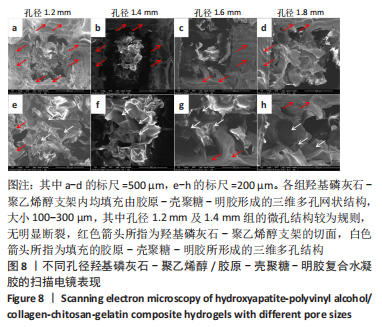
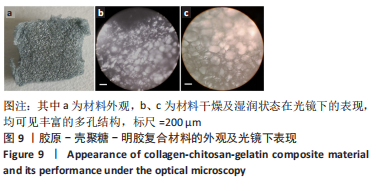
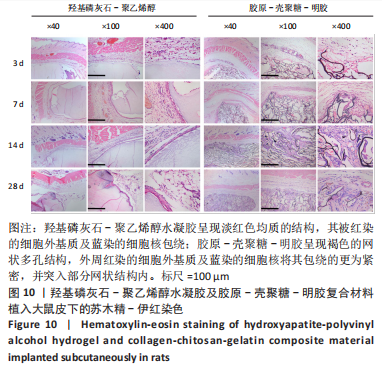
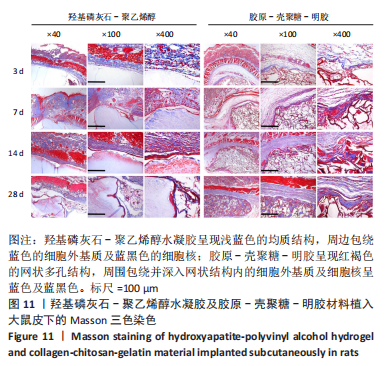
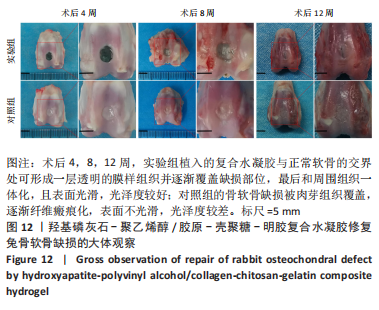
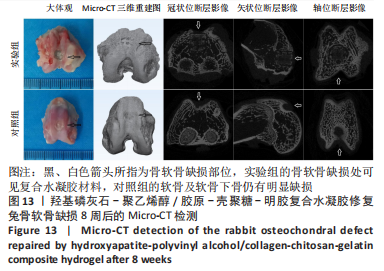
结果与结论:①综合孔隙率、含水率、力学测试及扫描电镜结果,得出孔径1.2 mm的羟基磷灰石-聚乙烯醇/胶原-壳聚糖-明胶复合水凝胶更符合天然软骨的一般特性,用于后续实验;②苏木精-伊红与Masson三色染色显示,随着材料植入大鼠皮下时间的延长,两种材料周边黏附的细胞均明显增多,其中胶原-壳聚糖-明胶植入后的细胞增殖状况更好,可见大量细胞长入其形成的网状结构,且网状结构也逐渐降解;③在兔骨软骨缺损实验中,至术后8周时,Micro-CT检查显示实验组植入的材料和周围骨-软骨整合良好,其表面及内部均有部分骨长入,对照组软骨及软骨下层仍然存在明显的缺损,未形成有效修复;苏木精-伊红与甲苯胺蓝染色显示,实验组植入复合水凝胶4-8周后即与周围骨软骨发生整合,随着时间的延长材料表面逐渐有新生软骨形成,至12周时缺损处大部分被新生软骨覆盖,软骨下层也出现良好的骨长入;对照组至术后12周虽然深层骨缺损大部分修复、浅层的软骨及软骨下骨缺损也有一定程度修复,但主要被纤维组织及部分纤维软骨替代;④结果表明,羟基磷灰石-聚乙烯醇/胶原-壳聚糖-明胶复合水凝胶材料可仿生天然软骨的结构和功能,在动物实验中能有效修复骨软骨缺损。
https://orcid.org/0000-0001-9791-9491(王武)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料;口腔生物材料;纳米材料;缓释材料;材料相容性;组织工程
中图分类号: