1.1 设计 多组分三维多孔支架的制备及体外性能评估实验,组间比较进行ANOVA单因素方差分析、Tukey’s检验及t检验等。
1.2 时间及地点 实验于2021年9月至2022 年5月在大连大学附属中山医院骨科实验室完成。
1.3 材料 蚕 茧(西北养蚕工业基地);透析袋、甲苯胺蓝染色液(索莱宝);壳聚糖(脱乙酰度≥95%)、明胶、溴化锂、N-羟基琥珀酰亚胺、碳酰二亚酸盐(上海麦克林);DMEM/F12培养基(美国 Hyclone);澳洲胎牛血清(美国 Gibco);CCK8细胞增殖试剂盒(活死细胞染色试剂盒(美国 Abbkine);碳酸氢钠(国药集团);Ⅱ型胶原酶(美国Bioshap);扫描电镜(日立Regulus8100);全自动X射线衍射仪(美国布鲁克D8 advance);通用万能试验机(深圳万测ETM系列);酶标仪(美国 Biotek);荧光显微镜(上海天省仪器 TXM-500C)。
1.4 实验方法
1.4.1 主要实验溶液的配制
壳聚糖溶液:称取3 g壳聚糖粉末溶解在1%醋酸溶液100 mL 中,磁力搅拌4 h直至完全溶解,然后过滤溶液以除去杂质。壳聚糖溶液的质量浓度为30 g/L。
明胶溶液:称取3 g生物明胶溶解在100 mL超纯水(50 ℃)中,水浴加热并持续搅拌至完全溶解。明胶溶液的质量浓度为30 g/L。
丝素蛋白溶液:①脱胶:挑选优质干净的蚕茧,将切好的茧块加入沸腾的0.5% Na2CO3溶液中,煮沸60 min,然后用蒸馏水浸泡洗涤10 min,重复两三次后烘干;②溶解:按照1∶6的比例将脱胶蚕丝在60 ℃条件下溶解于9.3 mol/L LiBr溶液中;③过滤离心:冷却至室温,使用不锈钢过滤网过滤去除较大颗粒杂质,9 000 r/min离心10 min;④透析:将离心后的丝素蛋白溶液转移至截留相对分子质量12 000±2 000的透析袋中,超纯水持续透析3 d,直至透析袋内水位不再变化;⑤浓缩:将含丝素蛋白溶液的透析袋放入浓度10%的聚乙二醇溶液中浓缩12 h,保存在4 ℃冰箱中备用。丝素蛋白溶液的质量浓度为30 g/L。
1.4.2 软骨组织支架的制备 见图1。
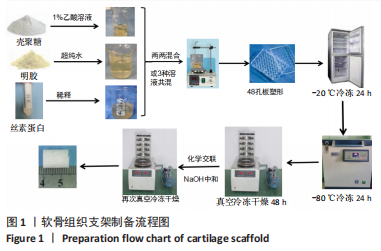
将质量浓度为30 g/L的丝素蛋白溶液、壳聚糖溶液、明胶溶液分别以1∶1体积比两两混合均匀或1∶1∶1等比例混合,并在磁力搅拌下保持30 min,制成4组均一混合溶液,分别为明胶/壳聚糖、丝素蛋白/壳聚糖、丝素蛋白/明胶和丝素蛋白/明胶/壳聚糖溶液。然后转移至48孔板内,每孔1 mL,在-20 ℃预冻12 h,放入-80 ℃冰箱中继续冷冻24 h,真空冷冻干燥48 h,经第一次塑形得到规则、圆柱状的冷冻干燥支架。
冷冻干燥后每孔中加入2 mL交联剂(交联剂各成分终浓度为:碳酰二亚酸盐50 mmol/L,N-羟基琥珀酰亚胺25 mmol/L,体积分数75%乙醇),在4 ℃条件下充分交联过夜;然后用体积分数75%乙醇和去离子水清洗数次,加入体积分数75%乙醇溶液浸泡处理24 h,使用NaOH溶液浸泡中和6 h,以去离子水洗净,再次放于-20 ℃冷冻过夜,-80 ℃冷冻48 h后行真空干燥24 h,进行第二次塑形。干燥完成后,将支架收集密封,置于4 ℃冰箱保存备用,得到明胶/壳聚糖支架、丝素蛋白/壳聚糖支架、丝素蛋白/明胶支架和丝素蛋白/明胶/壳聚糖支架。
1.4.3 软骨组织支架的物理性能表征
支架的大体外观:将不同类型的 3D 支架从48孔板中取出,并放在一起进行比较和摄影。
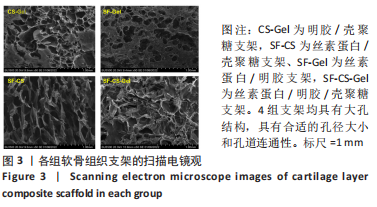
支架的扫描电镜观察:使用手术刀片将每个支架样品切成合适厚度,常规涂覆金膜后,通过扫描电镜对支架的内部结构和形貌进行了分析,采用ImageJ图像可视化软件对样品进行孔径分析,在样品中心部分至少随机选择20个孔的最大和最小直径,取平均值。
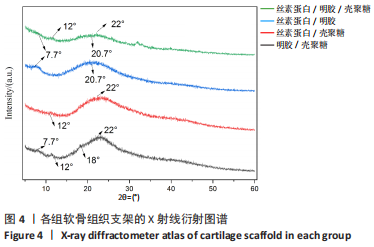
支架的X射线衍射分析:将支架研磨成粉末,使用全自动X射线衍射仪对粉末样品进行表征,在35 kV和10 mA的条件下用Cukα辐射(λ=1.542)记录样品的衍射图,扫描2θ角范围为5°-60°,扫描速率为5 (°)/min。
支架的溶胀率:采用质量法检测支架溶胀率。将冷冻干燥后的支架后称质量,记为m1;然后浸泡在PBS(pH=7.4)中24 h,取出样品,用纱布吸去支架表面多余的水分称质量,记为m2。每组实验进行3次。溶胀率=(m2-m1)/m1×100%。
支架的孔隙率:采用比重瓶法测定各组复合支架的孔隙率,用手术刀片将各支架切成统一大小的样品,以无水乙醇为液体介质,称量充满无水乙醇的比重瓶质量,记为m1;将干质量m0的支架浸入无水乙醇中,真空脱泡30 min,直至支架完全被无水乙醇所饱和,加入乙醇直至比重瓶充满相同刻度,再次称质量,记为m2;取出充盈乙醇的样品,称量剩余的液体与比重瓶质量,记为m3。支架孔隙率=(m2-m3-m0)/(m1-m3)。
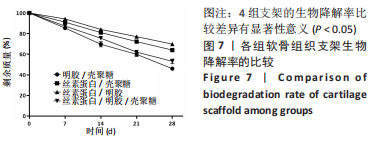
支架的生物降解率:称量真空干燥后的支架质量,记为m1,然后用含10 mg/mL溶菌酶的PBS(pH=7.4)在37 ℃下浸泡4周。在规定的时间间隔(7,14,21,28 d)取出样品,真空干燥24 h,称质量,记为mt。生物降解率=(m1-mt)/m1×100%。
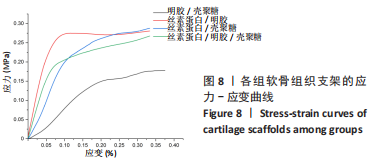
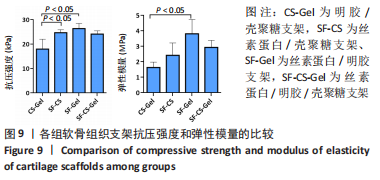
支架的机械性能:使用通用万能试验机进行支架压缩机械实验。在每次测试之前测量样品大小,支架样品为直径约10 mm、高15-18 mm的圆柱体,水平头速度设定为2 mm/min,
当压缩位移达到10 mm时停止加压。然后绘制应力-应变曲线以评估支架的机械性,应力-应变曲线初始线性阶段的斜率为弹性模量。每组3个平行样。
1.4.4 软骨细胞的提取和鉴定 收集2021年6-12月大连大学附属中山医院因骨关节炎行全膝关节置换患者的软骨组织,共10例,女7例,男3例,年龄(62.5±5.2)岁。供者对实验知情同意。实验经大连大学附属中山医院伦理委员会批准,伦理审查批件:2021073-1。
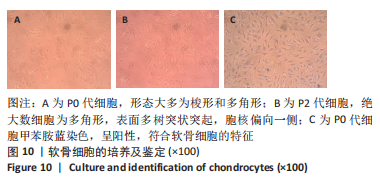
收集膝关节置换术中切除的股骨髁软骨,无菌条件下转移至在超净工作台,用无菌PBS连续漂洗两三次,分离出光滑透亮的透明软骨组织薄片,切成2 mm大小的组织块;使用5倍体积的0.2%Ⅱ型胶原酶消化过夜,消化结束后用100 μm细胞滤器过滤,然后终止消化;将获得的细胞悬液在室温下以1 500 r/min离心5 min,收集细胞沉淀,重悬后接种到T25 cm2培养瓶,置于37 ℃、体积分数5%CO2的细胞孵箱中培养。24 h后更换一次培养液以去除未贴壁的细胞,此后每3 d换液一次,建立原代培养。当贴壁细胞生长达到90%汇合时,用无菌PBS洗涤,然后使用胰蛋白酶(含EDTA)进行消化处理,并将细胞以1∶2的稀释度重新接种以进行传代培养,直到细胞达到第2代。采用甲苯胺蓝染色鉴定软骨细胞。
1.4.5 软骨组织支架与软骨细胞共培养 依据4组支架的物理性能检测结果,选择合适的软骨支架进行细胞实验。
支架接种前的处理:将支架样品切成直径10 mm、厚度为1.0-2.0 mm的薄片,在紫外光下用体积分数75%乙醇消毒过夜,然后用无菌PBS彻底冲洗3次,在细胞接种之前浸入DMEM培养基中2 h预润湿。
支架与软骨细胞共培养:取传代培养至第2代的软骨细胞悬液,接种至预先润湿的支架上,然后添加DMEM培养基,置于37 ℃、体积分数5%CO2的细胞孵箱中培养。以单独培养的软骨细胞为对照组。
支架上的细胞黏附率:将细胞浓度为108 L-1的软骨细胞接种于软骨组织支架上,每孔100 μL,然后添加DMEM培养基至300 μL。培养2,4,6 h后,从孔中取出支架,用细胞计数板(A1)计数细胞数,去除所有培养基溶液后,消化并计算黏附在孔壁上的细胞(A2)。细胞黏附率(%)=(A0-A1-A2)/A0×100%,其中A0为原始接种的细胞数。每组进行3次实验,计算平均黏附率。
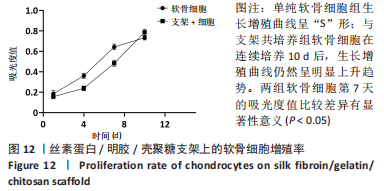
支架上的细胞增殖率:在48孔板内,将软骨细胞接种在软骨组织支架上,细胞密度为104/孔,每孔添加培养基至300 μL。每3 d更换一次培养基。培养1,4,7,10 d后,每孔加入30 μL CCK8反应溶液,37 ℃温育4 h。然后将100 μL含有CCK8反应液的培养基转移到96孔细胞培养板中,使用酶标仪在450 nm处读取吸光度值,绘制生长曲线,所有实验一式3份进行。
支架上的细胞活死染色:将细胞浓度为108 L-1的软骨细胞接种于软骨组织支架上,每孔100 μL,然后添加DMEM培养基至300 μL。培养3 d后,使用Live/Dead试剂盒进行染色,观察细胞在支架样品上的分布,该试剂盒分别用碘化丙啶和Calcein AM对死细胞和活细胞进行染色,并在细胞培养箱中孵育30 min后,使用荧光显微镜观察。
1.5 主要观察指标 各组软骨组织支架的物理性能,以及软骨组织支架的生物活性。
1.6 统计学分析 使用SPSS 20.0软件(SPSS,Inc,Chicago,USA)进行统计分析。多组样本间的比较进行ANOVA单因素方差分析,然后进行Tukey’s检验,以确定组间测量数据的差异,独立样本数据的比较使用t检验,重复测量数据使用球形检验,认为P < 0.05为差异有显著性意义。文章统计学方法经过大连大学附属中山医院生物统计学专家核实。