中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (6): 948-954.doi: 10.12307/2023.239
• 干细胞综述 stem cell review • 上一篇 下一篇
干细胞在皮肤抗衰老中的应用
熊 娟,关亚琳,杨雨童,王 矾,刘忠山
- 贵州医科大学附属医院整形烧伤科,贵州省贵阳市 550000
-
收稿日期:2021-11-15接受日期:2022-04-13出版日期:2023-02-28发布日期:2022-08-12 -
通讯作者:刘忠山,博士,副主任医师,贵州医科大学附属医院整形烧伤科,贵州省贵阳市 550000 -
作者简介:熊娟,女,1996年生,陕西省渭南市人,汉族,贵州医科大学在读硕士,主要从事临床工作及基础实验研究。 -
基金资助:国家自然科学基金(20210020)
Application of stem cells to skin anti-aging
Xiong Juan, Guan Yalin, Yang Yutong, Wang Fan, Liu Zhongshan
- Department of Plastic Surgery and Burn, Affiliated Hospital of Guizhou Medical University, Guiyang 550000, Guizhou Province, China
-
Received:2021-11-15Accepted:2022-04-13Online:2023-02-28Published:2022-08-12 -
Contact:Liu Zhongshan, MD, Associate chief physician, Department of Plastic Surgery and Burn, Affiliated Hospital of Guizhou Medical University, Guiyang 550000, Guizhou Province, China -
About author:Xiong Juan, Master candidate, Department of Plastic Surgery and Burn, Affiliated Hospital of Guizhou Medical University, Guiyang 550000, Guizhou Province, China -
Supported by:the National Natural Science Foundation of China, No.20210020
摘要:
文题释义:
干细胞:是一类具有自我更新和多向分化潜能的细胞,具有再生、替代、修复和分化能力,在个体发育和疾病发生中扮演着重要角色,是再生治疗中的关键细胞,根据个体发育过程中出现的先后次序不一样,可分为胚胎干细胞和成体干细胞。
皮肤衰老:是一种自然过程,受内源性及外源性因素影响,表现为皱纹、粗糙、色素沉着及弹性降低等。
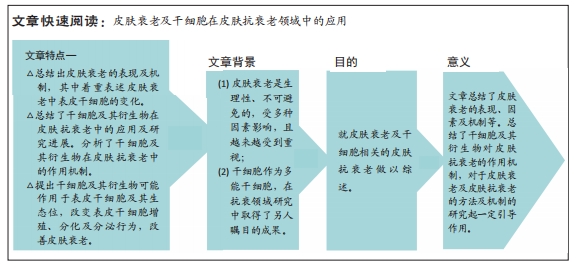
背景:由于皮肤衰老的必然性,以及人们生活水平提高所致的皮肤衰老受到了更多的重视,因此带来抗衰老领域强烈的市场需求及研究需求。
目的:综述皮肤衰老及干细胞用于皮肤抗衰老的研究进展,为干细胞相关皮肤抗衰老的应用及研究提供理论依据。
方法:检索PubMed及中国知网数据库2016年11月至2021年11月关于皮肤衰老及干细胞相关皮肤抗衰的文献,排除陈旧以及重复的观点,将检索到的文献进行整理,共纳入91篇文献来进行分析。
结果与结论:①皮肤衰老主要表现在皮肤出现皱纹、弹性降低、表皮变薄;皮肤衰老的因素包括内源性因素及外源性因素,以及皮肤衰老的机制包括表皮干细胞增殖及分化平衡的改变、氧化应激等,文章重点描述了衰老皮肤中表皮干细胞的变化,包括细胞内DNA损伤、活性氧增高;细胞增殖与分化减少,不对称及对称分裂平衡改变;生态微环境的改变;干细胞-免疫细胞信号传导异常;②文章介绍了间充质干细胞及干细胞衍生物在皮肤抗衰老中的研究应用,如在动物实验中皮下注射干细胞或其衍生物,通过观察真皮厚度、氧化应激及弹性纤维等,表明干细胞及其衍生物在皮肤抗衰老中的作用;③上述研究证明了干细胞相关皮肤抗衰老的有效性,具体抗衰老机制包括促进细胞增殖、降低活性氧水平及调节基因表达等。
https://orcid.org/0000-0001-5257-3212 (熊娟);https://orcid.org/0000-0002-6377-4818 (刘忠山)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号:
引用本文
熊 娟, 关亚琳, 杨雨童, 王 矾, 刘忠山. 干细胞在皮肤抗衰老中的应用[J]. 中国组织工程研究, 2023, 27(6): 948-954.
Xiong Juan, Guan Yalin, Yang Yutong, Wang Fan, Liu Zhongshan. Application of stem cells to skin anti-aging[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 948-954.
2.1.1 皮肤衰老的因素及表现 皮肤衰老源于2种不同的原因:内在因素和外在因素。不同因素所导致的皮肤衰老表现也有所差异,见表1。

内在因素是随着时间的推移进行的,并涉及有机体的所有组织。内在因素所致的衰老主要表现为非暴露的皮肤特征,如皱纹、皮肤下垂和干燥[3-4],这些特征可能是由激素变化引起 的[5]。活性氧是另一个内在老化的原因[6],类似于外在老化。在有氧代谢过程中,活性氧作为副产物不断产生于线粒体的电子传递链中,超氧阴离子的大量产生可能损害细胞功能,导致细胞衰老[7]。
皮肤衰老的外在因素是由各种环境因素引起的,如紫外线暴露和吸烟等。研究表明皮肤衰老80%的因素是由于紫外线暴露造成的,称为光老化[8]。在光老化皮肤中,整个真皮弹性纤维网络逐渐被破坏,纤维粗大、缠结、迂曲、降解和功能紊乱,导致弹性材料密度增加,致使整个真皮出现一簇无定形、营养不良的弹性材料,这是光老化的典型组织学特征[9]。紫外线辐射能够通过表皮到达真皮,导致深层皱纹、皮肤弹性丧失和皮肤色素沉着。光损伤皮肤中还观察到组织学变化、表皮增厚、黑素细胞分布不均匀[10]。中波紫外线穿透上皮层,对皮肤真皮造成DNA损伤[11]。长波紫外线会产生显著的氧化应激,从而介导对DNA和非DNA靶标的氧化损伤[12]。如紫外线照射会导致弹性蛋白基因选择性剪接[13],这将直接导致弹性蛋白的含量减少。除此之外,紫外线照射会促进基质金属蛋白酶的激活[14],这将导致细胞外基质蛋白分解增加。
2.1.2 皮肤衰老中表皮干细胞的变化 目前已有研究结果提供了干细胞功能的年龄依赖性进行性恶化的大量证据,包括活性氧等毒性代谢产物的累积、线粒体功能异常、DNA损伤、细胞外信号传导异常、表观遗传重塑等[15]。表2系统总结了皮肤衰老中表皮干细胞的相关变化。

表皮干细胞的内部变化:衰老会在表皮干细胞内诱发大量细胞结构紊乱,如活性氧升高。活性氧,包括自由基和非自由基含氧分子,被认为在固有衰老和光衰老的皮肤细胞外基质改变中起关键作用。活性氧可由不同来源产生,包括线粒体电子传递链、过氧化物酶体和内质网定位蛋白、Fenton反应等[16]。在干细胞中,活性氧调节干细胞对代谢和环境信号的反应性[17]。过量的活性氧影响细胞代谢调节进而导致细胞损伤或功能障碍。由于活性氧参与了多种类型的衰老相关变化,因此探究活性氧升高和皮肤抗氧化防御相关的潜在机制有助于理解干细胞内在的衰老过程。
持续将皮肤暴露于紫外线辐射会增加DNA损伤和突变,并导致过早衰老[18]。当DNA吸收紫外线的光子时,会发生核苷酸的结构重排,从而导致DNA链的变化[19]。紫外线辐射会导致过量的活性氧产生,从而引起端粒突变并进一步导致细胞衰老或死亡[20]。端粒是重复的核苷酸序列,它覆盖并保护染色体末端免受降解和异常重组。随着每次细胞分裂,端粒缩短,最终导致细胞衰老。端粒酶是一种在末端增加端粒重复序列以防止端粒变短的酶。端粒酶缺陷小鼠表现为端粒缩短加速,导致组织再生缺陷。此外,端粒短的表皮干细胞的增殖能力受到抑制,而在端粒极短的小鼠中重新引入端粒酶可以纠正表皮干细胞缺陷[21]。
糖基化是蛋白质或脂质被聚糖修饰的反应。蛋白质糖基化涉及逐步添加和去除聚糖,主要由糖基转移酶和糖苷酶介导。聚糖的存在决定了糖蛋白的结构、稳定性和定位,影响多种生物学过程,调节控制干细胞自我更新和分化的信号分子[22],考虑其在干细胞衰老过程中会发挥重要作用。已有研究表明,表皮干细胞在衰老过程中的聚糖变化可能是由糖基转移酶和糖苷酶表达随年龄的变化介导的。在衰老过程中,表皮干细胞的糖基化模式发生了整体性改变,甘露糖修饰减少,唾液酸修饰增加。老年表皮干细胞唾液酸转移酶和甘露糖苷酶基因上调。由于糖基化在细胞-细胞和细胞-基质相互作用中起着关键作用,表皮干细胞表面多糖的变化可能会影响它们与邻近干细胞、其他细胞类型(如成纤维细胞、免疫细胞和血管)、基底膜和信号分子相互作用的能力[23]。
表皮干细胞增殖与分化的变化:衰老与大多数组织的完整性和功能下降有关。随着年龄的增长,表皮会表现为发育不全和增殖不足。表皮的分层和分化减少,表皮的平均厚度减少。表皮维持需要在干细胞的自我更新和分化之间保持平衡,以确保在再生所有基底上层的同时保存干细胞群体。衰老导致的低增殖与多种鼠组织中干细胞自我更新减少相关[24]。哺乳动物表皮干细胞能够进行对称和不对称的干细胞自我更新分裂。不对称自我更新分支导致一个干细胞和一个承诺祖细胞,对称自我更新分支导致2个干细胞。对称干细胞自我更新分裂维持了干细胞库,但不对称干细胞分裂维持了表皮分层。干细胞自我更新随年龄增长而减少,在人类受试者(新生儿至78岁)中,表皮基底层分裂呈年龄依赖性减少。而且有证据表明在人类组织中,尽管干细胞自我更新的分裂随着年龄的增长而减少,但不对称/对称分裂的平衡会倾向于对称自我更新的方向转变。以此可以进一步得出结论,干细胞的分化随着年龄的增长进一步减少[24]。
相关RNA测序显示上皮分化基因随着年龄的增长而减少,表皮分化标志物K10随着年龄的增长而降低[25]。在小鼠表皮中缺失LGN (Leu‐Gly‐Asn重复序列)后,不对称干细胞分裂减少,导致基底上细胞减少和表皮变薄[26]。在磷酸肌醇依赖性激酶1条件性敲除小鼠中,不对称干细胞自我更新分裂从50%(野生型)降至13%,表皮厚度降低[27]。老年干细胞中p53表达降低,有研究发现激活老年角质形成细胞中的p53会增加不对称分裂的数量,减少对称干细胞自我更新分裂的数量,使不对称和对称干细胞自我更新分裂的比例恢复至与正常成人相似的水平[24]。以上研究成果提示,干细胞分化随着年龄的增长而减少,导致皮肤上皮变薄,造成这种现象的很大因素是干细胞基因的变化。这引起研究者思考,能否针对这些基因变化,目的性地对干细胞进行基因水平的改造,来进一步影响干细胞的增殖和分化等生物学行为,为临床干预皮肤抗衰老的举措提供研究方向。
表皮干细胞与其生态位:在大多数衰老组织中,再生能力的下降既源于干细胞内在变化,也源于干细胞生态位微环境的外在变化。干细胞生态位由间充质、内皮、神经元、免疫细胞及因子、细胞外基质成分以及干细胞自身提供的有丝分裂原、代谢物、机械线索和细胞因子组成[28]。干细胞自己的后代也能检测到环境变化,并将这些信息传递回干细胞[29]。这些特征赋予干细胞感知和响应环境中各种变化的能力,这些指导性信号指导干细胞静止或增殖,并根据组织的需要进行分化,其最终目标是让表皮干细胞在基底层微调自身增殖,同时产生恒定流量的终末分化保护细胞,维持体内平衡,同时每隔几周创造一个全新的皮肤屏障。干细胞不完全是其生态位的简单被动反应者;相反,它们在创造和沟通其周围生态位中发挥重要作用。
无论是来自生态位,还是来自损伤后显著的环境变化的再生信号[30],都会改变干细胞行为并破坏组织的稳态平衡。生态位通信已进一步被证明是维持干细胞功能、修复伤口和确保有效愈合的核心。在组织损伤和其生态位被破坏后,干细胞会分泌细胞因子和生长因子,释放信号,吸引不同类型细胞,其中,中性粒细胞和嗜酸性粒细胞是产生细胞因子生态位的早期反应性炎症细胞[31]。干细胞迅速恢复生态位稳态的能力对于皮肤损伤的恢复起重要作用[32]。基于当前研究,干细胞不仅能够修复轻微损伤和保持生态位平衡,还能感知和响应再生刺激以及各种各样的组织损伤和其他应力。研究表明,生态位细胞是炎性信息的重要整合者,特别是免疫细胞已经成为高度应激反应的生态位细胞。巨噬细胞和调节性T细胞(Tregs)2种驻留在组织中的免疫细胞,在正常生理条件下已成为干细胞调节因子。干细胞自身的子代可以成为重要的生态位组成部分:而早期的祖代可以将短暂的激活信号发送回其干细胞亲代,以促进其自我更新和促进组织生长[33-36],分化的子代可以回到它们的生态位以停止进一步增殖和组织再生并恢复体内平衡[37]。研究表明,在皮肤中,尽管成纤维细胞与表皮干细胞生态位的位置关系随着年龄的增长而保持不变,但成纤维细胞本身会逐渐显示出脂肪生成日益增加的特征[38]。随着年龄的增长,表皮干细胞本身以及其生态位的其他成分会产生变化,导致表皮干细胞生态位发生变化,进而影响干细胞功能。
表皮干细胞衰老与免疫:上皮组织会遇到各种各样的炎症反应,对于皮肤,这些因素包括化学品和其他有害物质、过敏原、病原体和紫外线照射。与年龄相关的组织功能下降通常表现为促炎递质水平升高、低度全身性炎症和伤口愈合受损。表皮含有一系列功能复杂的常驻免疫细胞。最近的研究表明,其中一些与年龄相关的缺陷是由免疫细胞和组织干细胞之间的信号传导异常以及组织中促炎递质的慢性积累造成的[39-40]。皮肤是常驻免疫细胞和老化干细胞之间对话的理想场所。免疫细胞作为干细胞生态位的组成部分,许多细胞是可移动的,能够迁移到局部淋巴结并刺激非常驻免疫细胞,然后这些细胞可以通过循环到达组织损伤部位,并有助于炎性反应,从而清除组织中的病原体和损伤细胞以促进其自我更新和促进组织生长,恢复体内平衡依赖性组织修复[41]。由于干细胞负责应答的修复阶段,存在复杂的免疫-干细胞通信,以确保入侵病原体得到控制。干细胞-免疫细胞的相互作用除了巨噬细胞和调节性T细胞(Tregs),还包括许多其他驻留在组织中的免疫细胞[42-43]。树突状表皮T细胞分泌生长因子和趋化因子,包括胰岛素样生长因子1和成纤维细胞生长因子7/10,均可促进表皮过度增殖[30]。在老化过程中,表皮干细胞向附近免疫细胞传输信号的能力会减弱,这可能是老年人常见慢性伤口的原因之一[44]。常驻免疫细胞群数量、比例及功能状态等的年龄相关性变化可能会影响这些活动。其中一种变化是常驻Tregs下降[45],这可以解释衰老过程中常见的炎症反应加剧的现象。另一值得注意的是,干细胞在其染色质中记录了它们所遇的炎症反应,这一特征随后会影响干细胞在下一次炎症反应中的行为。研究显示,暴露于炎症诱导药物咪喹莫特后,表皮干细胞的染色质发生显著变化,其中一些变化甚至可以在病理学恢复正常后6个月检测到[46]。值得注意的是,表皮干细胞需要在白细胞介素1β的协助下记住这些炎性记忆[47]。因此,逆转干细胞衰老过程和使组织再生的关键将不仅是刺激组织干细胞自我更新,而且要致力于随年龄积累的炎性递质的治疗。
2.2 干细胞相关的皮肤抗衰老 干细胞是一种最新的生物资源,分泌多种促进组织再生的生长因子,如碱性成纤维细胞生长因子、血管内皮生长因子、转化生长因子β等,这是干细胞区别于其他细胞类型的特征[12]。目前研究用于抗衰老美容医学领域的干细胞主要有间充质干细胞、诱导性多能干细胞以及其他一些新型干细胞等[48],其中应用较多的是间充质干细胞,在各类间充质干细胞中应用较多的属脂肪间充质干细胞。干细胞治疗作用的模式主要是干细胞分泌的细胞因子所介导的旁分泌效应[49]。因此随着干细胞研究的深入,干细胞的相关衍生物也逐渐得以验证其功能并加以应用。在众多干细胞衍生物中提出较多的是干细胞外泌体、干细胞条件培养基以及细胞工程纳米囊泡等。表3中总结了干细胞及其衍生物在皮肤抗衰老中的研究应用情况。

2.2.1 间充质干细胞在皮肤抗衰老中的应用 间充质干细胞来源于多种组织,如骨髓、脐带、脂肪组织、胎盘和月经血等。间充质干细胞因其对真皮细胞具有相对广泛的旁分泌作用而被应用于皮肤损伤及延缓衰老的治疗中;间充质干细胞刺激血管生成,保护其他细胞免受过氧化物介导的损伤,调节炎症、疼痛和免疫耐受[50-52]。在各种间充质干细胞中,脂肪间充质干细胞由于其丰度、易分离性和在临床采集期间的耐受性而被优选。脂肪来源的干细胞在皮肤治疗中的应用也已经在诸多实验研究中阐述,获得了令人满意的效果。
在一项对暴露于紫外线的小鼠中进行皮下注射脂肪间充质干细胞对皱纹影响的临床前研究表明,与对照组相比,脂肪间充质干细胞治疗可减少皱纹,而且注射脂肪间充质干细胞的真皮厚度显著增加,且还观察到胶原束增加[53]。也有研究表明,脂肪间充质干细胞可能具有激活皮肤成纤维细胞的能力,从而减少紫外线诱导的细胞凋亡,并刺激胶原合成[54]。在一项脂肪间充质干细胞皮肤治疗方案中,对弹性系统的所有分析均针对日光性弹性减退或完全逆转,在此过程中解决了2个问题:①乳头状真皮中丧失的氧合肌和弹性蛋白纤维网络的再生,新的弹性蛋白生产和聚合的完全再激活;②真皮深层中具有正常原纤维结构(弹性纤维)的光化弹性蛋白病理沉积物的置换[55]。即深层真皮细胞外基质的2种生化再生修饰的有序控制:异常弹性蛋白的过度弹性沉积物的降解和吸收,以及它们被深层真皮中新的正常聚合弹性纤维网络取代。
有研究通过针对衰老相关变化对间充质干细胞进行改造后评估其抗衰老效果,FAN的等[56]一项研究评估了脂肪间充质干细胞中Klotho对暴露于紫外线的皮肤成纤维细胞的影响,发现与Klotho过表达的脂肪间充质干细胞共培养的皮肤成纤维细胞显著减少了胶原降解酶和金属蛋白酶的产生,同时增加了Ⅰ型和Ⅲ型胶原的产生。有研究表明过表达NAMPT的脐带间充质干细胞外泌体可促进人皮肤成纤维细胞增殖和延缓衰老,且延长秀丽隐杆线虫寿命和增强其抗氧化能力。有研究证明NAMPT转基因人脐带间充质干细胞可产生载有高水平和功能性的NAMPT mRNA和蛋白质的外泌体[95]。作者在前文中论述过衰老相关的变化,包括干细胞表观遗传的变化,以及相关基因表达的变化。为此,作者提出假设,能否对治疗性间充质干细胞进行改造,逆转表皮干细胞的衰老局面。临床中脂肪间充质干细胞可以通过吸脂等操作获取,获取过程相对简单,且自体脂肪无排异反应,在临床上已成为一种辅助抗衰老手段,结合其他抗衰老措施达到了更好的皮肤抗衰老效果,但是对于其抗衰老的机制研究者们仍知之甚少,仍需更深入的研究工作。
2.2.2 干细胞衍生物在皮肤抗衰老中的应用 据报道外泌体在干细胞旁分泌效应中起主要作用[57-58],在发现外泌体作为细胞间通讯的信使后,引起人们对外泌体应用的极大关注。
外泌体是几乎所有真核细胞释放的纳米级细胞外囊泡。来源于干细胞的外泌体在多个方面都具有巨大的治疗潜力。外泌体能够保护其内容物免受降解,并且在血清和血液中高度稳定,因此能够有效地将内容物递送至靶细胞。有证据表明,细胞外囊泡调节正常的生理过程中,包括血管生成、抗原呈递、凋亡、凝血、细胞稳态、炎症、细胞分化和细胞间信号传导[59],除此之外还在干细胞维护、组织修复和免疫调节中发挥着重要作用[60-62]。外泌体的释放可能抑制或激活细胞凋亡,这取决于它们的内容物和受体细胞类型[63-64]。在正常和病理条件下,细胞外囊泡或外泌体介导旁分泌衰老,将衰老信号从衰老或患病细胞传递到正常细胞[65-71]。间充质干细胞-细胞外囊泡通过其独特的miRNA、lnRNA和酶含量赋予抗衰老作用,在衰老细胞中诱导增殖和减少衰老相关分泌表型,在减少组织中的衰老细胞方面具有巨大的潜力[72]。因此,来自干细胞的细胞外囊泡或外泌体可以减轻或逆转细胞衰老。
使用从脂肪间充质干细胞获得的细胞外囊泡进行的其他研究显示,用这些细胞外囊泡处理的人皮肤成纤维细胞培养物增加了细胞增殖和迁移,上调了与皮肤再生相关的分化簇34(CD-34)、Ⅰ型胶原、弹性蛋白和角质细胞生长因子基因的表达。值得注意的是,此类细胞外囊泡的基因组研究表明hsa-miR-4484,hsa-miR619-5p和hsa-miR-6879-5p为表达较多的miRNA,它们可以调节不同基因的表达,如核磷蛋白1、程序性细胞死亡4、趋化因子(C-C基序)配体5(CCL-5)和核孔蛋白62,其与增殖和衰老有关,因此参与组织再生[73]。另一项研究也报道年轻小鼠的外泌体可以将miR-126b-5p转移到老年小鼠组织中,逆转老年小鼠p16、mTOR、胰岛素样生长因子1R等衰老相关分子以及Men1,Mre11a,Tep1,Terf2,Tert和Tnks等端粒酶相关基因的表达[73-75]。此外,这些外泌体还促进了HaCaT的增殖和迁移,上调了增殖标记基因,如细胞周期蛋白A1,A2,D1和D2,以及纤维连接蛋白。皮下注射脂肪间充质干细胞外泌体通过以剂量依赖性方式产生神经酰胺和具有长酰基链的二氢神经酰胺来诱导皮肤屏障的修复。来自青年小鼠血浆的细胞外囊泡通过胞外烟酰胺磷酸核糖转移酶延缓衰老,从而延长老年小鼠的寿命。也有研究证明由诱导多能干细胞和年轻间充质干细胞分泌的细胞外囊泡通过降低细胞内活性氧水平,减少了与间充质干细胞培养物老化相关的细胞衰老[76]。来自最近报告的额外证据证实诱导性多能干细胞衍生的间充质干细胞分泌的外泌体加速皮肤细胞增殖[77-78]。
脂肪间充质干细胞条件培养基也含有脂肪间充质干细胞分泌的关键细胞因子和生长因子,可促进各种组织器官的再生和修复,起到抗氧化、抗皱和美白的作用[79]。制备良好的间充质干细胞条件培养基在一定程度上起到了预防皮肤成纤维细胞内源性和外源性衰老损伤的积极作用。脂肪间充质干细胞条件培养基中存在的旁分泌因子(表皮生长因子、碱性成纤维细胞生长因子、转化生长因子β、血管内皮生长因子)促进皮肤成纤维细胞增殖、迁移,增加细胞外基质、胶原蛋白的产生,从而改善皮肤弹性丧失等面部衰老体征[80]。间充质干细胞条件培养基已被证明可在体外保护皮肤成纤维细胞免受氧化应激[81]。体外实验中报道了脂肪间充质干细胞条件培养基中含有的血小板衍生生长因子AA(-AA)也可以激活磷脂酰肌醇-4,5-二磷酸3-激酶(PI3K)/蛋白激酶B(AKT)信号通路,介导光老化诱导的皮肤成纤维细胞增殖、细胞外基质沉积和重塑[82]。研究表明,来源于人诱导性多能干细胞的条件培养基和外泌体改善了由紫外线光老化和自然衰老诱导的人皮肤成纤维细胞的基因型和表型变化[83-84]。来源于诱导性多能干细胞的外泌体含有介导细胞内递送的功能因子,并通过调节衰老相关基因的表达和提高结构蛋白(即Ⅰ型胶原)的含量来重新平衡衰老皮肤中的基质,从而促进创伤损伤和衰老皮肤中真皮基质的重建[85]。BRANSCOME等[86]比较了诱导性多能干细胞-细胞外囊泡和间充质干细胞-细胞外囊泡,蛋白质分析结果显示,诱导性多能干细胞-细胞外囊泡含有参与受体酪氨酸激酶信号传导的蛋白质;间充质干细胞-细胞外囊泡含有参与Ras相关蛋白1途径和Janus激酶信号转导和转录激活因子(JAK-STAT)途径等途径的蛋白;诱导性多能干细胞-细胞外囊泡与成纤维细胞生长因子2、血管内皮生长因子和白细胞介素4的相关性高于间充质干细胞-细胞外囊泡。此外,将来源于诱导性多能干细胞的高纯度细胞外囊泡应用于活性氧升高的衰老间充质干细胞时,细胞活性氧水平降低,衰老间充质干细胞的衰老表型减轻。值得注意的是,人诱导性多能干细胞产生的细胞外囊泡是间充质干细胞的16倍。
细胞工程纳米囊泡是通过孔径逐渐减小的膜过滤器连续挤出细胞,从而机械破坏细胞的质膜,引入了生成细胞外囊泡模拟纳米囊泡的新方法[87-89]。有研究表明来源于诱导性多能干细胞的细胞工程纳米囊泡与来源于诱导性多能干细胞的外泌体具有相似的促进皮肤成纤维细胞增殖和迁移的作用[90]。研究表明与常规条件培养基衍生的细胞外囊泡相比,细胞工程纳米囊泡在大规模生产方面具有若干优势。当比较获得的颗粒总数相对于相同细胞数时,细胞工程纳米囊泡的平均产率比条件培养基衍生的细胞外囊泡高70倍以上[91]。相对于其他衍生物而言,细胞工程纳米囊泡具有更高的可塑性。
干细胞衍生物在面部抗衰老中的应用在许多方面是有优势的,如:①它们具有促进增殖、传达信号和血管生成等作用;②它们的内容物得益于脂质双层可以长期且稳定的存在于组织中;③它们可具有细胞毒性、天然细胞靶向性和有效的递送等特殊性质。因此在干细胞相关的皮肤抗衰老应用领域中应用前景可观。

| [1] RUSSELL GE, MURPHY GF. The pathobiology of skin aging: new insights into an old dilemma. Am J Pathol. 2020;190(7):1356-1369. [2] KIM DH, BANG E, JUNG HJ, et al. Anti-aging effects of calorie restriction (CR) and CR mimetics based on the senoinflammation concept. Nutrients. 2020;12(2):422. [3] HASHIZUME H. Skin aging and dry skin. J Dermatol. 2004;31(8):603-609. [4] JENKINS G. Molecular mechanisms of skin ageing. Mech Ageing Dev. 2002; 123(7):801-810. [5] MAKRANTONAKI E, ZOUBOULIS CC. Androgens and ageing of the skin. Curr Opin Endocrinol Diabetes Obes. 2009;16(3):240-245. [6] FARAGE MA, MILLER KW, ELSNER P, et al. Intrinsic and extrinsic factors in skin ageing: a review. Int J Cosmet Sci. 2008;30(2):87-95. [7] LOPEZ-OTIN C, BLASCO MA, PARTRIDGE L, et al. The hallmarks of aging. Cell. 2013;153(6):1194-1217. [8] TRAUTINGER F. Mechanisms of photodamage of the skin and its functional consequences for skin ageing. Clin Exp Dermatol. 2001;26(7):573-577. [9] UITTO J. Biochemistry of the elastic fibers in normal connective tissues and its alterations in diseases. J Invest Dermatol. 1979;72(1):1-10. [10] LANDAU M. Exogenous factors in skin aging. Curr Probl Dermatol. 2007;35: 1-13. [11] KWON OS, YOO HG, HAN JH, et al. Photoaging-associated changes in epidermal proliferative cell fractions in vivo. Arch Dermatol Res. 2008; 300(1):47-52. [12] KARRAN P, BREM R. Protein oxidation, UVA and human DNA repair. DNA Repair (Amst). 2016,44:178-185. [13] WEIHERMANN AC, LORENCINI M, BROHEM CA, et al. Elastin structure and its involvement in skin photoageing. Int J Cosmet Sci. 2017;39(3):241-247. [14] FISHER GJ, KANG S, VARANI J, et al. Mechanisms of photoaging and chronological skin aging. Arch Dermatol. 2002;138(11):1462-1470. [15] WANG Y, LAUER ME, ANAND S, et al. Hyaluronan synthase 2 protects skin fibroblasts against apoptosis induced by environmental stress. J Biol Chem. 2014;289(46):32253-32265. [16] RINNERTHALER M, BISCHOF J, STREUBEL MK, et al. Oxidative stress in aging human skin. Biomolecules. 2015;5(2):545-589. [17] LIDIJA M, ANA C G, MARINA C, et al. Short overview of ROS as cell function regulators and their implications in therapy concepts. Cells. 2019;8(8):793. [18] TSATSOU F, TRAKATELLI M, PATSATSI A, et al. Extrinsic aging: UV-mediated skin carcinogenesis. Dermatoendocrinol. 2012;4(3):285-297. [19] RAVANAT JL, DOUKI T, CADET J. Direct and indirect effects of UV radiation on DNA and its components. J Photochem Photobiol B. 2001;63(1-3):88-102. [20] BUCKINGHAM EM, KLINGELHUTZ AJ. The role of telomeres in the ageing of human skin. Exp Dermatol. 2011;20(4):297-302. [21] SIEGL-CACHEDENIER I, FLORES I, KLATT P, et al. Telomerase reverses epidermal hair follicle stem cell defects and loss of long-term survival associated with critically short telomeres. J Cell Biol. 2007;179(2):277-290. [22] NISHIHARA S. Glycans in stem cell regulation: from Drosophila tissue stem cells to mammalian pluripotent stem cells. FEBS Lett. 2018;592(23):3773-3790. [23] OINAM L, CHANGARATHIL G, RAJA E, et al. Glycome profiling by lectin microarray reveals dynamic glycan alterations during epidermal stem cell aging. Aging Cell. 2020;19(8):e13190. [24] CHARRUYER A, WEISENBERGER T, LI H, et al. Decreased p53 is associated with a decline in asymmetric stem cell self-renewal in aged human epidermis. Aging Cell. 2021;20(2):e13310. [25] PALAZZO E, MORANDI P, LOTTI R, et al. Notch cooperates with survivin to maintain stemness and to stimulate proliferation in human keratinocytes during ageing. Int J Mol Sci. 2015;16(11):26291-26302. [26] WILLIAMS SE, BERONJA S, PASOLLI HA, et al. Asymmetric cell divisions promote Notch-dependent epidermal differentiation. Nature. 2011;470 (7334):353-358. [27] DAINICHI T, HAYDEN MS, PARK SG, et al. PDK1 is a regulator of epidermal differentiation that activates and organizes asymmetric cell division. Cell Rep. 2016;15(8):1615-1623. [28] HSU YC, LI L, FUCHS E. Emerging interactions between skin stem cells and their niches. Nat Med. 2014;20(8):847-856. [29] GEHART H, CLEVERS H. Tales from the crypt: new insights into intestinal stem cells. Nat Rev Gastroenterol Hepatol. 2019;16(1):19-34. [30] JAMESON J, UGARTE K, CHEN N, et al. A role for skin gammadelta T cells in wound repair. Science. 2002;296(5568):747-749. [31] Tidball JG. Regulation of muscle growth and regeneration by the immune system. Nat Rev Immunol. 2017;17(3):165-178. [32] NETEA MG, DOMINGUEZ-ANDRES J, BARREIRO LB, et al. Defining trained immunity and its role in health and disease. Nat Rev Immunol. 2020;20(6): 375-388. [33] BLAU HM, COSGROVE BD, HO AT. The central role of muscle stem cells in regenerative failure with aging. Nat Med. 2015;21(8):854-862. [34] HSU YC, LI L, FUCHS E. Transit-amplifying cells orchestrate stem cell activity and tissue regeneration. Cell. 2014;157(4):935-949. [35] MONDAL BC, SHIM J, EVANS CJ, et al. Pvr expression regulators in equilibrium signal control and maintenance of Drosophila blood progenitors. Elife. 2014;3:e3626. [36] PORPIGLIA E, SAMUSIK N, HO A, et al. High-resolution myogenic lineage mapping by single-cell mass cytometry. Nat Cell Biol. 2017;19(5):558-567. [37] YU VW, SCADDEN DT. Hematopoietic stem cell and its bone marrow niche. Curr Top Dev Biol. 2016;118:21-44. [38] MARSH E, GONZALEZ DG, LATHROP EA, et al. Positional stability and membrane occupancy define skin fibroblast homeostasis in vivo. Cell. 2018; 175(6):1620-1633. [39] BLAU HM, COSGROVE BD, HO AT. The central role of muscle stem cells in regenerative failure with aging. Nat Med. 2015;21(8):854-862. [40] KEYES BE, LIU S, ASARE A, et al. Impaired epidermal to dendritic t cell signaling slows wound repair in aged skin. Cell. 2016;167(5):1323-1338. [41] FAN X, RUDENSKY AY. Hallmarks of tissue-resident lymphocytes. Cell. 2016; 164(6):1198-1211. [42] LINDEMANS CA, CALAFIORE M, MERTELSMANN AM, et al. Interleukin-22 promotes intestinal-stem-cell-mediated epithelial regeneration. Nature. 2015;528(7583):560-564. [43] VON MOLTKE J, JI M, LIANG HE, et al. Tuft-cell-derived IL-25 regulates an intestinal ILC2-epithelial response circuit. Nature. 2016;529(7585):221-225. [44] KEYES BE, LIU S, ASARE A, et al. Impaired epidermal to dendritic t cell signaling slows wound repair in aged skin. Cell. 2016;167(5):1323-1338. [45] GE Y, MIAO Y, GUR-COHEN S, et al. The aging skin microenvironment dictates stem cell behavior. Proc Natl Acad Sci U S A. 2020;117(10):5339-5350. [46] NAIK S, LARSEN SB, GOMEZ NC, et al. Inflammatory memory sensitizes skin epithelial stem cells to tissue damage. Nature. 2017;550(7677):475-480. [47] NAIK S, LARSEN SB, GOMEZ NC, et al. Author correction: inflammatory memory sensitizes skin epithelial stem cells to tissue damage. Nature. 2018; 560(7716):E2. [48] PARK B S, JANG K A, SUNG J H, et al. Adipose-derived stem cells and their secretory factors as a promising therapy for skin aging. Dermatol Surg. 2008; 34(10):1323-1326. [49] TIMMERS L, LIM SK, ARSLAN F, et al. Reduction of myocardial infarct size by human mesenchymal stem cell conditioned medium. Stem Cell Res. 2007; 1(2):129-137. [50] LEE SH, JIN SY, SONG JS, et al. Paracrine effects of adipose-derived stem cells on keratinocytes and dermal fibroblasts. Ann Dermatol. 2012;24(2):136-143. [51] KUSUMA GD, CARTHEW J, LIM R, et al. Effect of the microenvironment on mesenchymal stem cell paracrine signaling: opportunities to engineer the therapeutic effect. Stem Cells Dev. 2017;26(9):617-631. [52] PROCKOP DJ. Inflammation, fibrosis, and modulation of the process by mesenchymal stem/stromal cells. Matrix Biol. 2016;51:7-13. [53] KIM WS, PARK BS, PARK SH, et al. Antiwrinkle effect of adipose-derived stem cell: activation of dermal fibroblast by secretory factors. J Dermatol Sci. 2009;53(2):96-102. [54] WANG J V, SCHOENBERG E, ZAYA R, et al. The rise of stem cells in skin rejuvenation: a new frontier. Clin Dermatol. 2020;38(4):494-496. [55] CHARLES-DE-SA L, GONTIJO-DE-AMORIM N, SBARBATI A, et al. Photoaging skin therapy with PRP and ADSC: a comparative study. Stem Cells Int. 2020; 2020:2032359. [56] FAN F, LI Y, LIU Y, et al. Overexpression of klotho in adipose-derived stem cells protects against UVB-induced photoaging in co-cultured human fibroblasts. Mol Med Rep. 2018;18(6):5473-5480. [57] PHINNEY DG, PITTENGER MF. Concise review: MSC-Derived exosomes for cell-free therapy. Stem Cells. 2017;35(4):851-858. [58] LAI RC, ARSLAN F, LEE MM, et al. Exosome secreted by MSC reduces myocardial ischemia/reperfusion injury. Stem Cell Res. 2010;4(3):214-222. [59] CASADO-DIAZ A, QUESADA-GOMEZ JM, DORADO G. Extracellular vesicles derived from mesenchymal stem cells (MSC) in regenerative medicine: applications in skin wound healing. Front Bioeng Biotechnol. 2020;8:146. [60] MISTRY DS, CHEN Y, SEN GL. Progenitor function in self-renewing human epidermis is maintained by the exosome. Cell Stem Cell. 2012;11(1):127-135. [61] BASU J, LUDLOW JW. Exosomes for repair, regeneration and rejuvenation. Expert Opin Biol Ther. 2016;16(4):489-506. [62] CHAN BD, WONG WY, LEE MM, et al. Exosomes in inflammation and inflammatory disease. Proteomics. 2019;19(8):e1800149. [63] XIAO J, PAN Y, LI X H, et al. Cardiac progenitor cell-derived exosomes prevent cardiomyocytes apoptosis through exosomal miR-21 by targeting PDCD4. Cell Death Dis. 2016;7(6):e2277. [64] ZHU L, KALIMUTHU S, GANGADARAN P, et al. Exosomes derived from natural killer cells exert therapeutic effect in melanoma. Theranostics. 2017; 7(10):2732-2745. [65] BORGHESAN M, FAFIAN-LABORA J, ELEFTHERIADOU O, et al. Small extracellular vesicles are key regulators of non-cell autonomous intercellular communication in senescence via the interferon protein IFITM3. Cell Rep. 2019;27(13):3956-3971. [66] DAVIS C, DUKES A, DREWRY M, et al. MicroRNA-183-5p Increases with age in bone-derived extracellular vesicles, suppresses bone marrow stromal (Stem) cell proliferation, and induces stem cell senescence. Tissue Eng Part A. 2017;23(21-22):1231-1240. [67] DONG C, ZHOU Q, FU T, et al. Circulating exosomes derived-mir-146a from systemic lupus erythematosus patients regulates senescence of mesenchymal stem cells. Biomed Res Int. 2019;2019:6071308. [68] Jeon OH, Wilson DR, Clement CC, et al. Senescence cell-associated extracellular vesicles serve as osteoarthritis disease and therapeutic markers. JCI Insight. 2019;4(7):e125019. [69] KHALYFA A, MARIN JM, QIAO Z, et al. Plasma exosomes in OSA patients promote endothelial senescence: effect of long-term adherent continuous positive airway pressure. Sleep. 2020;43(2):zsz217. [70] MENON R. Initiation of human parturition: signaling from senescent fetal tissues via extracellular vesicle mediated paracrine mechanism. Obstet Gynecol Sci. 2019;62(4):199-211. [71] WONG PF, TONG KL, JAMAL J, et al. Senescent HUVECs-secreted exosomes trigger endothelial barrier dysfunction in young endothelial cells. EXCLI J. 2019;18:764-776. [72] HA DH, KIM HK, LEE J, et al. Mesenchymal stem/stromal cell-derived exosomes for immunomodulatory therapeutics and skin regeneration. Cells. 2020;9(5):1157. [73] Choi EW, Seo MK, Woo EY, et al. Exosomes from human adipose-derived stem cells promote proliferation and migration of skin fibroblasts. Exp Dermatol. 2018;27(10):1170-1172. [74] YOSHIDA M, SATOH A, LIN JB, et al. Extracellular vesicle-contained eNAMPT delays aging and extends lifespan in mice. Cell Metab. 2019;30(2):329-342. [75] LEE BR, KIM JH, CHOI ES, et al. Effect of young exosomes injected in aged mice. Int J Nanomedicine. 2018;13:5335-5345. [76] LIU S, MAHAIRAKI V, BAI H, et al. Highly purified human extracellular vesicles produced by stem cells alleviate aging cellular phenotypes of senescent human cells. Stem Cells. 2019;37(6):779-790. [77] KIM S, LEE SK, KIM H, et al. Exosomes secreted from induced pluripotent stem cell-derived mesenchymal stem cells accelerate skin cell proliferation. Int J Mol Sci. 2018;19(10):3119. [78] HAN C, JEONG D, KIM B, et al. Mesenchymal stem cell engineered nanovesicles for accelerated skin wound closure. ACS Biomater Sci Eng. 2019;5(3):1534-1543. [79] XIONG M, ZHANG Q, HU W, et al. Exosomes from adipose-derived stem cells: the emerging roles and applications in tissue regeneration of plastic and cosmetic surgery. Front Cell Dev Biol. 2020;8:574223. [80] YANG JA, CHUNG HM, WON CH, et al. Potential application of adipose-derived stem cells and their secretory factors to skin: discussion from both clinical and industrial viewpoints. Expert Opin Biol Ther. 2010;10(4):495-503. [81] KIM WS, PARK BS, KIM HK, et al. Evidence supporting antioxidant action of adipose-derived stem cells: protection of human dermal fibroblasts from oxidative stress. J Dermatol Sci. 2008;49(2):133-142. [82] GUO S, WANG T, ZHANG S, et al. Adipose-derived stem cell-conditioned medium protects fibroblasts at different senescent degrees from UVB irradiation damages. Mol Cell Biochem. 2020;463(1-2):67-78. [83] OH M, LEE J, KIM YJ, et al. Exosomes derived from human induced pluripotent stem cells ameliorate the aging of skin fibroblasts. Int J Mol Sci. 2018;19(6):1715. [84] MYEONGSIK O, YU JK, YOUNG JS, et al. Promotive effects of human induced pluripotent stem cell-conditioned medium on the proliferation and migration of dermal fibroblasts. Biotechnol Bioproc Eng. 2017;22(5):561-568. [85] CHA H, HONG S, PARK JH, et al. Stem cell-derived exosomes and nanovesicles: promotion of cell proliferation, migration, and anti-senescence for treatment of wound damage and skin ageing. Pharmaceutics. 2020; 12(12):1135. [86] BRANSCOME H, PAUL S, KHATKAR P, et al. Stem cell extracellular vesicles and their potential to contribute to the repair of damaged CNS cells. J Neuroimmune Pharmacol. 2020;15(3):520-537. [87] JANG SC, KIM OY, YOON CM, et al. Bioinspired exosome-mimetic nanovesicles for targeted delivery of chemotherapeutics to malignant tumors. ACS nano. 2013;7(9):7698-7710. [88] OH M, LEE J, KIM YJ, et al. Exosomes derived from human induced pluripotent stem cells ameliorate the aging of skin fibroblasts. Int J Mol Sci. 2018;19(6):1715. [89] KIM J, HAN C, JO W, et al. Cell-engineered nanovesicle as a surrogate inducer of contact-dependent stimuli. Adv Healthc Mater. 2017. doi: 10.1002/adhm.201700381. [90] LEE H, CHA H, PARK JH. Derivation of cell-engineered nanovesicles from human induced pluripotent stem cells and their protective effect on the senescence of dermal fibroblasts. Int J Mol Sci. 2020;21(1):343. [91] 周琦琦,孙振,刘洋洋,等.过表达NAMPT脐带间充质干细胞外泌体的抗衰老作用[J].扬州大学学报(农业与生命科学版),2021,42(4):1-6. |
| [1] | 潘钟杰, 秦志鸿, 郑铁军, 丁晓飞, 廖世杰. 股骨头坏死发病机制中非编码RNA的靶标性[J]. 中国组织工程研究, 2023, 27(9): 1441-1447. |
| [2] | 蔡志浩, 谢召勇. 股骨颈前倾角测量评估:如何建立统一的方法和标准[J]. 中国组织工程研究, 2023, 27(9): 1448-1454. |
| [3] | 党 祎, 杜成砚, 姚红林, 袁能华, 曹 金, 熊 山, 张顶梅, 王 信. 激素型骨坏死与氧化应激[J]. 中国组织工程研究, 2023, 27(9): 1469-1476. |
| [4] | 王 继, 张 敏, 杨中亚, 张 龙. 体力活动干预2型糖尿病肌少症的研究现状[J]. 中国组织工程研究, 2023, 27(8): 1272-1277. |
| [5] | 聂晨晨, 苏凯奇, 高 静, 凡勇福, 阮晓迪, 袁 洁, 段昭远, 冯晓东. 环状RNA调控脑缺血发病的作用与机制[J]. 中国组织工程研究, 2023, 27(8): 1286-1291. |
| [6] | 高 煜, 韩佳慧, 葛 新. 脊髓缺血再灌注损伤后的免疫炎性微环境[J]. 中国组织工程研究, 2023, 27(8): 1300-1305. |
| [7] | 徐星星, 文超举, 孟茂花, 王勤英, 陈镜桥, 董 强. 口腔种植中的碳纳米材料[J]. 中国组织工程研究, 2023, 27(7): 1062-1070. |
| [8] | 李 诚, 郑国爽, 蒯贤东, 于炜婷. 海藻酸盐支架修复关节软骨[J]. 中国组织工程研究, 2023, 27(7): 1080-1088. |
| [9] | 徐 聪, 赵 赫, 孙 岩. 生物材料导管修复面神经损伤与再生[J]. 中国组织工程研究, 2023, 27(7): 1089-1095. |
| [10] | 陈世崧, 刘晓红, 徐志云. 人工生物瓣膜的研究现状及展望[J]. 中国组织工程研究, 2023, 27(7): 1096-1102. |
| [11] | 芦 笛, 张 成, 段荣泉, 刘宗响. 磷酸钙陶瓷骨修复材料的骨诱导性能[J]. 中国组织工程研究, 2023, 27(7): 1103-1109. |
| [12] | 史业弘, 王 成, 陈世玖. 小口径人工血管的早期血栓形成与预防[J]. 中国组织工程研究, 2023, 27(7): 1110-1116. |
| [13] | 唐昊天, 廖荣东, 田 京. 压电材料修复骨缺损的应用及设计思路[J]. 中国组织工程研究, 2023, 27(7): 1117-1125. |
| [14] | 薛 婷, 张新日, 孔晓梅. 纳米材料多模态显像示踪技术在间充质干细胞治疗尘肺中的应用[J]. 中国组织工程研究, 2023, 27(7): 1133-1140. |
| [15] | 袁 维, 刘静东, 徐广辉, 康 健, 李富平, 王英杰, 支中正, 李冠武. 人血管周围干细胞成骨分化及Wnt/β-catenin信号通路的调控[J]. 中国组织工程研究, 2023, 27(6): 866-871. |
皮肤衰老是生理性、不可避免的,其具体表现多种多样,包括组织变得萎缩、脆弱,出现修复缺陷、免疫缺陷及易受感染[1]。皮肤衰老受内在及外在等多种不同因素的影响,同时在衰老局部留下多种印记。皮肤衰老所导致的一系列不良后果,使得人们对抗衰老的需求越来越强烈。
此篇综述旨在讲述皮肤衰老的表现及衰老原因,尤其是在表皮干细胞层面,着重阐述了衰老皮肤中表皮干细胞的变化,同时表述极受关注的干细胞相关抗衰老的研究进展,其中主要描述了应用较多的间充质干细胞及其衍生物在皮肤抗衰老中的研究成果及作用机制。提出干细胞及其衍生物作用于衰老皮肤可能在于影响干细胞部分基因表达、降低活性氧及改善生态位等,进而改变干细胞增殖及分化行为,改善皮肤衰老。同时提出了根据衰老表皮干细胞的变化,结合基因工程等技术,针对性地应用干细胞手段扭转衰老表皮干细胞的改变。
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
1.1.1 检索者 由第一作者在2021年11月进行检索。
1.1.2 检索文献时限 2016-11-01/2021-11-01。
1.1.3 检索数据库 PubMed和中国知网数据库。
1.1.4 检索词 中文检索词为“皮肤衰老,表皮干细胞,干细胞抗衰老”;英文检索词为“skin aging, epidermal stem cell, stem cell anti-aging”。
1.1.5 检索策略 中文检索式为:皮肤衰老OR表皮干细胞OR干细胞抗衰老;英文检索式为“Skin aging [MeSH terms]OR epidermal stem cell [MeSH terms]OR stem cell anti-aging[MeSH terms]”。
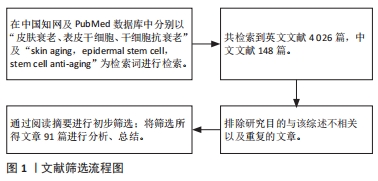
1.1.6 检索文献量 共检索到英文文献4 026篇,中文文献148篇。
1.2 入组标准 将所检索文献进行筛选,去除重复文献,优先选择发表时间靠前的文献,选择与研究目的和研究内容紧密联系的文献纳入分析。
1.3 文献质量评估 由第一作者进行信息情报检索,共选取91篇相关文献进行归纳整理,见图1。
在干细胞领域的皮肤抗衰老研究表明,干细胞及其衍生物通过激活细胞功能、重建弹性纤维蛋白、减少胶原蛋白降解、降低活性氧水平等从而减少皱纹、增加真皮厚度,取得了十分可观的抗衰老成果,其具体作用机制复杂,仍待探索。结合基因工程的干细胞及其衍生物的抗衰老能力也得以验证,但是相对基础支撑研究较少,对应基因工程干细胞及其衍生物的抗衰老研究局限。
3.2 综述的特点 该综述一方面总结出皮肤衰老的表现及机制,其中着重表述皮肤衰老中表皮干细胞的变化;另一方面总结了干细胞相关的皮肤抗衰老,其中着重表述间充质干细胞及其衍生物在皮肤抗衰老中的应用。在以上研究基础上,文章系统阐述了干细胞及其衍生物在皮肤抗衰老中的应用及研究进展。分析了干细胞及其衍生物在皮肤抗衰老中的作用机制。提出干细胞及其衍生物可能作用于表皮干细胞及其生态位,改变表皮干细胞增殖、分化及分泌行为,改善皮肤衰老。其具体机制包括:增加细胞增殖、降低活性氧水平、调节基因表达等。
3.3 综述的局限性 关于皮肤衰老及抗衰老领域的研究方向及研究内容多样,皮肤衰老因素及机制复杂,受不同条件影响,衰老皮肤不同组织结构都发生相应改变,该综述着重总结表皮干细胞变化,其他组织衰老相对描述较少。干细胞抗皮肤衰老研究中,干细胞种类多样,该综述着重总结间充质干细胞。
3.4 综述的意义 皮肤是人体与外界环境直接接触的载体,作为人体抵御外界有害因素的第一道防线,一生都要面对来自内源及外源的各种理化及生物损害因素的挑战。皮肤的衰老,对个人而言一方面会使其对机体保护能力下降,最终致病;另一方面,现如今越来越多人关注到皮肤衰老对个人外观的影响,包括皮肤松弛、皱纹、色素沉着等;这些因素带来皮肤抗衰领域研究热潮。该综述总结了皮肤衰老的因素、表现及机制等,同时总结了抗衰老领域中前景可观的干细胞及其衍生物在皮肤抗衰老领域的研究进展,这将在一定程度上协助进一步对于皮肤衰老机制的研究探索,同时对皮肤抗衰老的方法及机制的研究起一定引导作用。
3.5 展望 干细胞在皮肤抗衰老的应用中取得显著效果,在未来该领域的研究仍有许多方向,如最近提出的关于植物干细胞应用于皮肤抗衰老的研究。并且在干细胞抗衰老的基础上,可以针对性应用基因工程等手段,进一步具化。许多的证据表明,间充质干细胞外泌体具有与间充质干细胞相似的抗炎和免疫调节特性。来源于间充质干细胞的外泌体可以通过过滤进行灭菌,并作为现成产品生产,而间充质干细胞自身则不能。干细胞外泌体中,用于研究的类型诸多,其中笔者认为细胞工程纳米囊泡,可以成为未来皮肤抗衰老的主要方向。细胞工程纳米囊泡建立在细胞工程的基础上,具有强大的发展空间,其安全性及有效性应该得到关注,当然细胞工程纳米囊泡的应用需要建立在大量衰老及年轻化的机制基础研究之上。除此之外,干细胞衍生物制成产品在临床得以应用还有很多困难需要克服,包括其安全性、有效性的测定,衍生物的获取、分离、定性及定量等都有待标准化。
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程

文题释义:
干细胞:是一类具有自我更新和多向分化潜能的细胞,具有再生、替代、修复和分化能力,在个体发育和疾病发生中扮演着重要角色,是再生治疗中的关键细胞,根据个体发育过程中出现的先后次序不一样,可分为胚胎干细胞和成体干细胞。
皮肤衰老:是一种自然过程,受内源性及外源性因素影响,表现为皱纹、粗糙、色素沉着及弹性降低等。
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
皮肤衰老是一种自然过程,受内源性及外源性因素影响,表现为皱纹、粗糙、色素沉着及弹性降低等。皮肤抗衰老是通过相关抗衰老技术干预,从而减少自由基损伤、增加胶原蛋白量及皮肤厚度等缓解衰老皮肤症状。文章综述皮肤衰老及干细胞用于皮肤抗衰老的研究进展,为干细胞相关皮肤抗衰老的应用及研究提供理论依据。
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||