2.1 自组装肽定义及类别与功能特性
2.1.1 自组装肽定义 氨基酸是蛋白质的基本成分,具有多种功能,包括催化、支持细胞外基质中的细胞、DNA复制和运输所需的分子等[4]。自组装被定义为一种由于分子内/分子间相互作用,将混沌的分子单元组织成有序结构的自发的和可逆的过程,分子内和分子间的引力/排斥力的平衡控制着组装过程,其中分子间自组装肽通过氢键、离子键、范德华键、疏水相互作用和水介导的氢键等多种非共价相互作用形成结构清晰、稳定的组织[5]。此外,氨基酸侧链的各种性质(负电荷或正电荷、疏水性、亲水性和极性)为无限序列组合的化学修饰提供了可能性。不仅如此,氨基酸的一级结构为与聚合物底物的连接提供了场所。除了自组装外,还可以很容易地诱导出各种特性,包括自愈合、剪切稀化和形状记忆等。自20世纪80年代末以来,从天然蛋白质中提取的具有自组装特性的短肽开始引起人们的关注,见图1。
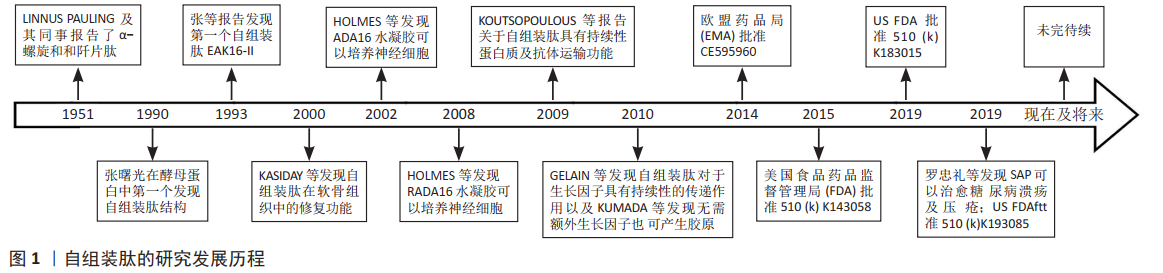
①β-片肽:这些肽由12-16个交替的亲水性残基(R或K为正残基,E或D为负残基)和疏水残基(A或L残基)组成,在水介质中形成一侧为疏水面,另一侧为亲水面的β-Sheet结构。②弹性蛋白样多肽:是一类由原弹性蛋白在一定生理条件下自组装而来的基因工程多肽[6],由重复的“VPGXG”序列组成,其中X位的极性(除脯氨酸外的一种可变氨基酸)决定了肽的转变温度[7]。③多肽两亲性:两肽类化合物是一种含有单链或多烷链的肽头的杂化化合物[8],具体是将具有自组装能力的多肽附着到两亲性表面活性剂上,从而控制纳米结构组装成圆柱形或纤丝几何形状。④α-螺旋:是蛋白质中发现的一种基本折叠模式,这些α-螺旋卷曲也被称为水凝胶自组装纤维 [9-10]。⑤胶原纤维肽:3个多脯氨酸-Ⅱ型螺旋之间的周期性链间氢键组成胶原三螺旋[11],每条链由“G-X-Y”三肽重复序列组成,由于使用动物源性胶原蛋白的局限性,天然的胶原样肽被开发出的各种人工胶原样肽所代替形成更加稳定的分子结构[12]。
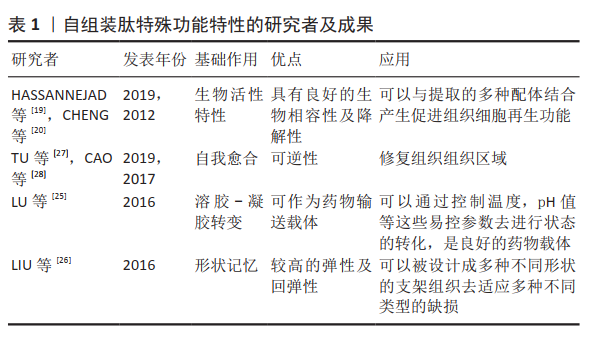
2.1.3 自组装肽功能特性 良好的生物相容性和力学性能使自组装肽水凝胶在生物医学领域具有广泛的应用前景。接下来文章将从生物活性、溶胶-凝胶转变、自我修复和形状记忆功能等方面分别来概括自组装肽近期研究的成果。
(1)生物活性特性:尽管裸露自组装肽水凝胶在体内外都表现出良好的生物相容性和生物降解性,但在生物医学领域的应用需要增强细胞黏附和整合素结合。大量研究已经发现,从细胞外基质蛋白中提取出的许多配体,包括LGTIPG,PDGSR,LRE,LRCDN,IKLLI,KQAGDV和REDV可以促进细胞黏附[13-15]。尤其是层粘连蛋白衍生的IKVAV配体能促进细胞黏附、分化和轴突生长[16-18],当它与RADA16-I肽或两亲分子连接时可通过延长轴突和减轻星形胶质细胞增生以及减少胶质细胞瘢痕形成促进神经再生[19]。有研究将eYIGSR配体加入到β片状形成肽中,可以观察到阿尔茨海默病大鼠的空间学习和记忆功能显著提高[20]。关于促进成骨能力的研究结果也层出不穷,研究人员将从骨形态发生蛋白7中提取的骨形成肽(BFP,如GQGFSYPYKAVFSTQ和KGGQGFSYPYKAVFSTQ)去处理研究组,可以观察到经骨形成肽处理的干细胞发生成骨表型的转化[21-22]。
除此之外,从骨形态发生蛋白中提取骨诱导功能肽序列,这些骨形态发生蛋白可以通过异构体与靶细胞相互作用使丝氨酸/苏氨酸激酶激活Smad细胞内途径[23]。FINETTI等[24]研究发现,血管内皮生长因子衍生出的QK肽序列在诱导内皮细胞增殖、迁移和侵袭方面起着与血管内皮生长因子相似的作用。
(2)溶胶-凝胶转变:可注射水凝胶因具有亲水性、非侵入性和生物相容性等优势可被用作药物、细胞和其他生物活性分子的载体,而溶胶-凝胶转变特性是设计的前提条件。对于某些肽水凝胶,可以通过改变介质的离子强度、温度或pH值来触发从液体到类固体状态(凝胶)的转变[25]。
(3)形状记忆特性:由于弹性蛋白样多肽具有较高的弹性和回弹性,因此常被设计为有形状记忆的水凝胶去适应不同形状及大小的骨组织缺损。例如,LIU等[26]便开发出了具有固定形状、优异柔韧性和较好可注射性的多功能弹性蛋白杂化水凝胶。
(4)自我愈合特性:大多数生物系统损伤后可自发愈合,因此研究出大量具有类似自愈合性能的智能合成材料,自组装肽通过氢键、疏水相互作用、离子相互作用、π-π堆积和主客体相互作用可逆性的特点已经被报道,并成功修复了组织的受损区域[27-29],详见表1。
2.2 自组装肽在牙体牙髓方向的应用
2.2.1 自组装肽在牙本质敏感中的应用 牙本质敏感可由牙龈退缩引起,通常是在牙周治疗或牙齿龋坏之后。流体力学理论认为,剧烈的疼痛是由牙本质液流量的变化引起的,这些变化是由外界刺激如触觉、寒冷和/或空气刺激引起的,体验到疼痛的特征是暴露于刺激后轻微的、短暂的疼痛。传统意义上的治疗是通过降低神经兴奋水平或封闭牙本质小管,然而使用任何一种药剂都需要几天到几周症状才有所缓解[30]。一项临床研究报道,使用自组装肽基质凝胶的实验组较对照组具有更高的抗敏感特性[31],并且临床反应时间也明显缩短,这种差异可能来源于作用模式的不同,由于自组装肽基质有钙离子结合点,牙本质表层会吸引唾液中的钙离子形成羟基磷灰石晶体[32],从而形成更坚固、更稳定、更不容易磨损的组织层[33]。因此这是一种新的牙本质敏感治疗方法的研究结果,在后期研究者应该进行更多的临床研究并提供动力。
2.2.2 自组装肽在龋病中的应用 龋病被定义为在细菌等因素下牙体组织脱矿-再矿化平衡失衡,牙齿矿物质的净流失最终形成牙体缺损。传统治疗中,宏观层面的空洞性龋损是通过手术方式进行“治疗”的,包括彻底去除龋齿和封闭龋齿。目前越来越多的国际共识支持使用侵入性较小的干预措施,其重点放在病变控制上,例如生物组织的再矿化和再生[34]。基于先前大量关于早期龋损非侵入性和非恢复性治疗的方法,目前另一种新方法是引入自组装肽[35],P11-4(自组装肽水凝胶)用于在光滑表面上再生脱矿的牙齿组织,这种肽在脱矿的龋损区域形成3D基质,使羟基磷灰石晶体能够新生,促进引导牙釉质丢失的釉质结构再生并模仿釉质基质蛋白[36],不仅如此P11-4基质对Ca2+有很高的亲和力,可以作为从头形成羟基磷灰石的成核剂[37]。对再矿化标本的显微断层扫描(Micro CT)分析显示,再矿化可达到原始牙釉质密度的90%。临床试验也得出相似的结果,经自组装肽水凝胶治疗的龋损中有31%显示出强烈的矿化。在一项随机、对照、单盲研究中,ALKILZY等[38]采用随机对照试验设计评估了自组装肽治疗初期龋齿的安全性和临床疗效,结果未发现与治疗相关的不良事件、医疗并发症或过敏反应的报道,试验和对照治疗的临床适用性被认为是令人满意的。与传统治疗相比,自组装肽仿生技术为牙釉质再生提供了一种支架可以促进病变体的再矿化,因此,一种新的龋病治疗方式在未来不免被期待。
2.2.3 自组装肽在牙髓再生中的应用 牙髓再生的目的是用再生的牙髓样组织代替发炎/坏死的牙髓,使牙齿活力最大化,并继续发育未成熟的牙齿。基于细胞的组织工程是一种很有前途的牙本质-牙髓复合体再生方法,它利用干细胞、支架和生长因子的组合[39-40]。其中干细胞生态位是由细胞外基质蛋白、氧、营养物质和生长因子组成的交联网络构成的三维微环境。
然而,目前的牙本质-牙髓复合体再生方案有2个显著的局限性:①新形成的“牙本质样”桥通常是碎裂的、可渗透的,导致细菌再污染,这可能是现有的生物材料不能在牙髓干细胞中提供足够的附着和诱导矿化;②暴露的轴壁血供受阻导致的牙髓组织坏死,这一限制可能是牙髓中缺乏有效及快速的牙髓干细胞血管化,想要解决这一问题可以将诱导细胞黏附的支架功能化,促进细胞存活,并为牙髓干细胞的血管生成和牙齿形成提供形态发生信号[41]。细胞外基质不仅提供结构支持,还调节细胞功能,如细胞黏附、增殖和分化,此外,细胞外基质还调节各种生物活性分子(如生长因子和细胞因子)激活的信号转导通路。自组装肽是一种智能材料,它可以被修饰以生成具有与天然细胞外基质非常相似的结构的定制基质。近年来,自组装肽已被证明是组织工程中用于3D细胞培养的独特生物材料和用于软组织和矿化牙体组织的优秀候选支架[42]。由于根管具有不规则的几何形状,自组装肽可注射性的特点可以很好地填充各种形状的根管,当RADA16-I自组装肽作为载体将干细胞因子和牙髓干细胞包裹到根管内后可以提供一个更接近牙髓干细胞内部环境的三维环境,从而实现体内富含血管样结构的牙髓组织的再生[43]。
DISSANAYAKA等[44]将牙髓干细胞和人脐静脉内皮细胞在Ac-(RADA)4-CONH_2自组装肽水凝胶内共培养4周后,观察到在没有添加生长因子的情况下多肽纳米纤维水凝胶内的3D组织培养仍然支持细胞存活、迁移和毛细血管网络的形成,可能是由于牙髓干细胞通过促进人脐静脉内皮细胞的迁移和血管内皮生长因子的表达,增加血管网络的形成,从而显著地产生细胞外基质,延长血管化,并使含有共培养细胞的水凝胶矿化这一协同效应导致。研究表明,RAD(是一种自组装肽水凝胶,由水溶液中的16个残基组成)能迅速生成结构类似于天然细胞外基质的新型超分子结构,它有可能被倒入牙髓室,随后细胞在多肽水凝胶中迁移和增殖。另一项研究也得出相似结果,RAD中的牙髓干细胞表现出胞浆延长并表达重组人牙本质基质蛋白1和牙本质涎磷蛋白[45],这2种被认为是成牙细胞分化的标志物。此外干细胞+RAD的构建也显著加速了牙本质桥及具有成牙本质细胞和毛细血管牙髓样组织的形成[46-47]。
不仅如此,有研究在动物实验中将培养扩增的鼠牙髓干细胞组合移植到RAD/PRG(将2个单位的精氨酸-甘氨酸-天冬氨酸结合序列直接与RAD偶联的一种自组装肽,可以促进细胞黏附) [48],RAD/KLT(KLT是在血管内皮生长因子螺旋区域复制氨基酸的基序,与RAD结合并激活血管内皮生长因子受体,可以促进血管生成)水凝胶中也同样可以观察到牙本质桥和排列良好的成牙本质样细胞层的数量显著增加,其结构类似于天然牙齿。最近,一种被命名为“多结构域肽”的新型自组装肽被设计成显示不同“结构域”的功能区域,这些区域可以相互独立地改变和优化,从而可以设计出量身定制的自组装材料,在这种复合支架、细胞和生长因子的牙本质柱体中,多肽水凝胶在6周内降解,并被具有成牙本质细胞的血管化软结缔组织所取代[49]。大量实验研究证明了创造支持干细胞黏附和血管生成的微环境有助于牙髓的再生,而自组装肽因其自身的优势可以成为一个牙髓再生治疗的新切入点。
2.3 自组装肽在牙周方向的应用
2.3.1 自组装肽作为牙周治疗辅助的应用 牙周炎是一种由细菌感染的慢性炎症性和组织破坏性疾病,是牙齿脱落最主要的原因,现阶段临床上常采用龈下刮治及根面平整术去消除牙面和龈下结构中的病原菌菌斑,但是这些技术在有效去除致病菌斑时有一定局限性。因此,在纯机械治疗中应用抗菌剂作为一种附加疗法去防止病原菌的再繁殖方面有一定价值[50]。全身应用抗菌剂与不良反应有关,如过敏、胃肠道不耐受和细菌耐药性的发展,因此局部药物的输送显得很重要。由于自组装肽同时具有可注射性、给药系统可与牙齿表面的黏附,防止从牙周袋中脱落、生物降解性、无细胞毒性、在高浓度负荷下具有良好的分子封闭性、延长和控制释放及实现引导组织再生等能力,相对于传统的单独抗生素药物输送更加稳定。有实验研究证明封装不仅不会通过自组装肽单体与盐酸四环素、环丙沙星和盐酸多西环素的相互作用来干扰自组装[51],而且与抗生素的联合使用还可以持续让药物以较高浓度(盐酸四环素、环丙沙星和盐酸多西环素浓度分别在5.7-48.1、4.2-30.5和7.9-38.1 mg/L)的释放作用时间延长达120 h,此外,P11-4和P11-28/29释放后的抗生素浓度不仅超过了测定的最低抑菌浓度值,而且最低抑菌浓度值据报道要高出数倍,除此之外,同时自组装肽水凝胶还具有固有的抗菌活性及增强牙囊干细胞的成骨分化,可能成为未来牙周治疗的有吸引力的候选药物输送系统,为牙周后期长远的疗效提供一定的保障[52]。
2.3.2 自组装肽在牙周组织工程的应用 牙周炎损伤的牙周组织再生是牙周治疗的最终目标,如结缔组织附着物、牙骨质和牙槽骨,传统的治疗方法从形成新的附着体到形成长连接的上皮细胞都没有产生理想的结果,而想要达到最佳结果的牙周组织工程则需要合适的细胞、生物信号、支架、血液供应、机械负荷和微生物控制这些缺一不可的因素[53]。直接充填生物活性因子现场存活率较低,然而支架提供了一种模板结构来支持和促进牙周再生的基本过程[54],因此当生物材料支架与活性因子联合使用时,既能募集内源性干细胞至缺损区,又能在原位促进干细胞的增殖和分化,是一种很有前途的牙周再生的组织工程策略。多肽在大分子结构中的自组装模拟了一些自然的生物学过程(例如,胶原在骨骼中的纤维形成和釉原蛋白在发育中的牙釉质中的自组装[55]),从而提供了具有与细胞外基质相似特性的三维水凝胶支架。
Takeuchi等[56]研究得出应用RADA16的实验组比对照组更早的表现出新骨形成、牙周膜样胶原束定位于牙根表面以及增殖细胞核抗原、血管内皮生长因子和骨桥蛋白阳性细胞的明显增加。相似的结果在Yoo等[57]的研究中也可以观察到,他们使用透明质酸载体的薄片与牙周膜前体细胞联合应用到治疗Beagle犬的裂开缺损处,牙骨质形成明显多于假手术对照组,并且胶原纤维均匀地插入到新形成的牙骨质中,这一结果可以被解释为牙周膜前体细胞具有促进牙周组织再生的多潜能,而自组装肽可以提供较好的空间管理,从而促进细胞的黏附和增殖,更大概率的促进牙周再生。不仅如此,一项体外实验证明自组装肽还可以通过促进牙周膜来源的细胞增殖和增殖细胞核抗原1、血管内皮生长因子和α-平滑肌肌动蛋白阳性细胞的表达,这可能有助于促进牙周组织的愈合[58]。
众所周知,整合素为细胞迁移提供了必要的信号[59],不同的整合素在牙周病组织中表现出不同的表达模式,每个整合素亚基的选择性调控可调节牙周膜细胞的迁移,注射含有RGD或层粘连蛋白细胞黏附基序的多肽可以更有效地促进牙周膜成纤维细胞的活性。
在以往研究中已证明质量浓度10 g/L的P11-4(自组装肽)对于龋损的治疗是一种成功材料,但在近期的研究中发现,用P11-4处理SD大鼠的牙周缺损后可以看到牙根附近再生的结缔组织和新形成的骨组织中骨钙素、骨保护素和骨保护素/RANKL水平显著升高,提示形成更有利的成骨环境和更有助于成骨组织学特征的增强[60]。此外,硅酸羟丙基甲基纤维素是一种自交联的可吸收水凝胶自组装肽,由于其交联和弹性的特性可以作为一种有效的牙髓干细胞屏障,通过缓慢降解硅酸羟丙基甲基纤维素来延迟细胞和组织的定植,潜在地阻止上皮和结缔组织的迁移,在愈合阶段提高骨填充材料的稳定性[61]。综上,自组装肽的应用有望成为治疗牙周病的一种有吸引力的治疗策略,详见表2。

 文题释义:
文题释义:

