中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (25): 3956-3961.doi: 10.12307/2021.004
• 牙髓及牙周膜干细胞 Dental pulp and periodontal ligament stem cells • 上一篇 下一篇
人生长激素对人牙周膜干细胞增殖及成骨分化的影响
杨俊辉1,2,罗金莉1,2,袁小平1,2
- 1西南医科大学附属口腔医院正畸科,四川省泸州市 646000;2西南医科大学口颌面修复重建与再生实验室,四川省泸州市 646000
Effects of human growth hormone on proliferation and osteogenic differentiation of human periodontal ligament stem cells
Yang Junhui1, 2, Luo Jinli1, 2, Yuan Xiaoping1, 2
- 1Department of Orthodontics of Stomatological Hospital of Southwest Medical University, Luzhou 646000, Sichuan Province, China; 2Laboratory of Oral and Maxillofacial Reconstruction and Regeneration of Southwest Medical University, Luzhou 646000, Sichuan Province, China
摘要:
文题释义:
间充质干细胞:是一种多能干细胞,它具有干细胞的所有共性。目前能够从很多组织发现和获得间充质干细胞,比如脐血、羊水、脂肪和骨髓等组织,而最多的还是骨髓来源间充质干细胞。
人生长激素:是垂体分泌的一种肽类激素,对人体的生长发育起着非常关键的作用,能促进骨组织的生长。许多学者发现生长激素能加快正畸牙移动,缩短正畸疗程。由于生物技术的发展,应用基因重组技术已成功生产出重组人生长激素,一些欧美国家已经广泛应用重组人生长激素防治儿童生长发育不良。
背景:生长激素已被证明对于非牙源性间充质干细胞的增殖和骨向分化有促进作用,但对于人牙周膜干细胞的生物学效应还不明确。
目的:探讨人生长激素对人牙周膜干细胞增殖以及成骨分化的影响。
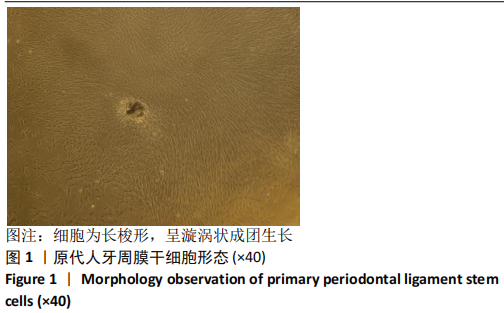
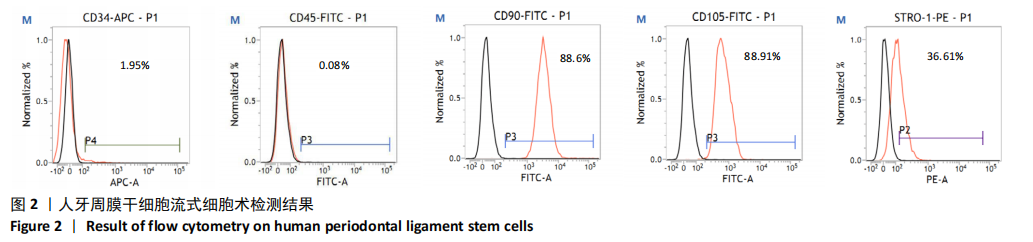
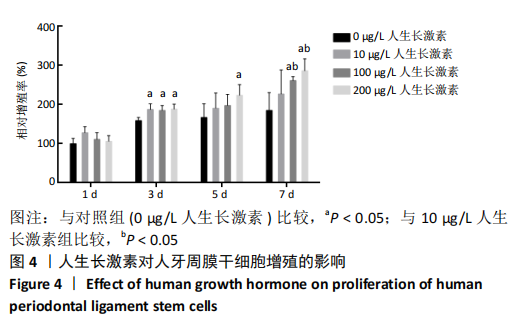
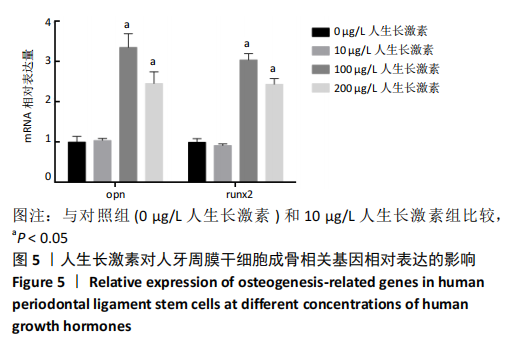
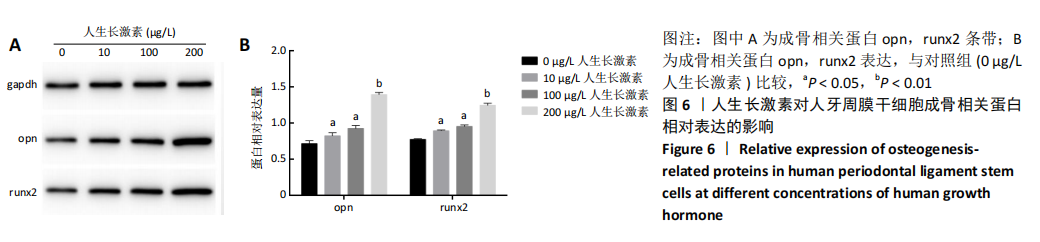
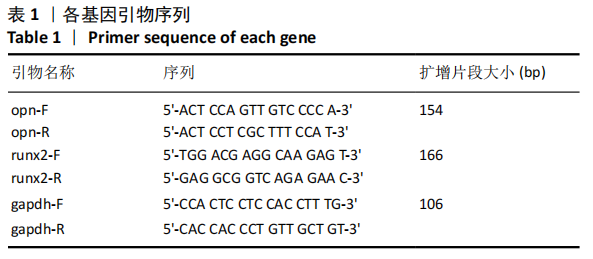
方法:用含0(对照组),10,100,200 μg/L人生长激素的α-MEM完全培养基干预第3代人牙周膜干细胞,分别在第1,3,5,7天采用CCK-8法检测各组细胞增殖情况;用含0(对照组),10,100,200 μg/L人生长激素的成骨诱导液干预第3代人牙周膜干细胞,第7天时采用Real-Time PCR和Western blot检测骨向分化相关因子opn、runx2的基因和蛋白表达,第14天时进行茜素红染色以及茜素红半定量分析人牙周膜干细胞成骨后期矿化情况。
结果与结论:100,200 μg/L人生长激素组的人牙周膜干细胞增殖能力明显优于对照组(P < 0.05);100,200 μg/L人生长激素组opn、runx2的基因和蛋白表达高于对照组(P < 0.05);100,200 μg/L人生长激素组人牙周膜干细胞的矿化能力优于对照组(P < 0.05);结果显示,在体外实验中,100,200 μg/L人生长激素能促进人牙周膜干细胞的增殖和成骨分化。
https://orcid.org/0000-0003-0747-7402(杨俊辉)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号: