设计:细胞学观察实验。
材料:
实验动物:取孕12-14 d昆明小鼠,取出胚胎,用于培养小鼠胚胎成纤维细胞。实验过程中对动物的处置符合2009年《Ethical issues in animal experimentation》相关动物伦理学标准的条例。
.jpg)
实验方法:
表达克隆pLVX-NCX1-luc+-IRES-puro-ZsGreen1的构建和鉴定:
引物设计:根据Genebank中钠钙交换体1启动子基因的cDNA序列,设计钠钙交换体1引物序列为:Forward primer 5’-CCC ATC GAT TTT ATG GTC CCT CGG CAC AGC C-3’,Reverse primer 5’-CCG GAA TTC CGG TTT ACC AAC AGT ACC GGA ATG CCA AGC-3’。分别在上下游引物引入ClaⅠ、EcoRⅠ序列(下划线),目的扩增片段为2 024 bp。
PCR扩增:在上述引物的作用下,以钠钙交换体1启动子(获赠自Yigang Wang,cincinnati,USA)的cDNA为模板进行扩增,电泳检测PCR产物,切胶回收纯化目的条带。
将载体pLVX-luc+-IRES-puro-ZsGreen1与扩增钠钙交换体1序列在ClaⅠ、EcoRⅠ酶作用下重组,取2 μL重组反应液转化50 μL感受态细胞,氨卞西林LB培养平板筛选阳性重组克隆并扩增,菌液行PCR扩增验证,挑取构建正确的菌落培养过夜,提取质粒DNA,测序验证。将构建正确标记为:pLVX- NCX1-luc+-IRES-puro-ZsGreen1。
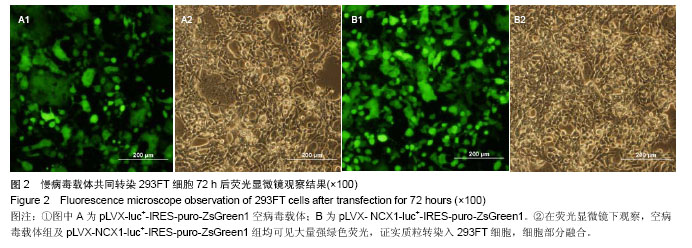
慢病毒的包装和浓缩:将慢病毒包装质粒ViraPowerTM Lentiviral Packaging Mix和载体质粒pLVX-NCX1-luc+- IRES-puro-ZsGreen1以1∶1的摩尔比例混合,在Lipofectamine2000的作用下共转染293FT细胞,置于 37 ℃、体积分数5% CO2的培养箱中培养。12 h后换液,加入新鲜293FT细胞培养液。72 h后观察有强绿色荧光及细胞融合现象时收集培养上清,4 ℃、4 500 r/min离心 15 min,将病毒上清液用0.45 μm滤膜过滤以去除细胞碎片,4 ℃、50 000×g高速离心90 min。用RNase-free L-DMEM悬浮病毒颗粒沉淀,-80 ℃冻存备用。同法构建只含增强型绿色荧光蛋白的空病毒,标记pLVX-luc+- IRES-puro-ZsGreen1。
慢病毒的滴度测定:接种293FT细胞于6孔板,每孔接种2×105个细胞,37 ℃培养过夜;第2天将慢病毒溶液用无血清DMEM(不含抗生素)按1×10-2,1×10-3,1×10-4,1×10-5,1×10-6,1×10-7进行系列稀释,将其分别加入到相应的孔中,加入聚酰胺(Polybrene)终浓度至8 mg/L,置 37 ℃、体积分数5%CO2培养箱培养。12 h后全量换液,加入新鲜的293FT培养液。第4天观察荧光表达情况,荧光细胞数随稀释倍数增加而减少,计数出表达荧光的细胞个数,将得到的数值乘以相应的稀释倍数就得到病毒原液的滴度数。
原代胎鼠成纤维细胞饲养层制备:①小鼠胚胎成纤维细胞培养:孕12-14 d昆明小鼠,取出胚胎,去头、尾、四肢和肝脏,以0.05%胰酶分次消化后培养,取第3或4代的细胞备用。②小鼠胚胎成纤维细胞饲养层处理:小鼠胚胎成纤维细胞准备后加入终浓度为10 mg/L的丝裂霉素C处理3 h,PBS洗涤3次,消化、离心并细胞计数后按5×105/cm2浓度接种到预铺0.5%明胶的培养皿中制成饲养单层细胞。
诱导多能干细胞的培养:小鼠诱导多能干细胞获赠自Dr.Shinya Yamanaka (Kyoto University,Japan),诱导多能干细胞在含有1 000 IU/mL 白血病抑制因子的DMEM中培养。未分化的诱导多能干细胞以20 000/cm2的浓度铺于低贴附的培养皿(Corning)中。诱导多能干细胞生长培养基(高糖DMEM,体积分数10%胎牛血清,0.1 mmol/L β-巯基乙醇,1%非必需氨基酸,1 000 U/mL白血病抑制因子,1%青链霉素)重悬后接种于预先用10 mg/L丝裂霉素C处理过的小鼠胚胎成纤维细胞饲养层上。每天半量更换培养基。当克隆团过大或过密时用胰酶消化传代,传代时先差速贴壁1 h去除MEF,再将悬液重新接种到刚准备的MEF饲养层上。培养液每24-48 h更换。
悬浮法制备拟胚体:取小鼠诱导多能干细胞,胰酶溶液消化制成单细胞悬液,以差速贴壁1 h去除MEF,吸取细胞悬液直接接种于35 mm细菌培养皿进行悬浮培养,每皿加入2 mL的分化培养基(高糖DMEM,体积分数10%胎牛血清,0.1 mmol/L β-巯基乙醇,1%非必需氨基酸),置于细胞培养箱中培养,每隔1 d半量换液1次,持续培养5 d。
pLVX-NCX1-luc+-IRES-puro-ZsGreen1稳定转染诱导多能干细胞株向心肌细胞分化的观察:将对数生长期诱导多能干细胞消化并离心后,以分化培养基重悬成浓度2×107 L-1细胞悬液,分化培养基为含有0.1 mmol/L非必需氨基酸、2 mmol/L谷氨酰胺、50 U/mL青霉素、50 mg/L链霉素、0.1 mmol/L β-巯基乙醇,体积分数20%胎牛血清的DMEM。细胞悬液以20 μL/滴接种到直径10 cm的细菌培养皿盖上,培养皿内加少许PBS。悬滴48 h后将形成的诱导多能干细胞拟胚体悬浮到内有新鲜培养液的培养皿内。将病毒pLVX-NCX1-luc+-IRES-puro-ZsGreen1和对照病毒pLVX-luc+-IRES-puro-ZsGreen1转染诱导多能干细胞的胚胎体。比较各组(每组50个拟胚体)之间心肌细胞的诱导效率,每天更换1次培养基。病毒感染24-48 h后,更换新鲜培养液。并同时使用嘌呤霉素进行筛选。第10天将悬浮的诱导多能干细胞拟胚体接种到预铺0.5%明胶的24孔培养板中,用上述分化液继续培养。在倒置荧光显微镜下每日观察诱导多能干细胞拟胚体生长情况及出现自发性搏动情况。
分化诱导多能干细胞肌钙蛋白I的表达:将转染得到的诱导多能干细胞株通过悬滴和悬浮培养形成的诱导多能干细胞拟胚体接种到预铺0.5%明胶的盖玻片上,出现自发性搏动细胞团时行细胞免疫组化检测。将筛选后细胞克隆分化得到的自发性搏动诱导多能干细胞拟胚体,室温下 40 g/L多聚甲醛固定15 min,冷PBS洗涤2次,0.25%Triton 100透膜10 min;PBS洗涤后加1%BSA室温下封闭30 min。加入小鼠抗肌钙蛋白I抗体(1∶200稀释)4 ℃孵育过夜。次日PBS洗涤后加入Cy3标记的肌钙蛋白I羊抗鼠荧光抗体(1∶100稀释),室温下孵育1h;PBS洗涤后复染0.1 mg/L DAPI。封固后荧光显微镜下观测。
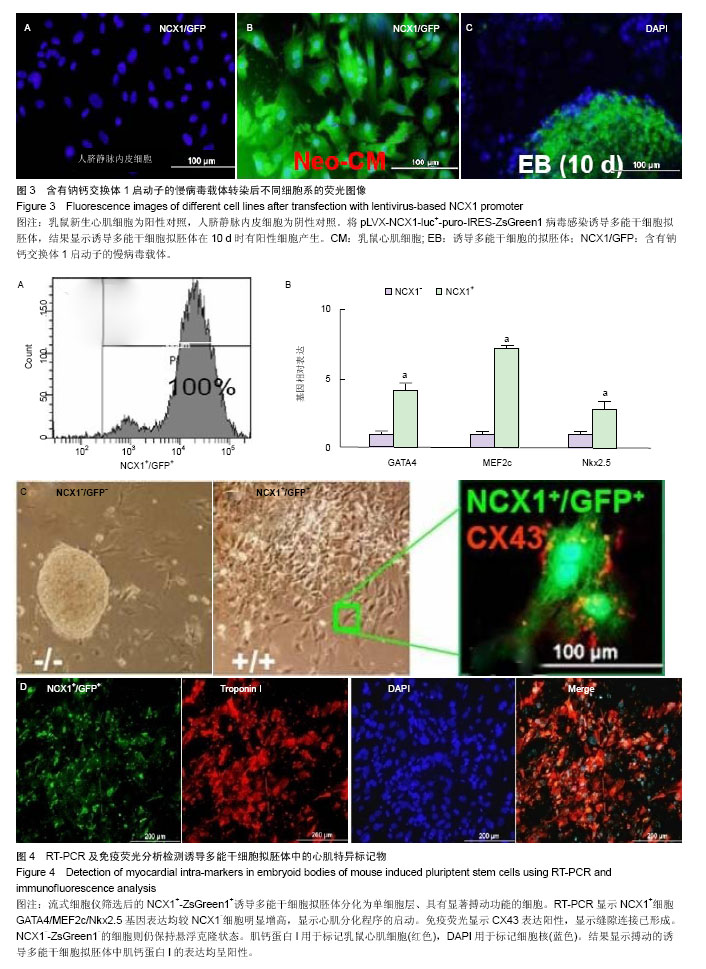
人脐静脉内皮细胞和乳鼠心肌细胞分别为阴性对照和阳性对照检测pLVX-NCX1-luc+-IRES-puro-ZsGreen1慢病毒载体的特异性:将病毒pLVX-NCX1-luc+-IRES- puro-ZsGreen1和对照病毒pLVX-luc+-IRES-puro- ZsGreen1转染人脐静脉内皮细胞系及乳鼠心肌细胞。病毒感染24-48 h后,更换新鲜培养液。室温下40 g/L多聚甲醛固定15 min,冷PBS洗涤2次,0.25%Triton 100透膜 10 min;PBS洗涤后加1%BSA室温下封闭30 min。PBS洗涤后复染0.1 mg/L DAPI。封固后荧光显微镜下观测。
pLVX-NCX1-luc+-IRES-puro-ZsGreen1及空病毒分别转染诱导多能干细胞株标记为NCX1+诱导多能干细胞及NCX1-诱导多能干细胞分化为心肌样细胞能力,在mRNA水平检测。RT-PCR检测心脏特异性转录因子GATA4,NKx2.5和MEF2C mRNA水平。引物序列:GATA4 正义链5’-GCT GGA GCT CAA GGA GAC TC-3’,反义链5’-TAC TGA TTT TCC AGC CAT TTC A-3’;NKx2.5正义链5’-GCT CCC AAC ATG ACC CTG AG-3’,反义链5’-TGC CCA TGG ACT TGG CGT ATG GCA C-3’;MEF2C正义链5’-ATA TCA TTG GCG TAT GGC AC-3’,反义链5’-AAA AAG CCA CAA ATG CTT TG-3’。
主要观察指标:pLVX-NCX1-luc+-IRES-puro- ZsGreen1的构建和鉴定;慢病毒的包装与浓缩;慢病毒的滴度测定;慢病毒载体转染纯化后诱导多能干细胞绿色荧光观察;含有钠钙交换体1启动子的慢病毒载体在转染后不同细胞系的荧光观察;RT-PCR及免疫荧光分析检测心肌特异标记物。

.jpg)