• 材料生物相容性 material biocompatibility • 上一篇 下一篇
新型生物全降解药物支架置入小型猪冠状动脉的安全性
李 虎,李晓艳,蒋学俊,郑晓新,冯高科,贺素媛,任 珊,易 欣
- 武汉大学人民医院心内科,湖北省武汉市 430060
Safety of a novel biodegradable stent implanted in the coronary artery in a porcine model
Li Hu, Li Xiao-yan, Jiang Xue-jun, Zheng Xiao-xin, Feng Gao-ke, He Su-yuan, Ren Shan, Yi Xin
- Department of Cardiology, Renmin Hospital, Wuhan University, Wuhan 430060, Hubei Province, China
摘要:
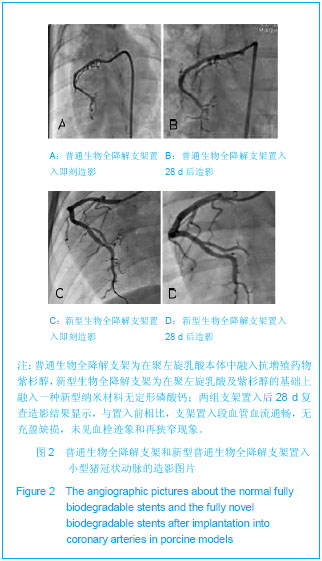
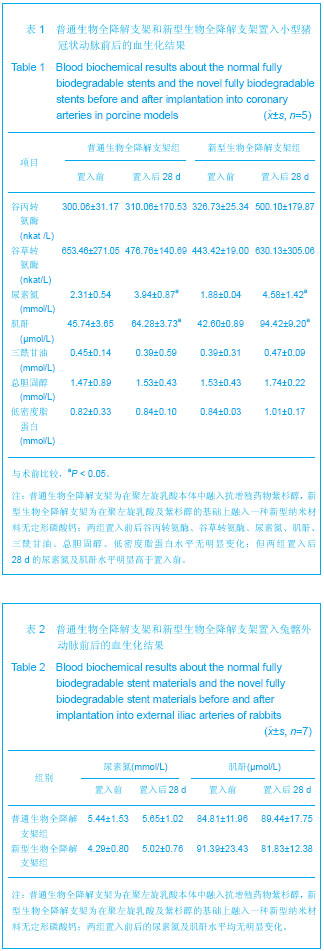
背景:目前冠状动脉支架的主要研究方向是高生物相容性的全降解生物材料及药物控释体系。 目的:评价2种新型生物全降解药物支架置入小型猪冠状动脉后的安全性。 方法:普通生物全降解支架为在聚左旋乳酸本体中融入抗增殖药物紫杉醇,新型生物全降解支架为在聚左旋乳酸及紫杉醇的基础上融入一种新型纳米材料无定形磷酸钙。①将普通生物全降解支架和新型生物全降解支架各5枚在冠状动脉造影下分别随机置入小型猪的冠状动脉,每种支架5头。于置入前和置入后28 d行血生化及C-反应蛋白水平检测;术后28 d冠状动脉造影观察支架置入段管腔通畅情况。②在微创显微镜辅助下于兔右髂外动脉分别置入普通生物全降解支架和新型生物全降解支架管状半成品(材料成分与上述支架一致),每种支架7只,在术前和术后28 d检测血尿素氮及肌酐水平。 结果与结论:置入后28 d两组猪谷丙转氨酶、谷草转氨酶、三酰甘油、总胆固醇、低密度脂蛋白及C-反应蛋白水平与置入前相比均无明显变化,但尿素氮、肌酐水平均明显高于置入前(P < 0.05);两组支架置入段血管均血流通畅、无血栓迹象和狭窄形成。支架置入前后两组兔肌酐和尿素氮水平无明显变化。表明新型生物全降解药物支架置入健康小型猪冠状动脉后是相对安全的,并且支架具有良好的组织相容性。
中图分类号:
.jpg)
.jpg)