中国组织工程研究 ›› 2015, Vol. 19 ›› Issue (23): 3736-3743.doi: 10.3969/j.issn.2095-4344.2015.23.022
• 骨髓干细胞 bone marrow stem cells • 上一篇 下一篇
骨髓间充质干细胞诱导胆管内皮细胞与电纺纳米纤维的生物相容性
杨 扬1,周家华1,殷雪琰2,徐 勇1,曹 阳2,许 茜2
- 1东南大学附属中大医院肝胆胰中心,江苏省南京市 210009;
2东南大学公共卫生学院,江苏省南京市 210009
Biocompatibility of porcine bone marrow mesenchymal stem cells-derived bile duct endothelial cells with electrospun nanofibers
Yang Yang1, Zhou Jia-hua1, Yin Xue-yan2, Xu Yong1, Cao Yang2, Xu Qian2
- 1Hepatobiliary & Pancreatic Center, Zhongda Hospital, Southeast University, Nanjing 210009, Jiangsu Province, China;
2College of Public Health, Southeast University, Nanjing 210009, Jiangsu Province, China
摘要:
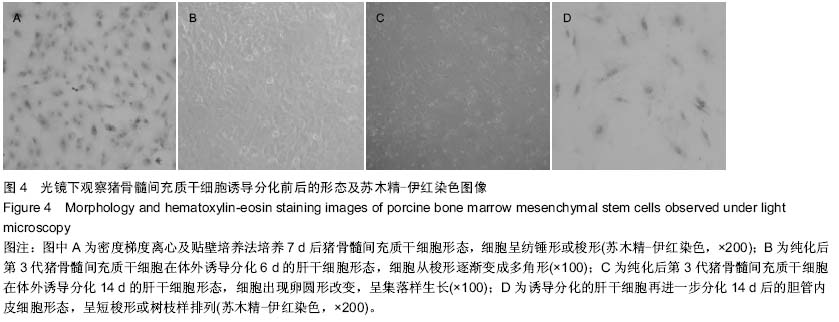
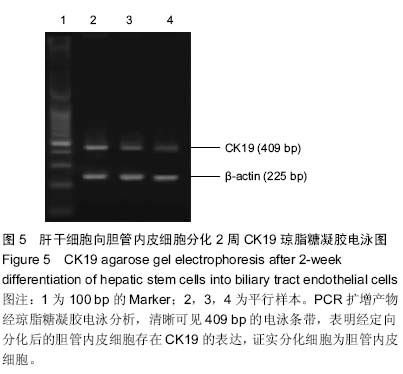
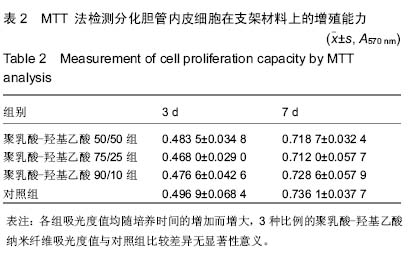
背景:胆管损伤修复是腹部外科手术的难题,组织工程胆管是解决这一难题的理想方法,而构建性能优异的组织工程胆管支架是这一研究的关键。 目的:观察猪骨髓间充质干细胞诱导分化的胆管内皮细胞与电纺纳米纤维的生物相容性。 方法:将猪骨髓间充质干细胞于体外定向分化为肝干细胞,再进一步分化为胆管内皮细胞,并通过形态学及RT-PCR对分化完成的细胞加以鉴定。用静电纺丝方法制备聚乳酸-羟基乙酸纳米纤维膜,通过扫描电镜观察其形态,并测定其短期(2周)内体外降解率。将分化的胆管内皮细胞与纳米纤维复合培养,观察细胞在纳米纤维表面的黏附、增殖能力,荧光染色观察细胞形态及在材料表面的分布情况,扫描电镜观察细胞在纳米纤维表面生长形貌。 结果与结论:骨髓间充质干细胞体外定向分化4周后,细胞呈现典型树枝状胆管内皮细胞形态学改变,并且有CK19的表达。扫描电镜照片显示电纺材料为连续的纳米纤维,纤维直径均分布在200-500 nm范围内,在2周内聚乳酸-羟基乙酸纳米纤维没有发生明显的降解。通过细胞黏附率计算、MTT法检测、荧光染色及扫描电镜观察证明猪骨髓间充质干细胞诱导分化后的胆管内皮细胞与聚乳酸-羟基乙酸纳米纤维具有良好的生物相容性。 中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程
中图分类号:


.jpg)