中国组织工程研究 ›› 2022, Vol. 26 ›› Issue (22): 3498-3504.doi: 10.12307/2022.277
• 材料生物相容性 material biocompatibility • 上一篇 下一篇
不同孔隙率多孔ZnO/羟基磷灰石复合材料的力学性能与生物相容性
孟增东1,朱 斌2,张亚楠1,罗丽琳3,张玉勤2
- 云南省第一人民医院(昆明理工大学附属医院),1骨科,3骨科病理科,云南省昆明市 650032;2昆明理工大学材料科学与工程学院,云南省昆明市 650093
Mechanical properties and biocompatibility of porous ZnO/hydroxyapatite composites with different porosities
Meng Zengdong1, Zhu Bin2, Zhang Yanan1, Luo Lilin3, Zhang Yuqin2
- 1Department of Orthopedics, 3Department of Orthopedic Pathology, the First People’s Hospital of Yunnan Province, Kunming 650032, Yunnan Province, China; 2School of Materials Science and Engineering, Kunming University of Science and Technology, Kunming 650093, Yunnan Province, China
摘要:
文题释义:
羟基磷灰石基复合材料:羟基磷灰石具有良好的生物相容性、生物活性、骨传导性及可降解性,单一羟基磷灰石只有骨传导性,缺乏骨诱导性,将羟基磷灰石作为基体,加入活性物质制备出羟基磷灰石基复合材料,使其具备骨诱导性。
多孔材料:存在大量的孔隙结构,可以为成骨细胞提供增殖与长大所需的空间;有利于人体体液的流入,加速体液与材料间的离子交换,可以提高其降解速率;具有较大的比表面积,移植后能提高与人体体液和宿主骨组织的接触面积,加快成骨细胞的黏附及长入,提高其界面稳定性;存在通孔结构,有利于成骨细胞间的信息交流与爬行、微血管的长入及骨组织的长入。
背景:前期研究发现,在纳米羟基磷灰石中加入氧化锌并将其多孔化可明显提高磷灰石的形成能力,同时具有良好的生物相容性,但孔隙率的提高会导致力学性能的劣化。
目的:观察不同孔隙率下多孔氧化锌/羟基磷灰石复合材料微观结构、孔隙特征、力学性能、体外矿化与降解性能的变化,以及在适宜孔隙率下该复合材料的细胞相容性。
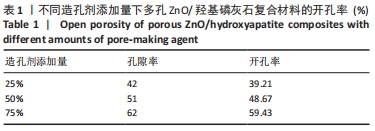
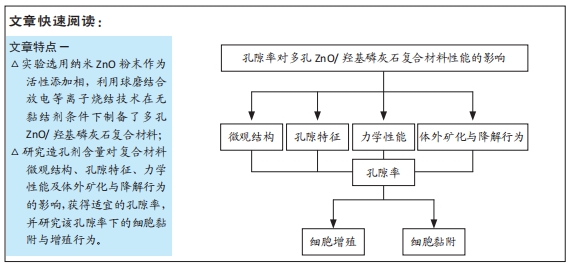
方法:通过改变造孔剂(医用级碳酸氢铵)添加量来控制复合材料的孔隙率,利用放电等离子烧结技术制备不同孔隙率(42%,51%,62%)的多孔氧化锌/羟基磷灰石复合材料,研究3种复合材料的微观结构、孔隙特征、力学性能、体外矿化与降解性能。将兔骨髓间充质干细胞接种于适宜孔隙率的多孔氧化锌/羟基磷灰石复合材料表面,观察细胞黏附和增殖情况。
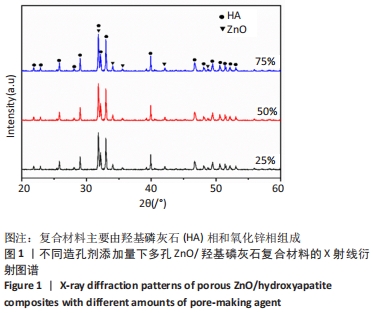
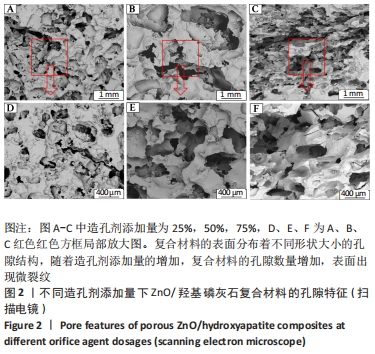
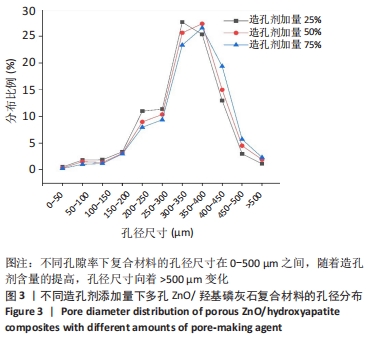
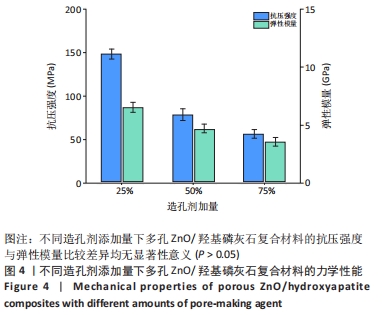
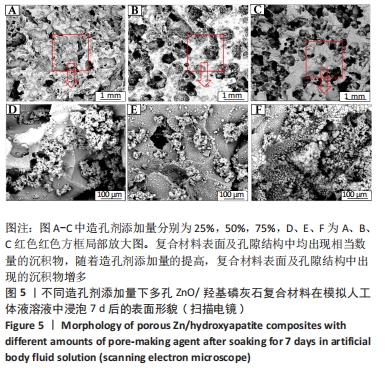
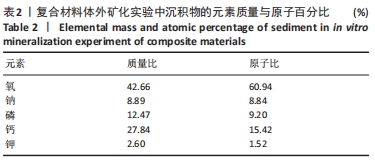
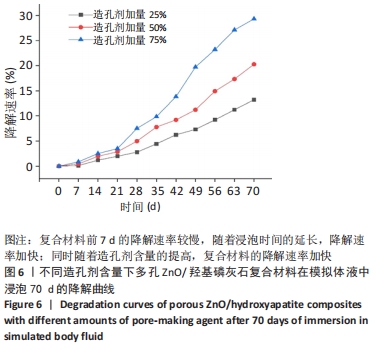
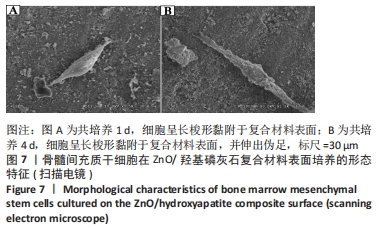
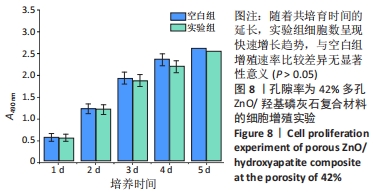
结果与结论:①扫描电镜显示,随着孔隙率的提高,复合材料的孔隙数量明显增加,通孔结构增加,表面也出现微裂纹,复合材料的孔径在0-500 μm之间;②随着孔隙率的提高,复合材料的抗压强度与弹性模量降低,抗压强度由148 MPa下降至56 MPa,弹性模量由6.5 GPa下降至3.5 GPa;③体外矿化与降解实验显示,随着孔隙率的提高,复合材料表面及孔隙结构中出现的类骨磷灰石沉积物增加,降解速率加快;④综合上述实验结果,选取孔隙率为42%的复合材料与兔骨髓间充质干细胞共培养,直接接触培养实验显示,细胞在复合材料表面与空隙内部生长黏附良好;复合材料浸提液CCK-8实验显示,随着培养时间的延长,兔骨髓间充质干细胞快速增殖;⑤结果表明,孔隙率为42%的多孔氧化锌/羟基磷灰石复合材料具有良好的力学性能、降解性能与生物相容性。
https://orcid.org/0000-0002-7539-613X (孟增东)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料; 口腔生物材料; 纳米材料; 缓释材料; 材料相容性;组织工程
中图分类号: