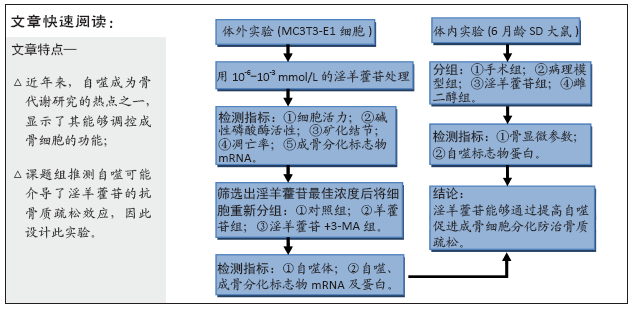
1.1 设计 细胞及动物对比观察实验,分为3个部分:①淫羊藿苷最佳浓度的筛选;②淫羊藿苷通过自噬促进成骨细胞分化;③动物实验。
1.2 时间及地点 实验于2019年7月至2020年3月在广州中医药大学岭南医学研究中心骨伤科重点实验室以及广州中医药大学实验动物中心完成。
1.3 材料
1.3.1 细胞株 小鼠前体成骨细胞株MC3T3-E1购自武汉
Procell,货号:CL-0378。
1.3.2 实验动物 6月龄SPF级雌性SD大鼠24只,体质量200-300 g,由广州中医药大学实验动物中心提供,实验动物质量合格证明编号:NO.44005800009602,实验动物许可证号编号:SCXK(粤)2018-0034,实验单位使用许可证编号:SYXK(粤)2018-0001。实验方案经广州中医药大学实验动物中心动物实验伦理委员会批准,批准号:20190225007。
1.3.3 药物 淫羊藿苷购于MACKLIN,货号:I811797,纯度≥
98%,20 mg/支。
1.3.4 主要实验仪器 细胞超净工作台(苏州安泰空气技术有限公司);移液器、冷冻离心机(Eppendorf,德国);倒置相差显微镜(Leica,德国);全自动酶标仪、细胞培养箱(Thermo
Fisher,美国);实时荧光定量PCR仪(Applied Biosystems Inc,美国);多功能激光扫描成像系统(Amersham,英国);凝胶成像系统(上海天能科技,中国);Micro-CT(Encho-MRI/LCT-200,美国)。
1.3.5 主要试剂 α-MEM培养基(Hyclone,美国);磷酸缓冲盐溶液(phosphate buffer saline,PBS)、胎牛血清、青链霉素、0.25%胰蛋白酶(Gibco,美国);β-甘油磷酸钠、抗坏血酸、地塞米松(Sigma,美国);碱性磷酸酶(alkaline phosphatase,
ALP)活性试剂盒(南京建成生物工程研究所,中国);ALP染色试剂盒(碧云天生物技术有限公司,中国);茜素红粉剂(阿拉丁试剂有限公司,上海);细胞计数试剂盒(cell counting kit-8,CCK8)、ANNEXIN V-FITC/PI凋亡试剂盒(索莱宝科技有限公司,北京);单丹磺酰戊二胺(Monodansylcadaverin,MDC)染色试剂盒(雷根生物技术有限公司,北京);3-甲基腺嘌呤(3-methyl adenine,3-MA,上海源叶生物,中国);戊酸雌二醇(拜尔医药保健有限公司,中国);细胞RNA快速提取试剂盒、两步法荧光定量反转录PCR试剂盒(Takara,日本)。
1.4 实验方法
1.4.1 淫羊藿苷最佳浓度的筛选 消化第3代MC3T3-E1细胞,将细胞分为对照组和淫羊藿苷不同浓度组(10-3,10-4,10-5,10-6 mmol/L),进行以下测试:
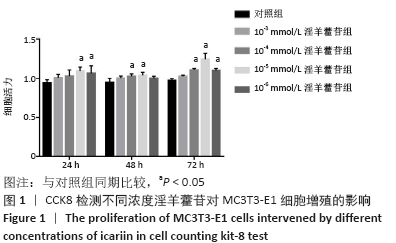
(1)CCK8检测细胞增殖:消化第3代细胞以3×103个/孔
的密度接种于96孔板,细胞分组同上,每组设置6个复孔;接种24 h待细胞贴壁后,弃去旧培养基,加入含淫羊藿苷的培养基,干预24,48,72 h后弃去培养基,每孔加入100 μL混匀好的CCK8溶液(将CCK8溶液与培养基按照1∶9的比例混匀),避光孵育2 h后用酶标仪在450 nm处测定吸光度(A)值,并计算细胞活力。
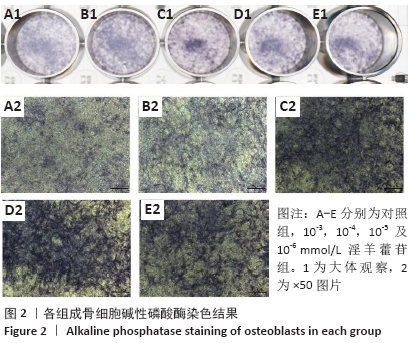
(2)ALP染色:消化第3代细胞,以3×104个/孔的密度接种于24孔板,细胞分组同上,每组4个复孔,在培养箱中培养24 h;24 h弃去培养基,加入含淫羊藿苷或不含淫羊藿苷的新鲜成骨诱导培养基(10 mmol/L的β-甘油磷酸钠、50 μmol/L抗坏血酸、10-8 mol/L地塞米松),每2 d换液1次;培养7 d后按试剂盒步骤进行染色,扫描并显微镜拍照。
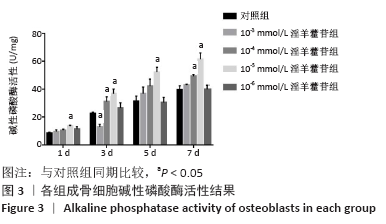
(3)ALP活性检测:消化第3代细胞,以5×104个/孔的密度接种于24孔板,细胞分组以及培养方法同“CCK8检测细胞增殖”,于干预1,3,5,7 d后弃去培养液,用裂解液裂解细胞后按照ALP活性试剂盒的说明进行操作,计算金氏单位(U/mg)用以反映ALP活性。
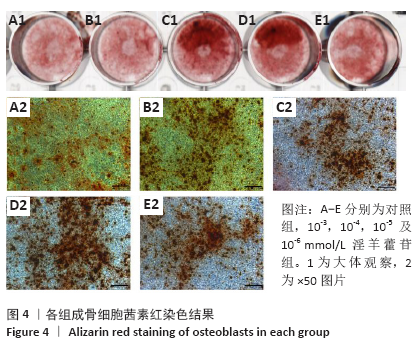
(4)茜素红染色:消化第3代细胞,以1×104个/孔的密度接种于24孔板,细胞分组以及培养方法同“CCK8检测细胞增殖”,培养21 d后弃去培养液,用PBS清洗3遍,每次5 min,使用40 g/L的多聚甲醛固定30 min后弃去多聚甲醛,PBS清洗3遍,每孔加入300 μL(覆盖细胞)茜素红染色液,室温下染色10 min,PBS清洗3遍,扫描以及显微镜拍照。
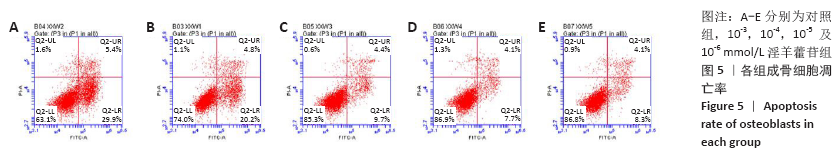
(5)ANNEXIN V-FITC/PI凋亡检测:消化第3代细胞,以1×104个/孔的密度接种于24孔板,细胞分组以及培养方法同“CCK8检测细胞增殖”,干预48 h后,按照试剂盒说明进行操作。
(6)实时荧光定量聚合酶链反应(RT-qPCR)检测:取第4代细胞,调整细胞密度至3×104个/cm2,每孔0.5 mL接种于6孔板中,补齐培养基至2 mL,然后置于37 ℃,体积分数5%CO2的培养箱中培养,细胞分组以及培养方法同上;
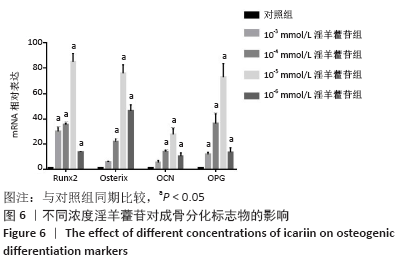
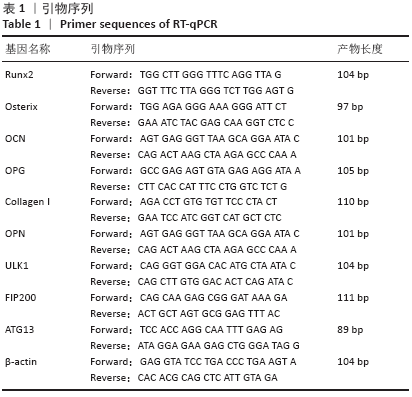
24 h后弃培养基,加入不同浓度的淫羊藿苷直至2 mL/孔,培养7 d,弃去培养液,用RNA提取试剂盒提取总RNA,紫外分光光度计测定RNA纯度,每组取1.0 μg总RNA,分别加入反转录试剂盒的反应体系,在反转录仪中进行反转录生成cDNA后,采用RT-qPCR测定Runx2、Osterix、OCN、OPG的表达情况,采用2-∆∆Ct法并以β-actin为内参计算上述指标的相对表达量,用于统计学分析,引物序列见表1。
1.4.2 淫羊藿苷通过自噬促进成骨细胞分化的研究 消化第4代MC3T3-E1细胞,将细胞分为3组:对照组、淫羊藿苷组、淫羊藿苷+3-MA组,后2组用前面实验得出的最佳浓度淫羊藿苷处理细胞,淫羊藿苷+3-MA组在此基础上加10 mmol/L自噬抑制剂3-MA ,进行以下测试:
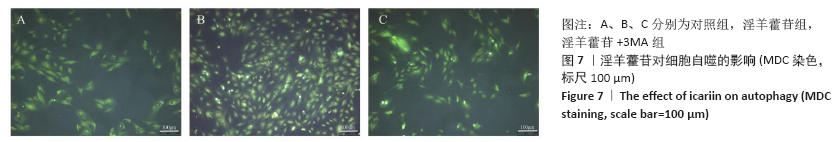
(1)MDC染色:消化第4代细胞,以3×103个/孔的密度接种于96孔板,细胞同上分3组,每组6个复孔,待细胞贴壁后弃去培养基,加入含药或不含药的新鲜成骨诱导培养基,培养48 h;按照MDC Stain(×500):Stain buffer=1∶499的比例配制成MDC染色工作液,每孔加入100 μL的MDC染色工作液,37 ℃,体积分数5%CO2避光孵育60 min,弃去工作液,加入Wash buffer清洗3遍,荧光显微镜下观察(激发滤光片波长355 nm,阻断滤光片波长512 nm)。
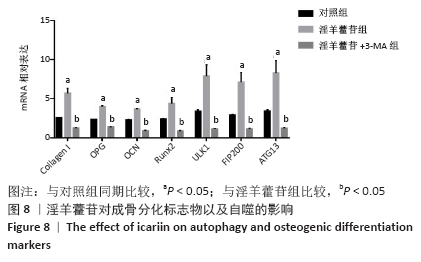
(2)RT-qPCR:细胞分组以及培养方法同“MDC染色”,余步骤同“1.4.1中(6)”,检测指标为Runx2、OCN、Collagen I、OPN、ULK1、FIP200、ATG13,引物序列见表1。
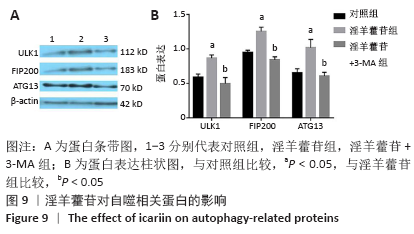
(3)免疫印迹(Western-Blotting):收集第4代细胞,制成细胞浓度为1×108 L-1的细胞混悬液,加2 mL到6孔板中,细胞分组以及培养方法同“MDC染色”,置37 ℃,体积分数5%CO2培养过夜,7 d后分别提取各组细胞总蛋白,
12 000 r/min离心15 min,取上清100 μL,蛋白定量,配制样品,通过上样、电泳、转膜、封闭、孵育一抗二抗后显影,测出相应灰度值进行分析。
1.4.3 动物实验
(1)动物分组方法:SD大鼠24只分为4组,假手术组、病理模型组、淫羊藿苷组、戊酸雌二醇组,每组6只。打开Excel,利用升序排序,首先将所有SD大鼠按体质量由小到大编号,利用Excel生成24个两位整数的随机数,将所得的两位随机数除以4,余数为0放在假手术组,余数为1的放在病理模型组,余数为2的放在淫羊藿苷组,余数为3的放在戊酸雌二醇组,如果余数为0的那一组动物数已经达到6只,则将下次余数为0的动物分配至第二组,其他同理,按照这种分组方法,一般情况下,得到的各组动物在体质量方面均无差异。
(2)造模及给药:采取双侧卵巢切除术构建动物模型,具体步骤同前期研究[15];术后连续3 d肌注青霉素钠,然后开始给药进行干预;淫羊藿苷溶解在0.5%的羧甲基纤维素钠中,戊酸雌二醇以生理盐水直接溶解;淫羊藿苷以
200 mg/(kg·d)的剂量进行灌胃,戊酸雌二醇以0.1 mg/(kg·d)剂量灌胃,假手术组和病理模型组予以等量生理盐水灌胃,疗程为12周。

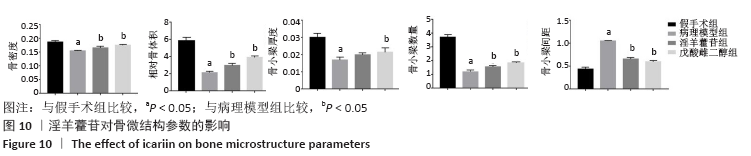
(3)Micro-CT检测:药物干预12周后,麻醉后处死所有大鼠,取大鼠右侧股骨置于40 g/L的多聚甲醛中固定2 d后更换为体积分数75%的乙醇浸泡,在扫描前1 d更换为生理盐水浸泡。扫描时,将股骨放在Micro-CT线圈中,从股骨远端开始进行CT螺旋扫描,每18 μm作为一个断层,将所有标本以股骨远端生长板顶点往上除去50张,再开始往上取100张去掉皮质为兴趣区域,自带软件分别测定骨密度、骨小梁数量(trabecular number,Tb.N)、骨小梁厚度(trabecular thickness,Tb.Th)、相对骨体积(bone volume/tissue volume,BV/TV)、骨小梁间距(trabecular separation,Tb.Sp)等指标。
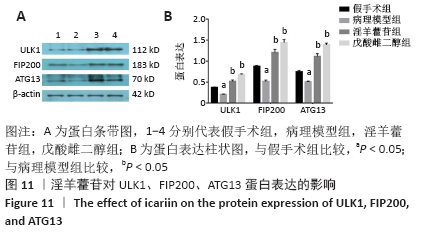
(4)Western-Blotting:取大鼠的左侧股骨进行检测,余步骤同“1.4.2中(3)”。
1.5 主要观察指标 ①细胞活力;②ALP活性;③茜素红染色结果;④凋亡率;⑤MDC染色结果;⑥成骨分化及自噬相关基因、蛋白的表达;⑦骨骼显微参数。
1.6 统计学分析 采用SPSS 19.0软件进行统计学分析,计量数据用x±s表示,若数据呈正态分布且方差齐,采用单因素方差分析,进一步多重比较采用LSD法,P < 0.05为差异有显著性意义。