1.1 设计 体外观察性实验。
1.2 时间及地点 实验于2016年9月至2019年6月在南方医科大学口腔医院实验室完成。
1.3 材料 壳聚糖(脱乙酰度≥95%,上海麦克林生化科技有限公司);β-磷酸三钙(生物医用级,β相磷酸三钙≥98%,粒径< 0.1 μm,上海阿拉丁生化科技股份有限公司);京尼平(纯度>98%,大连美仑生物技术有限公司);β-甘油磷酸钠(纯度≥99.0%,美国Sigma公司);无水乙醇(广州化学试剂厂);盐酸(广州化学试剂厂);电热恒温水浴锅(HWS-12,上海一恒科学仪器有限公司);生化培养箱
(SPX-1508-Z,上海博迅实业有限公司医疗设备厂);精密电子天平(MS603S,上海天能科技有限公司);磁力搅拌机(JB-2,上海雷磁新径仪器有限公司);二氧化碳培养孵育箱(德国GMBH公司);光学显微镜(日本OLYMPUS公司);倒置显微镜及照相系统(IX51,日本OLYMPUS公司);超净工作台(苏州净化设备有限公司);移液枪(德国Eppendorf公司);细胞培养皿(美国Corning公司);CellTiter-Lumi™发光法细胞活力检测试剂盒(碧云天);DMEM培养基、胎牛血清、双抗、胰酶(美国Sigma公司);OriCell 人牙髓干细胞成骨诱导分化培养基试剂盒(美国Cyagen Biosciences公司)。
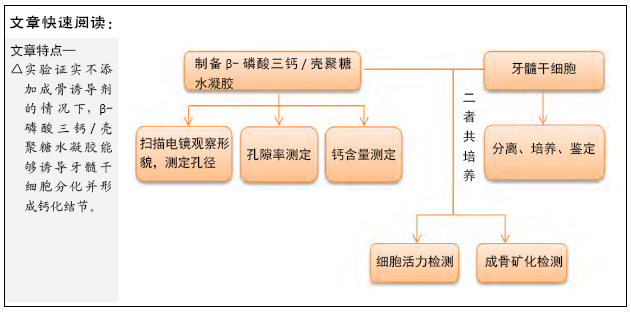
1.4 方法
1.4.1 水凝胶的制备 称取适量壳聚糖粉末溶解于配置好的0.1 mol/L盐酸溶液;称取适量β-甘油磷酸钠溶于超纯水中;称取适量京尼平溶于超纯水中。称取适量β-磷酸三钙溶于2%壳聚糖溶液中,使其与壳聚糖溶液的质量体积比分别为0.5%,1%及2%,逐滴加入β-甘油磷酸钠溶液,直到pH值达到中性,搅拌均匀后逐滴加入京尼平溶液,待气泡排除后将水凝胶接入离心管、6孔板、96孔板中,37 ℃生化培养箱交联24 h。以上操作皆在无菌条件、4 ℃冰水浴下进行。
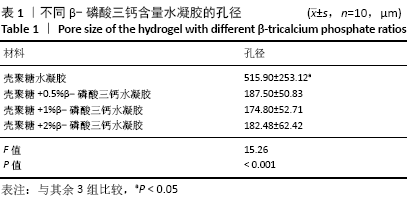
1.4.2 电镜观察 将各组水凝胶冻干后裁剪为1 cm×1 cm× 0.3 cm的相等大小立方体,使用扫描电子显微镜观察断面的内部结构和形貌,选取10个随机区域以平均值计算孔径大小。
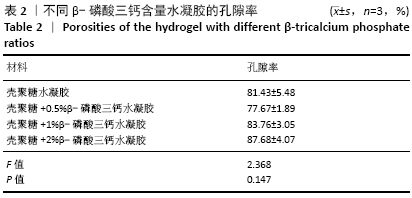
1.4.3 孔隙率测定 在恒温恒压的条件下,首先选取适当大小的称量瓶,倒入适量乙醇,将大小已剪裁好的一定体积的待测支架材料(干质量为m0),浸入容量瓶中直至完全浸透,称取称量瓶质量记为ma,将已经浸透的湿支架取出,称得称量瓶的质量为mb。选取50 mL的比重瓶,装满乙醇溶液至刻度后称质量,记为m1,将已经浸透乙醇的湿支架材料放入容量瓶,继续加入乙醇至比重瓶规定刻度,称质量记为m2。
根据以下公式计算孔隙率:
v1=(ma-mb-m0)/ρ
v2=[(ma-mb)- (m2-m1)] /ρ
ε=[v1/v2]×100%=(ma-mb-m0)/(ma-mb)-(m2-m1)×100%
其中v1为样品支架孔体积,v2为样品支架表观体积,ε为样品支架孔隙率,ρ为乙醇密度,将相同支架重复测定3次,取平均值。使用Original pro软件观察。
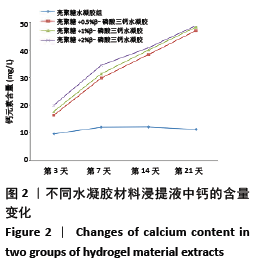
1.4.4 水凝胶浸提液中钙浓度检测 制备好的水凝胶成胶后放于6孔板中,每孔添加1 mL DMEM培养基,放入37 ℃,体积分数为5%CO2生化培养箱中孵育。收集第3,7,14,21天的培养基,使用电感耦合等离子体发射光谱法进行水凝胶浸提液中钙浓度检测。
1.4.5 水凝胶材料的生物相容性及成骨性能
(1)人牙髓干细胞的获取和培养:于南方医科大学口腔医院口腔颌面外科门诊收集16-25岁健康青年的正常无龋恒牙,需无明显龋损、无牙髓炎、无根尖周炎。该研究经南方医科大学口腔医院伦理委员会批准并取得患者知情同意。将恒牙沿牙颈部磨沟,沿沟槽劈开恒磨牙,暴露内部的牙髓组织,组织镊小心夹取牙髓组织,组织剪剪碎牙髓组织,离心后弃去上清,加入新鲜DMEM培养基反复吹打直至组织分散均匀,吸取适量混悬液滴入6孔板中央,盖玻片压紧。待见到细胞自盖玻片下爬出后将盖玻片翻开,换液,继续培养至长满6孔板,利用胰酶消化分离得到人牙髓干细胞,接种于25 cm3培养瓶中,添加DMEM培养基,在37 ℃,体积分数为5%CO2饱和湿度的条件下静置培养,待牙髓干细胞长至80%融合成片时进行传代。

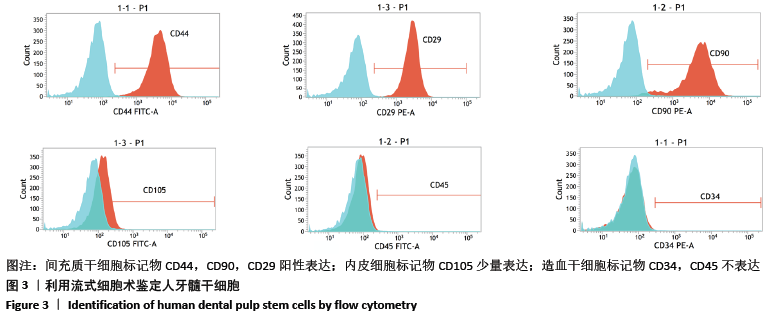
(2)流式细胞术鉴定人牙髓干细胞:选取CD90、CD29和CD44作为间充质干细胞的标志;选取CD105作为内皮细胞的标志;选取CD34、CD45作为造血干细胞的标志。胰蛋白酶消化获得第3代人牙髓干细胞的单细胞悬浮液,使用荧光染料缀合表面标志物:CD29/PE,CD34/PE,CD90/PE,CD44/FITC,CD45/PE,CD105/FITC,40 g/L多聚甲醛固定细胞,FACS缓冲液(PBS+1%BSA+0.1%NaN3)染色和洗涤细胞后,用Guava®easyCyte8HT台式流式细胞仪进行分析。
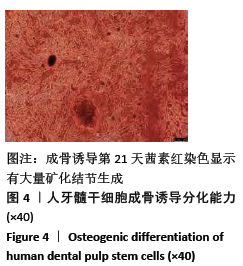
(3)人牙髓干细胞的成骨诱导:第3代牙髓干细胞培养至融合度达到80%-90%时,用0.25%Trypsin-0.04%EDTA进行消化,按照2×104/cm2的细胞密度接种在事先包被0.1%明胶的6孔板中,每孔加入2 mL完全培养基,置于37 ℃,体积分数为5% CO2培养箱中进行培养。当细胞融合度达到60%-70%时,小心吸弃孔内完全培养基,加入2 mL OriCell 人牙髓干细胞成骨诱导分化完全培养基,每隔3 d换液1次,诱导21 d后进行茜素红染色,操作如下:吸弃6孔板中的成骨诱导分化完全培养基,用1×PBS冲洗一两次,每孔加入
2 mL 体积分数4%中性甲醛溶液固定30 min,1×PBS冲洗2次,每孔加入1 mL茜素红染液染3-5 min,1×PBS冲洗两三次,将培养板置于显微镜下观察成骨染色效果。
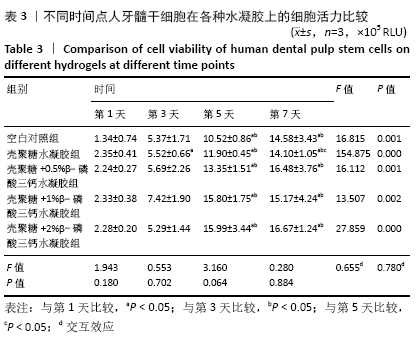
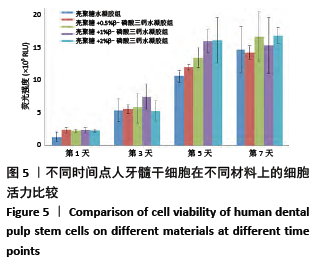
(4)细胞活力检测:利用CellTiter-Lumi™发光法细胞活力检测试剂盒检测第1,3,5,7天的细胞活力,操作如下: 取出细胞培养板在室温平衡10 min(通常不宜超过30 min),96孔板每孔加入100 μL CellTiter-Lumi™发光法检测试剂,室温振荡2 min,以促进细胞的裂解;室温(约25 ℃)孵育10 min,使发光信号趋于稳定;使用多功能酶标仪进行化学发光检测,根据化学发光读数直接计算细胞的相对活力。
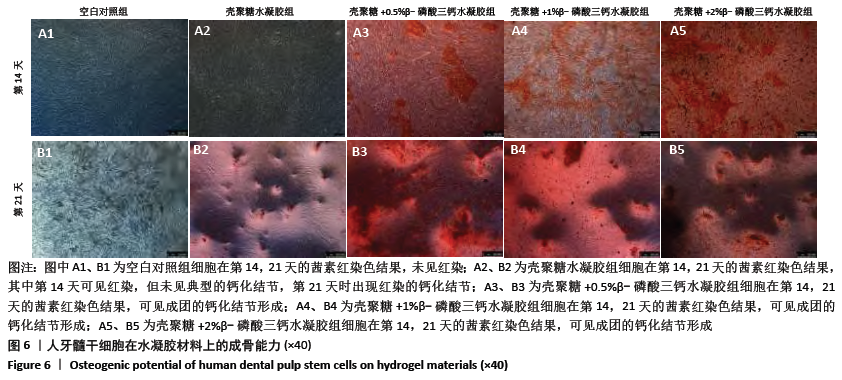
(5)人牙髓干细胞在水凝胶材料上的钙化结节观察:在铺好水凝胶材料的6孔板中调整细胞密度为1×105,第14天和第21天进行茜素红染色,光镜下观察染色情况。
1.5 主要观察指标 ①水凝胶的形态及孔径;②水凝胶孔隙率;③水凝胶材料浸提液中的钙含量;④牙髓干细胞在水凝胶上的生长以及钙化结节生成情况。
1.6 统计学分析 采用SPSS 19.0统计分析软件。数据以x±s表示,进行析因方差分析。每一时间段的组间比较,先用Levene检验方差齐性,其中方差齐性进行One-Way ANOVA分析,同时采用S-N-K组间两两多重比较;若方差不齐采用Welch稳健方差分析,并采用Dunnett’s T3进行组间两两多重比较。为探讨时间和组别对细胞增殖性的协同作用,进行单因素重复测量的方差分析。假设检验为双侧检验,检验水准为P=0.05,以P < 0.05为差异有显著性意义。