中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (1): 26-31.doi: 10.3969/j.issn.2095-4344.2128
• 骨髓干细胞 bone marrow stem cells • 上一篇 下一篇
脱钙骨基质体外诱导骨髓间充质干细胞的成骨分化
陈俊毅,王 宁,陈西淼,朱伦井,段江涛,张贤平,贝朝涌
- 桂林医学院附属医院四肢创伤骨科,广西壮族自治区桂林市 541001
Osteogenic differentiation of bone marrow mesenchymal stem cells induced by demineralized bone matrix in vitro
Chen Junyi, Wang Ning, Chen Ximiao, Zhu Lunjing, Duan Jiangtao, Zhang Xianping, Bei Chaoyong
- Department of Limb Trauma, Affiliated Hospital of Guilin Medical University, Guilin 541001, Guangxi Zhuang Autonomous Region, China
摘要:
文题释义:
脱钙骨基质:是骨组织工程中理想的支架材料。理论上脱钙骨基质的成骨特性是其在去抗原后分泌骨形态发生蛋白2等生长因子,这些因子能够促进骨形成及骨组织矿化,加速愈合。
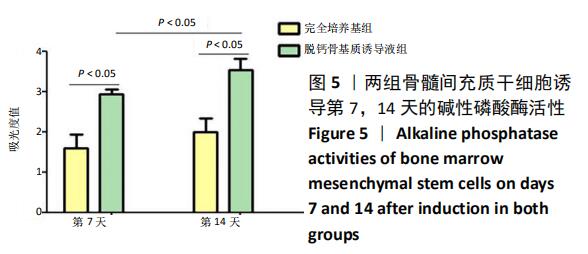
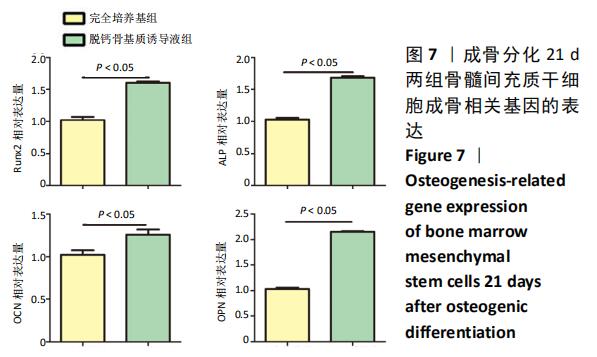
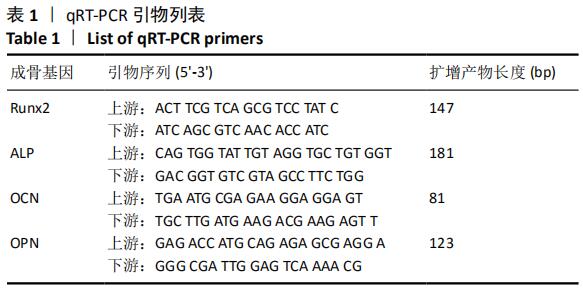
成骨分化:成骨分化过程中碱性磷酸酶活性升高,钙结节的形成和成骨相关因子ALP、RUNX2、OCN等表达增加等能从定性、定量方面确定成骨情况。
背景:脱钙骨基质脱钙去抗原处理后含有骨形态发生蛋白2等多种活性因子,在特定的关节微环境条件下这些活性因子能促进骨髓间充质干细胞转化为软骨细胞,并能促进其增殖。
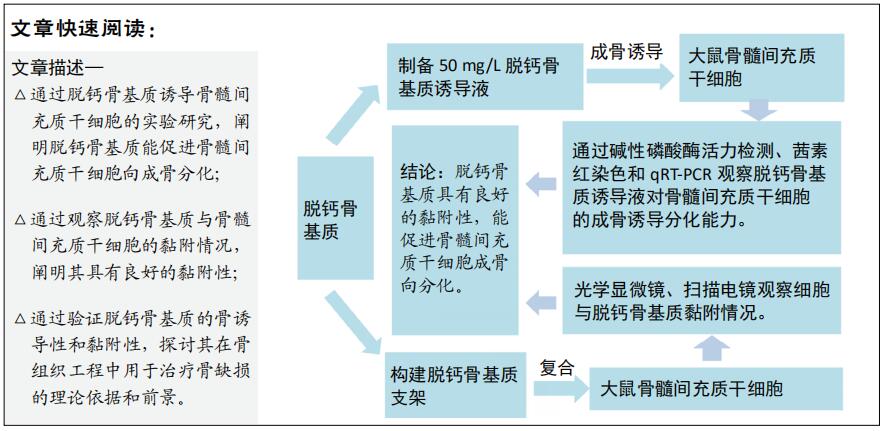
目的:探索脱钙骨基质诱导骨髓间充质干细胞成骨分化及其作为细胞载体支架治疗骨缺损的研究价值。
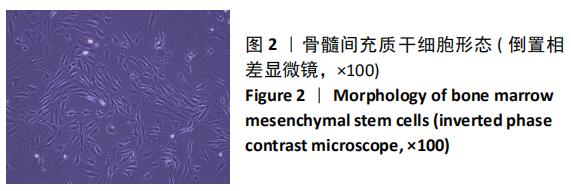
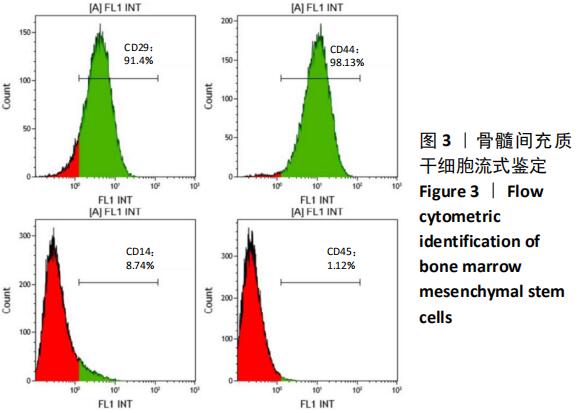
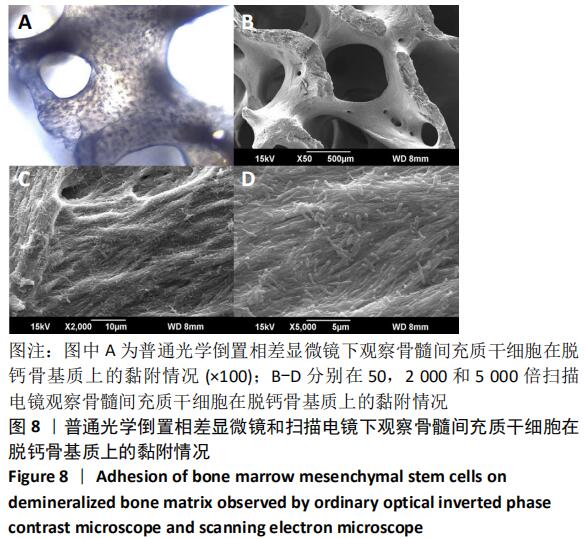
方法:用全骨髓分离贴壁法提取大鼠股骨骨髓间充质干细胞,选取第3代骨髓间充质干细胞,添加完全培养基和50 mg/L脱钙骨基质诱导液培养,采用CCK-8方法检测骨髓间充质干细胞的增殖活性;诱导培养7,14 d后采用酶标法定量检测碱性磷酸酶活性;诱导培养21 d后茜素红染色观察钙结节形成情况;诱导培养21 d后采用qRT-PCR检测成骨相关因子的表达。脱钙骨基质与骨髓间充质干细胞复合培养21 d采用普通光学倒置相差显微镜和扫描电镜观察两者的黏附情况。
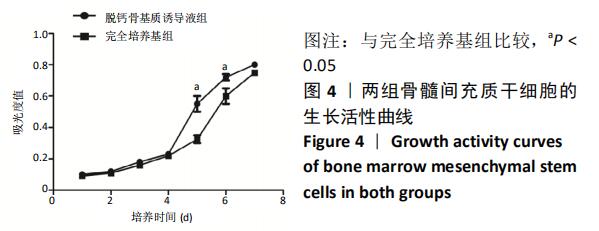
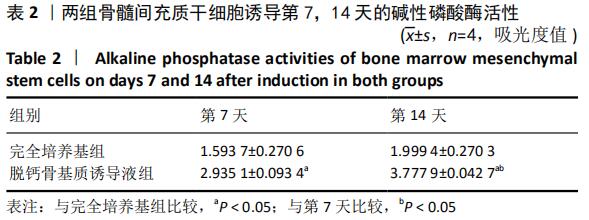
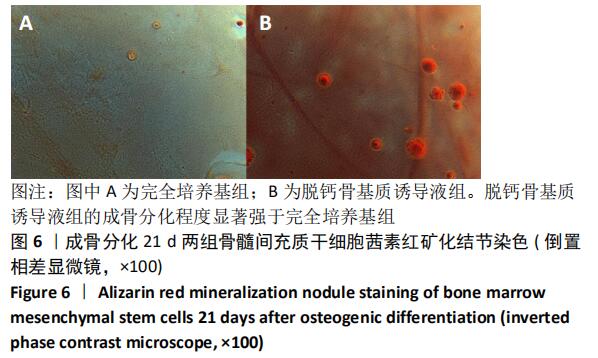
结果与结论:①脱钙骨基质诱导液组第5,6天的细胞数量高于完全培养基组(P < 0.05);②脱钙骨基质诱导液组诱导分化7,14 d的细胞碱性磷酸酶活性明显高于完全培养基组(P < 0.05);③脱钙骨基质诱导液组形成钙结节明显多于完全培养基组;④脱钙骨基质诱导液组成骨因子RUNX2、ALP、OCN和OPN表达明显高于完全培养基组(P < 0.05);⑤骨髓间充质干细胞在脱钙骨基质上贴附情况良好,分布在支架空隙间,互相爬行;⑥结果表明,脱钙骨基质可正向诱导骨髓间充质干细胞成骨分化,黏附性良好,为组织工程复合材料的研究提供理论参考。
中图分类号: