中国组织工程研究 ›› 2016, Vol. 20 ›› Issue (49): 7327-7333.doi: 10.3969/j.issn.2095-4344.2016.49.005
• 脑及脊髓损伤动物模型 Animal models of brain and spinal cord injuries • 上一篇 下一篇
银杏平颤方对帕金森病模型小鼠多巴胺神经元丢失及其凋亡的影响
吴亚丹,梁培日,龙登毅,高炳淼
- 海南省老年病医院神经内科,海南省海口市 571100
Effects of Ginkgo biloba Pingchan Recipe on loss and apoptosis of dopamine neurons in mouse models of Parkinson’s disease
Wu Ya-dan, Liang Pei-ri, Long Deng-yi, Gao Bing-miao
- Department of Neurology, Geriatrics Hospital of Hainan Province, Haikou 571100, Hainan Province, China
摘要:
文章快速阅读:
.jpg) 文题释义:
特发性帕金森病:病因迄今未明,以中枢神经系统不同部位变性为主,尚有其他临床特点,某些中枢神经系统变性疾病伴Parkinson病症状,故可称之为症状性Parkinson病。如进行性核上性麻痹、纹状体黑质变性、Shy-Drager综合征及橄榄脑桥小脑萎缩(OPCA)等。还有一些疾病或因素可以产生类似帕金森病的临床症状,其病因为感染、应用多巴胺受体阻滞药等、毒物作用、血管性(多发性脑梗死)及脑外伤等所致,临床上称为帕金森综合征。
多巴胺:C6H3(OH)2-CH2-CH2-NH2,由脑内分泌,可影响一个人的情绪。它正式的化学名称为4-(2-氨基乙基)-1,2-苯二酚(4-(2-aminoethyl)benzene-1,2-diol)。Arvid Carlsson确定多巴胺为脑内信息传递者的角色使他赢得了2000年诺贝尔医学奖。多巴胺是一种神经传导物质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌主要负责大脑的情欲,感觉将兴奋及开心的信息传递,也与上瘾有关。
文题释义:
特发性帕金森病:病因迄今未明,以中枢神经系统不同部位变性为主,尚有其他临床特点,某些中枢神经系统变性疾病伴Parkinson病症状,故可称之为症状性Parkinson病。如进行性核上性麻痹、纹状体黑质变性、Shy-Drager综合征及橄榄脑桥小脑萎缩(OPCA)等。还有一些疾病或因素可以产生类似帕金森病的临床症状,其病因为感染、应用多巴胺受体阻滞药等、毒物作用、血管性(多发性脑梗死)及脑外伤等所致,临床上称为帕金森综合征。
多巴胺:C6H3(OH)2-CH2-CH2-NH2,由脑内分泌,可影响一个人的情绪。它正式的化学名称为4-(2-氨基乙基)-1,2-苯二酚(4-(2-aminoethyl)benzene-1,2-diol)。Arvid Carlsson确定多巴胺为脑内信息传递者的角色使他赢得了2000年诺贝尔医学奖。多巴胺是一种神经传导物质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌主要负责大脑的情欲,感觉将兴奋及开心的信息传递,也与上瘾有关。
.jpg) 文题释义:
特发性帕金森病:病因迄今未明,以中枢神经系统不同部位变性为主,尚有其他临床特点,某些中枢神经系统变性疾病伴Parkinson病症状,故可称之为症状性Parkinson病。如进行性核上性麻痹、纹状体黑质变性、Shy-Drager综合征及橄榄脑桥小脑萎缩(OPCA)等。还有一些疾病或因素可以产生类似帕金森病的临床症状,其病因为感染、应用多巴胺受体阻滞药等、毒物作用、血管性(多发性脑梗死)及脑外伤等所致,临床上称为帕金森综合征。
多巴胺:C6H3(OH)2-CH2-CH2-NH2,由脑内分泌,可影响一个人的情绪。它正式的化学名称为4-(2-氨基乙基)-1,2-苯二酚(4-(2-aminoethyl)benzene-1,2-diol)。Arvid Carlsson确定多巴胺为脑内信息传递者的角色使他赢得了2000年诺贝尔医学奖。多巴胺是一种神经传导物质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌主要负责大脑的情欲,感觉将兴奋及开心的信息传递,也与上瘾有关。
文题释义:
特发性帕金森病:病因迄今未明,以中枢神经系统不同部位变性为主,尚有其他临床特点,某些中枢神经系统变性疾病伴Parkinson病症状,故可称之为症状性Parkinson病。如进行性核上性麻痹、纹状体黑质变性、Shy-Drager综合征及橄榄脑桥小脑萎缩(OPCA)等。还有一些疾病或因素可以产生类似帕金森病的临床症状,其病因为感染、应用多巴胺受体阻滞药等、毒物作用、血管性(多发性脑梗死)及脑外伤等所致,临床上称为帕金森综合征。
多巴胺:C6H3(OH)2-CH2-CH2-NH2,由脑内分泌,可影响一个人的情绪。它正式的化学名称为4-(2-氨基乙基)-1,2-苯二酚(4-(2-aminoethyl)benzene-1,2-diol)。Arvid Carlsson确定多巴胺为脑内信息传递者的角色使他赢得了2000年诺贝尔医学奖。多巴胺是一种神经传导物质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌主要负责大脑的情欲,感觉将兴奋及开心的信息传递,也与上瘾有关。摘要
背景:现代药理研究证明银杏叶及其提取物生物具有抗氧化作用以及刺激神经生长因子产生等保护多巴胺神经元的存活,减少其凋亡。
目的:验证银杏平颤方对帕金森病小鼠多巴胺神经元丢失及其凋亡的影响以及的神经母细胞瘤衍生细胞株SH-SY5Y的增殖情况的影响。
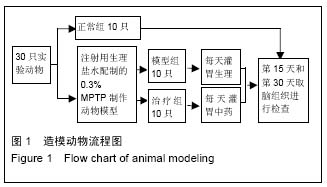
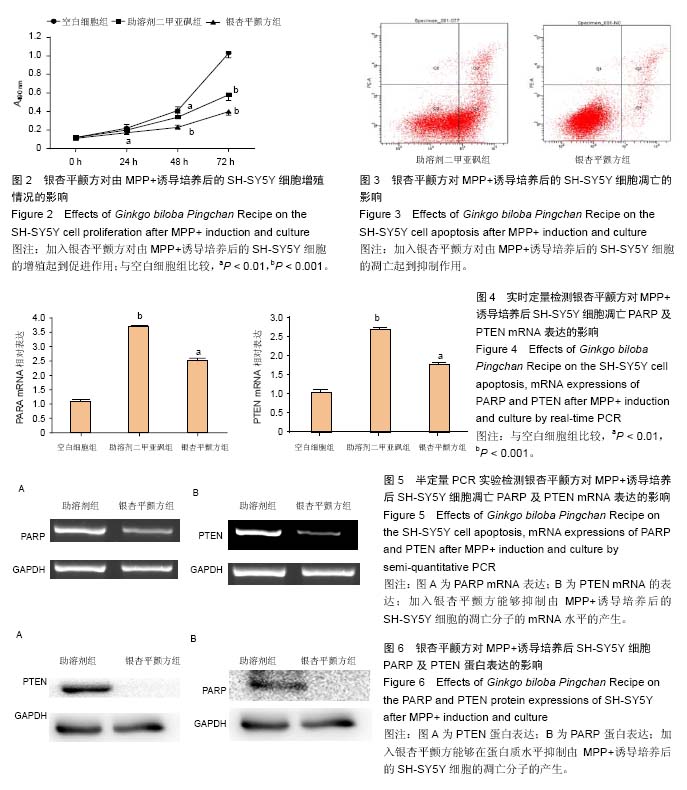
方法:①C57BL小鼠随机分成3组。正常组10只不处理。其他2组小鼠每天腹腔注射MPTP建立小鼠帕金森病的模型,连续6周;每次腹腔注射前30 min进行灌胃处理,模型组10只灌胃生理盐水;治疗组10只灌胃中药银杏平颤方。分别在造模开始后的第15天和第30天取脑组织,免疫组织化学观察中脑黑质多巴胺神经元丢失和细胞凋亡情况;②体外培养神经母细胞瘤衍生细胞株SH-SY5Y并用银杏平颤方处理细胞,MTT 法检测人SH-SY5Y的增殖,流式细胞术检测细胞凋亡情况;Real-time PCR 和Western blotting检测细胞PARP、PTEN mRNA和蛋白质表达。
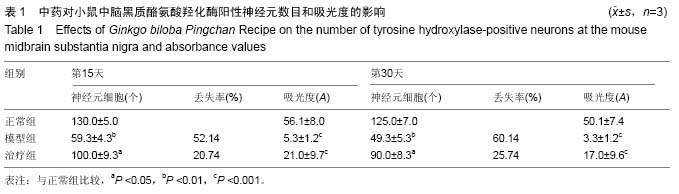
结果与结论:①动物实验结果:正常组小鼠的中脑黑质致密部酪氨酸羟化酶阳性神经元的数目多于模型组,并存在时间依赖关系;银杏平颤方中药治疗组小鼠中脑黑质致密部酪氨酸羟化酶阳性神经元的数目多于模型组(P < 0.05);②体外细胞实验结果:银杏平颤方处理的细胞凋亡率低于模型组;银杏平颤方处理细胞的PARP、PTEN的mRNA及蛋白水平均低于模型组。③结果说明,银杏平颤方治疗可在一定程度上抑制中脑神经元细胞的凋亡;其分子机制可能是银杏平颤方通过抑制PTEN表达进而降低细胞凋亡水平,保护多巴胺神经元,阻止其丢失,起到防治帕金森病的作用。
中国组织工程研究杂志出版内容重点:肾移植;肝移植;移植;心脏移植;组织移植;皮肤移植;皮瓣移植;血管移植;器官移植;组织工程
ORCID: 0000-0002-4661-3908(吴亚丹)
中图分类号:
.jpg) 文题释义:
特发性帕金森病:病因迄今未明,以中枢神经系统不同部位变性为主,尚有其他临床特点,某些中枢神经系统变性疾病伴Parkinson病症状,故可称之为症状性Parkinson病。如进行性核上性麻痹、纹状体黑质变性、Shy-Drager综合征及橄榄脑桥小脑萎缩(OPCA)等。还有一些疾病或因素可以产生类似帕金森病的临床症状,其病因为感染、应用多巴胺受体阻滞药等、毒物作用、血管性(多发性脑梗死)及脑外伤等所致,临床上称为帕金森综合征。
多巴胺:C6H3(OH)2-CH2-CH2-NH2,由脑内分泌,可影响一个人的情绪。它正式的化学名称为4-(2-氨基乙基)-1,2-苯二酚(4-(2-aminoethyl)benzene-1,2-diol)。Arvid Carlsson确定多巴胺为脑内信息传递者的角色使他赢得了2000年诺贝尔医学奖。多巴胺是一种神经传导物质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌主要负责大脑的情欲,感觉将兴奋及开心的信息传递,也与上瘾有关。
文题释义:
特发性帕金森病:病因迄今未明,以中枢神经系统不同部位变性为主,尚有其他临床特点,某些中枢神经系统变性疾病伴Parkinson病症状,故可称之为症状性Parkinson病。如进行性核上性麻痹、纹状体黑质变性、Shy-Drager综合征及橄榄脑桥小脑萎缩(OPCA)等。还有一些疾病或因素可以产生类似帕金森病的临床症状,其病因为感染、应用多巴胺受体阻滞药等、毒物作用、血管性(多发性脑梗死)及脑外伤等所致,临床上称为帕金森综合征。
多巴胺:C6H3(OH)2-CH2-CH2-NH2,由脑内分泌,可影响一个人的情绪。它正式的化学名称为4-(2-氨基乙基)-1,2-苯二酚(4-(2-aminoethyl)benzene-1,2-diol)。Arvid Carlsson确定多巴胺为脑内信息传递者的角色使他赢得了2000年诺贝尔医学奖。多巴胺是一种神经传导物质,用来帮助细胞传送脉冲的化学物质。这种脑内分泌主要负责大脑的情欲,感觉将兴奋及开心的信息传递,也与上瘾有关。