中国组织工程研究 ›› 2014, Vol. 18 ›› Issue (25): 4038-4042.doi: 10.3969/j.issn.2095-4344.2014.25.018
• 生物材料基础实验 basic experiments of biomaterials • 上一篇 下一篇
芍药苷对白色念珠菌生物膜的作用
王殿明1,王健平1,杨景云2,张慧明2,刘淑红3
- 1佳木斯大学附属口腔医院,黑龙江省佳木斯市 154003;2佳木斯大学基础医学院,黑龙江省佳木斯市 154007;3黑龙江省林业卫生学校,黑龙江省佳木斯市 154007
Paeoniflorin effects on Candida albicans biofilms
Wang Dian-ming1, Wang Jian-ping1, Yang Jing-yun2, Zhang Hui-ming2, Liu Shu-hong3
- 1The Affiliated Stomatological Hospital of Jiamusi University, Jiamusi 154003, Heilongjiang Province, China; 2School of Basic Medical Sciences, Jiamusi University, Jiamusi 154007, Heilongjiang Province, China; 3Heilongjiang Province Forestry Health School, Jiamusi 154007, Heilongjiang Province, China
摘要:
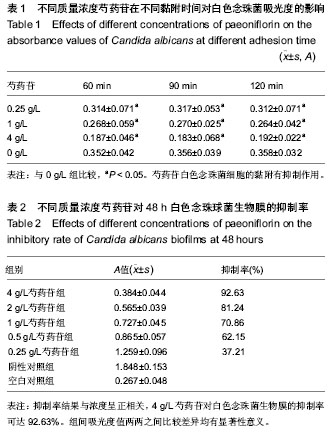
背景:研究证实中药赤芍有效成分对白色念珠菌有较好的抑制作用,但其单体芍药苷对白色念珠菌生物膜是否有抑制作用未见报道。 目的:观察芍药苷对体外白色念珠菌生物膜的影响。 方法:用RPMI-1640分别按2倍稀释法制备5个浓度梯度(4,2,1,0.5,0.25 g/L)的芍药苷溶液。用RPMI-1640稀释洗必泰为5个浓度梯度(2%,1%,0.5%,0.25%,0.125%)。采用琼脂扩散法检测不同浓度梯度芍药苷或洗必泰对白色念珠菌的抑菌直径。MTT法检测不同浓度洗必泰或芍药苷对白色念珠菌细胞黏附的作用,以及对白色念珠菌生物膜的抑制作用,并且利用激光共聚焦扫描显微镜和死菌活菌荧光染色技术相结合方法观察常态及药物作用下的白色念珠菌生物膜。 结果与结论:洗必泰与芍药苷均有抑菌能力,抑菌环直径与药物浓度呈正相关;除2 g/L芍药苷组与1%,2%洗必泰组抑菌环直径无差异外,其余组间两两比较差异均有显著性意义。不同质量浓度芍药苷对白色念珠菌的细胞黏附都具有抑制作用,对白色念珠菌生物膜也具有抑制作用,且抑制率与药物质量浓度呈正相关。观察48 h时常态生物膜结构中大部分是活菌,有少量死菌存在;随芍药苷质量浓度改变白色念珠菌生物膜中死菌比例不断增高,其抑菌活性相对弱于洗必泰。表明芍药苷对体外白色念珠菌生物膜有较明显的抑制作用。
|
中图分类号: