2.1 最大吸收波长的确定 通过对卡马西平对照品溶液、卡马西平pH /磁双重敏感性凝胶小球供试品溶液和空白pH/磁双重敏感性凝胶小球阴性供试品溶液在200-
400 nm波长范围内进行扫描发现,卡马西平对照品溶液、卡马西平pH/磁双重敏感性凝胶小球供试品溶液均在 285 nm波长处有最大吸收,而空白pH/磁双重敏感性凝胶小球阴性供试品溶液在该波长处无吸收,表明该凝胶小球处方所用载体材料不干扰卡马西平的测定,对测定无影响,方法专属性较好,因此确定285 nm波长为测定波长。
2.2 方法学考查实验结果 对卡马西平系列对照品溶液的紫外吸光度进行测定,并用最小二乘法进行处理,得线性回归方程为:A=0.051 6C+0.008 8,r=0.999 9。卡马西平在4.004-18.018 mg/L的质量浓度范围内线性关系良好。
精密度实验结果显示相对标准偏差值均小于1%,方法精密度良好,结果见表1。
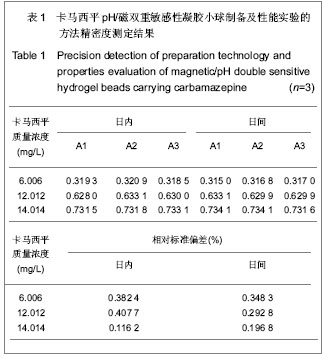
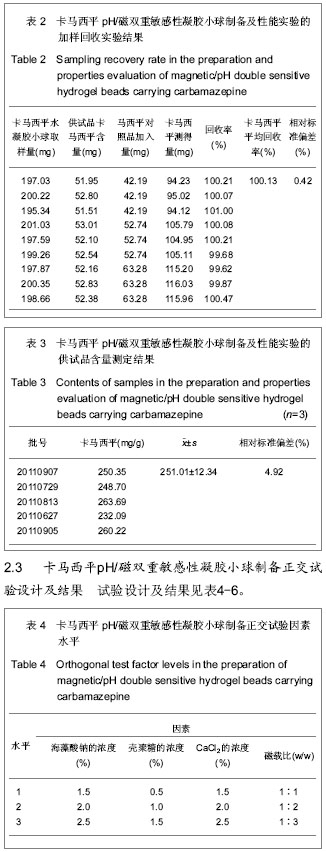
方法稳定性实验结果显示吸光度基本无变化,供试品溶液至少在6 h内稳定;重复性实验结果显示吸光度基本无变化,相对标准偏差为0.95%(
n=6),方法重复性较好;加样回收率实验结果满意,见表2;供试品含量测定结果见表3。
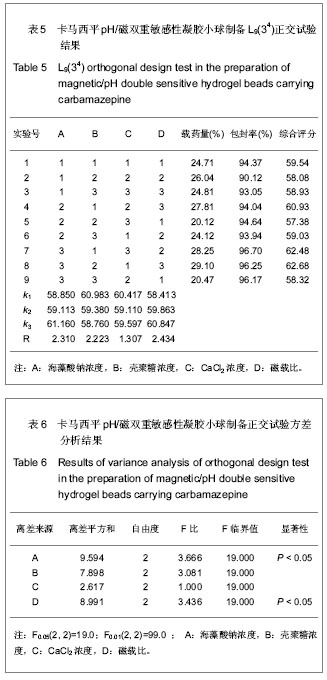
对表6进行直观分析,各因素的影响大小顺序依次为:D>A> B>C,最佳工艺条件为A
3B
1C
1D
3,即海藻酸钠浓度为2.5%,壳聚糖浓度为0.5%,氯化钙浓度为1.5%,磁载比为1∶3。而表6方差分析结果显示,海藻酸钠的浓度(A)和磁载比(D)为比较显著的影响因素。实验发现海藻酸钠浓度为2.5%时,凝胶小球溶胀行为较差,而氯化钙浓度为2.0%与1.5%时溶胀行为无明显差别,磁载比为1∶3时凝胶小球磁响应性较差。综合考虑,选择A
1B
2C
2D
2为最佳制备工艺,即海藻酸钠浓度为1.5%,壳聚糖浓度为0.5%,氯化钙浓度为2.0%,磁载比为1∶2。
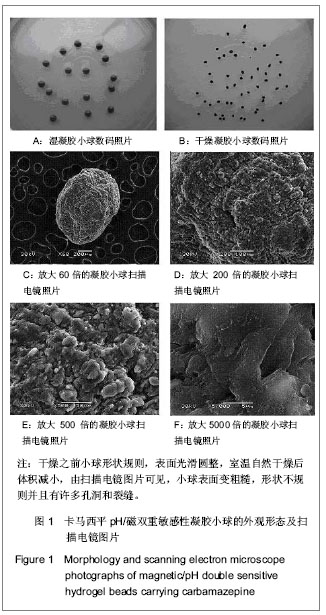
2.4 卡马西平pH/磁双重敏感性凝胶小球外观形态观察结果 见图1。
由图1可以看出,干燥之前小球形状规则,表面光滑圆整,直径为3.5-4.5 mm,见图1A,室温自然干燥后体积减小,直径为1.0-2.0 mm,见图1B;由扫描电镜图片可见,小球表面变粗糙,形状不规则并且有许多孔洞和裂缝,这是由于小球在自然干燥过程中失水不均匀所致。
 2.5 卡马西平pH/磁双重敏感性凝胶小球红外图谱测定结果
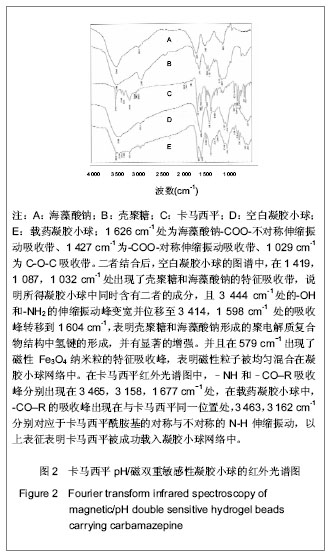
2.5 卡马西平pH/磁双重敏感性凝胶小球红外图谱测定结果 见图2。由图2可见,3 444 cm
-1处是壳聚糖分子中-OH 和-NH2 的伸缩振动峰,2 877 cm
-1处是-CH
2和-CH的振动峰,1 656 cm
-1处是酰胺I的吸收峰,1 598 cm
-1处的峰是酰胺Ⅱ吸收峰
[6]。而1 095 cm
-1和1 042 cm
-1处分别是仲羟基和伯羟基的振动吸收峰
[7]。图中1 626 cm
-1处为海藻酸钠-COO-不对称伸缩振动吸收带、1 427 cm
-1为-COO-对称伸缩振动吸收带、1 029 cm
-1为C-O-C吸收带。二者结合后,空白凝胶小球的图谱中,在1 419,1 087,1 032 cm
-1处出现了壳聚糖和海藻酸钠的特征吸收带,说明所得凝胶小球中同时含有二者的成分,且
3 444 cm-1处的-OH和-NH2的伸缩振动峰变宽并位移至3 414,1 598 cm
-1处的吸收峰转移到1 604 cm
-1,表明壳聚糖和海藻酸钠形成的聚电解质复合物结构中氢键的形成,并有显著的增强。并且在579 cm
-1出现了磁性Fe
3O
4纳米粒的特征吸收峰,表明磁性粒子被均匀混合在凝胶小球网络中。在卡马西平红外光谱图中,-NH和-CO-R吸收峰分别出现在3 465,3 158,1 677 cm
-1处
[8],在载药凝胶小球中,-CO-R的吸收峰出现在与卡马西平同一位置处,3 463和3 162 cm
-1分别对应于卡马西平酰胺基的对称与不对称的N-H伸缩振动,以上表征表明卡马西平被成功载入凝胶小球网络中。
 2.6 卡马西平pH/磁双重敏感性凝胶小球磁性能测定结果
2.6 卡马西平pH/磁双重敏感性凝胶小球磁性能测定结果 见图3。图3显示,Fe
3O
4纳米粒的饱和磁化强度为
58.57 emu/g,由于磁性纳米粒在凝胶小球中的含量较小,因此小球具有相对较小的磁饱和强度,为13.24 emu/g,但是由图可知,凝胶小球没有矫顽力,剩余磁化强度为0,可以完全消除磁性团聚,因此其在室温下拥有良好的超顺磁性,可以在外加磁场的诱导下定向移动而聚集,在撤去外加磁场后不显示磁性,并且可以均匀的分散而定期、安全排出体外
[9],为一种性能良好的磁性载体。
由图4可见,凝胶小球在人工胃液中几乎不溶胀,而在人工肠液中溶胀度最大可达到32%。因为凝胶小球在pH值1.5溶液中有收缩的趋势,比较稳定,这是因为海藻酸钠的羧基在pH值小于4的环境中发生了质子化,所以他们之间的静电排斥力减小而使凝胶网络趋向于收缩
[10]。在pH值6.8的缓冲液中,海藻酸钠结构中未参与交联的羧基和从海藻酸钙凝胶网络中解离的羧基离子化产生大量的静电斥力并且吸收水分,因此使网络结构膨胀而表现为较大的溶胀度
[11]。
 2.8 卡马西平pH/磁双重敏感性凝胶小球的连续释放行为考查结果
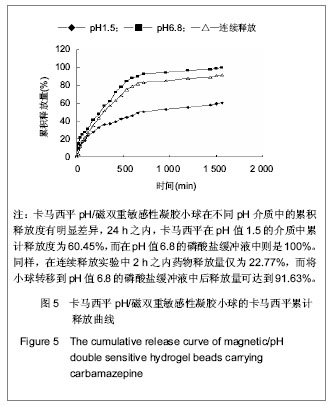
2.8 卡马西平pH/磁双重敏感性凝胶小球的连续释放行为考查结果 见图5。由图5可知,卡马西平pH /磁双重敏感性凝胶小球在不同pH介质中的累积释放度有明显的差异,24 h之内,卡马西平在pH值1.5的介质中累计释放度为60.45%,而在pH6.8的磷酸盐缓冲液中则是100%。同样,在连续释放实验中,2 h之内药物释放量仅为22.77%,而将小球转移到pH值6.8的磷酸盐缓冲液中后释放量可达到91.63%。在pH值1.5的环境中,羧基的电离受到抑制,同时壳聚糖氨基正电荷增多,与海藻酸盐羧酸根负离子间的静电作用加强,使整个凝胶网孔缩小,吸水力下降,保持紧缩状态,药物的释放主要是靠酸性溶液对外层壳聚糖的溶解以及药物的扩散作用,因此人工胃液中释放量较小。而在pH值6.8的人工肠液中时,环境中的钠离子能与钙离子发生交换反应,使其与海藻酸钠的交联减弱;同时由于海藻酸盐羧酸根离子解离度增加,分子间斥力增大,凝胶网孔变大,结构疏松而迅速膨胀,通透性增大,这时,药物的释放主要靠凝胶网络的瓦解及海藻酸盐核心的溶解而大量释放,因此在人工肠液中有较大的释放量
[12]。所以,卡马西平pH/磁双重敏感性凝胶小球经口服给药以后,在胃中释放极少量药物,待进入到肠道以后,药物才被缓慢释放出来,减小了突释效应,有利于维持血药浓度的稳定。
 2.9 卡马西平pH/磁双重敏感性凝胶小球释放机制分析
2.9 卡马西平pH/磁双重敏感性凝胶小球释放机制分析 为了进一步阐明药物在卡马西平pH/磁双重敏感性凝胶小球中释放机制,实验采用peppas方程对药物释放机制进行分析。
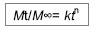
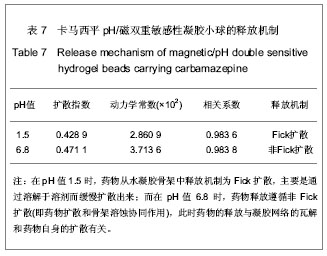
方程中Mt/M∞为药物在某一时刻的累积释放分数(以%表示);
t为释放时间;
k为常数,该常数随不同药物或不同处方以及不同释放条件而变化,该常数的大小是表征释放速率大小的重要参数;
n为释放参数,该参数是peppas方程中表征释放机制的特征参数,该参数与制剂骨架的形状有关;对于球型制剂,peppas方程认为当0.43<
n<0.85时,药物释放机制为非Fick扩散(即药物扩散和骨架溶蚀协同作用);当
n<0.43时,为Fick扩散;当
n>0.85时,为骨架溶蚀机制
[13]。
将方程演化成以下形式:lg Mt/M∞=lgk+nlgt
采用最小二乘法即可得到peppas方程中的n值,用以判断药物从骨架中的释放机制。卡马西平pH/磁双重敏感性凝胶小球在不同pH条件下的药物释放机制结果见表7。
由表7可知,在pH值1.5时,药物从水凝胶骨架中释放机制为Fick扩散,主要是通过溶解于溶剂而缓慢扩散出来;而在pH值6.8时,药物释放遵循非Fick扩散(即药物扩散和骨架溶蚀协同作用),此时药物的释放与凝胶网络的瓦解和药物自身的扩散有关。因此,当凝胶小球经口服进入人体以后,其在胃中的药物释放是由凝胶网络内外浓度差引发的自由扩散所产生的,而在肠道中则是由自由扩散和凝胶网络自身的破裂瓦解共同作用的。







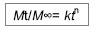

.jpg)
.jpg)