中国组织工程研究 ›› 2013, Vol. 17 ›› Issue (1): 86-91.doi: 10.3969/j.issn.2095-4344.2013.01.014
• 干细胞培养与分化 stem cell culture and differentiation • 上一篇 下一篇
以4种基因诱导产前诊断绒毛细胞建立诱导性多能干细胞
骆玉梅,范 勇,陈欣洁,岳 磊,黎 青,余波澜,何文智,马晓燕,孙筱放
- 广东省产科重大疾病重点实验室,广东省高校生殖与遗传重点实验室,广州医学院第三附属医院,广东省广州市 510150
Generation of induced pluripotent stem cells from villus cells after induction by four kinds of genes during prenatal diagnosis
Luo Yu-mei, Fan Yong, Chen Xin-jie, Yue Lei, Li Qing, Yu Bo-lan, He Wen-zhi, Ma Xiao-yan, Sun Xiao-fang
- Key Laboratory for Major Obstetric Diseases of Guangdong Province, Key Laboratory of Reproduction and Hereditary of the Universities in Guangdong Province, the Third Affiliated Hospital of Guangzhou Medical College, Guangzhou 510150, Guangdong Province, China
摘要:
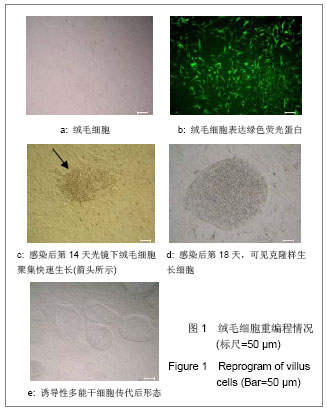
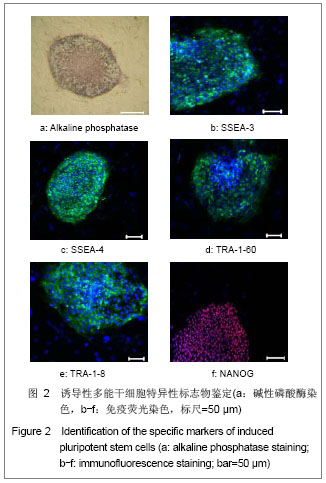
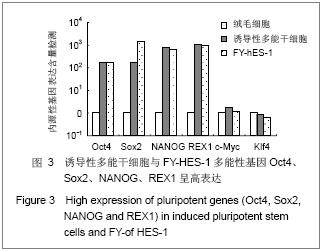
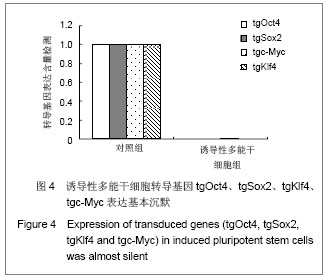
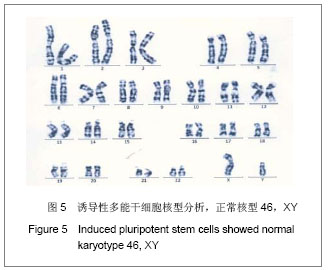
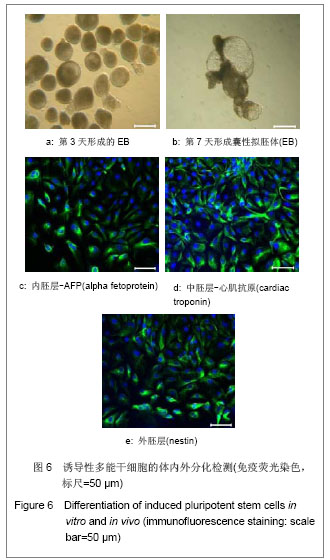
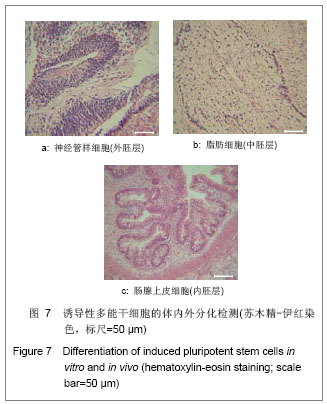
背景:诱导性多能干细胞因具有多能性特征,可以诱导分化为特定的细胞,包括神经细胞、造血细胞等。 目的:建立产前诊断绒毛细胞来源的诱导性多能干细胞。 方法:运用反转录病毒介导4种基因hOct4、hSox2、hc-Myc、hKlf4诱导产前诊断绒毛细胞,对建立的诱导性多能干细胞进行多能性、体内外分化能力、核型等鉴定。 结果与结论:建立的诱导性多能干细胞能维持自我更新状态,在蛋白和mRNA水平上高表达全能性的标志基因,具有体内、外分化潜能;在体外长期培养能维持正常核型。说明4种全能性基因转入绒毛细胞可获得具有多能性的诱导性多能干细胞,这为胎儿的细胞自体移植治疗提供理想来源,为产前诊断疾病机制研究提供很好的细胞模型。
中图分类号: