2.1 跟腱生物力学 跟腱起于小腿中部约1/3处,止于跟骨后结节中点,由腓肠肌和比目鱼肌肌腱合并构成,是连接脚后跟和小腿肌肉的重要纤维组织[3]。跟腱的主要功能是使踝关节跖屈,因此跟腱是人体做后蹬、起跳等动作的主要受力器官[4]。同时,跟腱是人体中韧性最强、能够承受拉力最大的肌腱,在缓冲和吸收肌肉力量、减少肌肉损伤以及保护骨骼中具有重要作用[4]。
跟腱主要由跟腱纤维构成,胶原蛋白约占跟腱干重的70%,其中几乎95%是弹性蛋白较少的Ⅰ型胶原蛋白,这些致密的胶原蛋白纤维形成很多交联,使跟腱具有良好的韧性和力量,能够承受非常大的张力[5]。Ⅲ型胶原蛋白纤维较细且易拉伸,对拉力的抵抗能力较弱,更容易断裂;当跟腱受损或断裂时,Ⅲ型胶原蛋白的优势是能够快速的进行交联,使跟腱受伤或修复处尽快达到稳定状态[5-6]。在静止状态时,由于胶原蛋白纤维的褶皱形态,跟腱外形为锯齿状[7]。当肌腱拉伸超过原有长度的2%时,跟腱的锯齿状消失;如果跟腱拉伸长度超出原长度的4%,跟腱可能会出现受伤状况;拉伸超出原长度8%时,跟腱会发生断裂[7]。
2.2 运动性跟腱断裂的原因 对于导致运动性跟腱断裂的原因,目前并没有一致的结论。相关研究主要集中在退化论和力学论两方面。在多数跟腱断裂案例中,不同断裂机制之间可能是共同作用、相互关联的,而在个案中,根据人群和运动种类的不同,跟腱断裂可能受某一方面原因的影响较大。
2.2.1 退化论 在运动中最容易出现跟腱断裂的人群为40-60岁的中年男性。研究认为,40-60岁的中年男性肌腱发生退化较明显,而运动量并没有因此而明显下降,造成此人群跟腱发生断裂的概率增加[8-9]。根据Tuite等[10]的研究,年龄老化能对人体内所有胶原结构产生影响,这种影响包括胶原纤维褶皱角度变小、胶原纤维直径变小、细胞外水分含量下降、弹性蛋白含量增加以及跟腱内血管数量减少等不利变化。这些变化能降低跟腱处胶原纤维撕裂的阈值,增加运动中发生跟腱断裂的可能性[10]。
跟腱劳损也是导致跟腱退化的重要原因。研究报道,跟腱劳损和断裂的位置多发生在跟骨上方2-6 cm处。此处为跟腱最窄位置,且血管密度最低,血液循环不畅通,受损后恢复较慢[11]。在激烈运动中,踝关节频繁而急速的跖屈动作可能会使此处出现劳损。在此处已经发生劳损的情况下,若继续过度使用,会使血液供应更加困难,可能发生跟腱细胞坏死,造成跟腱钙化,使跟腱弹性受损,增加运动中跟腱断裂的可能性[11]。若出现跟腱劳损症状(一般表现为跟腱处疼痛)后,必须减少运动量甚至停止运动,待跟腱痊愈后再投入运动,防止由跟腱劳损发展为跟腱断裂[11]。
此外,部分药物的使用也可能成为跟腱断裂的原因。氟喹诺酮类、类固醇等药物作用于跟腱可能会打乱跟腱细胞正常代谢,影响细胞增殖,造成跟腱炎、腱鞘炎等,使跟腱处于脆弱状态[12]。长期使用此类药物将增加运动中跟腱断裂的概率[12]。可的松虽然能缓解跟腱出现损伤时的不适感,但接受可的松注射可能使跟腱在无意识情况下出现过度拉伸,导致跟腱断裂[12]。
2.2.2 力学论 跟腱是一种刚性较大、弹性较小的生物材料,当所承受拉力导致跟腱拉伸超过原长度4%时便会有受伤和断裂的危险[7]。当跟腱受力突然剧增时,跟腱被急剧拉伸,最为狭窄的跟腱中段应力增幅和被拉伸程度比两端更为明显。若小腿肌群收缩的合力超过跟腱的承受范围,跟腱中段最狭窄处可能首先达到拉伸极限而发生跟腱断裂[12]。跟腱受力达到峰值瞬间出现在踝关节从背屈转为跖屈的过程中,常见于跑步、跳跃等动作中。研究发现,在专业跳远运动员踏跳瞬间,其起跳腿跟腱承受的拉力高达780 kg,需要跟腱具备极强的抗拉能力[13-14]。
在正常状态中,人体小腿肌肉、跟腱和骨骼构成的系统在运动中承受的力是协调、均匀的。在大强度运动中,特别是需要用力起跳或急转急停的运动中,足的位置频繁快速转换,造成跟腱需要在不稳定的位置承受小腿肌群突然的过度或不协调收缩,引起跟腱承载负荷不均匀,导致跟腱受伤,而在跟腱处于疲劳状态时则可能造成跟腱的断裂[13](表1)。

2.3 运动性跟腱断裂的治疗 治疗跟腱断裂的最终目的是恢复跟腱的长度和韧性,使跟腱在运动中能恢复到正常的功能。运动性跟腱断裂的治疗选择一般分为两类:保守治疗和手术治疗。在20世纪20年代Abrahamsen研究[2]报道手术治疗的理想效果后,手术治疗跟腱断裂开始普及。
2.3.1 保守治疗 跟腱具有自愈性,因此在出现跟腱断裂后,采用夹板及石膏外固定踝关节和小腿8-10周后断裂处会自动愈合[15]。保守治疗已经被证明能够取得理想的修复结果,并且可以避免手术修复带来的并发症。然而,多数研究表明,保守治疗跟腱断裂后患者跟腱二次断裂概率较高,为11%-39%,这可能与保守治疗中跟腱的愈合不完全有关[16-18]。总体来看,目前保守治疗适用于康复后对跟腱所能承受强度要求不高或者有手术禁忌证的患者。
近年研究发现,选择保守治疗跟腱断裂时,如果放弃石膏外固定,在跟腱愈合早期配合适度功能锻炼能够降低愈合后的二次断裂概率[19]。对于患者可以进行患侧肢体承重康复训练的具体时间,Thermann等[19]研究认为跟腱断裂患者在受伤后5 d可开始进行一定的运动,然而目前此方面研究的观点并不一致。
2.3.2 手术治疗
⑴开放手术:开放手术治疗被认为是治疗急性跟腱断裂的理想方法。开放手术治疗的优点是患者康复后跟腱二次断裂概率较低,仅为1.5%-5%[20-22]。同时,手术修复断裂的跟腱能够在愈合早期使跟腱具备一定的抗拉能力,有利于愈合早期康复训练的开展[4]。
目前存在的治疗跟腱断裂的开放手术方法主要有:直接缝合法、自身腱组织转移修复法、V-Y肌腱延长修补术、人工材料修复等。其中,将跟腱两断端直接缝合的方法最为简单实用,且术后恢复较快,恢复后跟腱能够承受较大的负荷和运动强度,二次断裂率低,是康复后需要继续投入运动训练的人群的理想选择[23]。
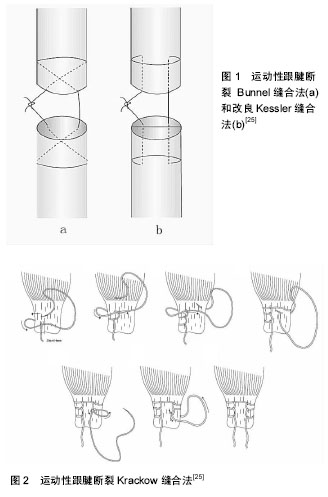
在直接缝合跟腱断端手术中,需要在断裂跟腱内侧缘打开一个长度为6-10 cm的切口(切口因不同缝合方法而异),使跟腱露出[24]。确认跟腱的准确位置后,将血肿块去除[24]。清理并理顺两断端后,主要有3种主流的缝合方式可供选择:Bunnel缝合法(图1a)、改良Kessler缝合法(图1b)和Krackow缝合法(图2)[25]。3种缝合方法各有优、缺点:Bennel缝合法能最大程度的恢复跟腱的最初形态,避免跟腱长度缩短,破环腱旁组织较少;相比于Bennel缝合法,改良Kessler缝合法的优点是缝合强度高,恢复后跟腱抗拉伸能力较强。但这两种缝合法一般适用于跟腱断端比较整齐的类型,对断端为马尾状的撕裂类型并不适用,而运动性跟腱断裂多为马尾状撕裂[25-26]。同时,改良Kessler缝合法需要较长的切口,较其他方法可能会造成较大的软组织损伤,不利于早期康复训练的开展。Krackow缝合法不但缝合强度较高,能使跟腱愈合后恢复至较强的抗拉伸能力,而且对跟腱两侧有锁边功能,是运动性跟腱断裂的理想缝合方法[25,27-28]。
由于需要对皮肤进行较长的切口,手术缝合治疗跟腱断裂的主要缺点是可能引起术后并发症。Nistor研 究[29]报道,在接受开放手术治疗后,跟腱处出现深部感染概率为1%,瘘口形成概率达3%,皮肤和肌腱坏死概率为2%。Lemaire等研究[30]报道,在4477例开放手术治疗跟腱断裂病例中,出现并发症的概率为12.5%。
⑵经皮手术:经皮手术修复跟腱断裂不需要打开皮肤,也无需露出跟腱,只需要采用有限的软组织开放,使用Bunnell针沿着跟腱内侧和外侧进行穿刺修复。因此经皮手术修复跟腱断裂最大的优点是伤口较小,避免过多的组织切除,将对局部血液供应的干扰程度下降到最低,因此降低了术后组织感染等并发症的发生率。Sirovy等[31]对115例运动性跟腱断裂案例进行了研究(73例采用开放手术治疗,42例采用经皮手术治疗),结果显示:在采用开放手术治疗的患者中,发生术后并发症的患者占24.7%;在采用经皮手术修复的患者中,此比例仅为11.8%。
从生物力学角度,采用经皮手术修复跟腱断裂很难达到最好的缝合效果,可能会使跟腱愈合后的力量受到影响,因此与开放手术相比可能会有更高的跟腱二次断裂概率。Cretnik等[32]对132例经皮穿刺手术与105例Kessler缝合法修复跟腱断裂的效果进行了对比,发现采用经皮手术的患者中出现跟腱二次断裂的比例为3.7%,高于采用Kessler缝合法的患者(2.8%)。然而,对于经皮手术修复跟腱断裂的生物力学效果,目前研究结果并不一致。Goren等[33]研究发现采用经皮手术修复跟腱断裂,愈合后患者跖屈强度和耐力与传统开放手术无显著性差异。就目前存在的研究来看,对经皮手术和开放手术治疗运动性跟腱断裂的生物力学效果方面的细微差异,还有待日后深入研究。
2.3.3 术后康复 有研究表明,田径运动员的跟腱相对于普通人群更加粗壮,说明训练可能能够诱导跟腱肥 大[34]。Woo等[35]以猪跟腱为研究对象进行12个月的运动训练,发现跟腱的刚度、极限载荷和干质量均显著增加,胶原蛋白含量显著增加,认为长期运动能够提高猪跟腱的抗拉伸能力,增加其质量,使其能够承受的载荷增加。以上研究结果均能够表明运动训练在提高和维持跟腱性能中的重要作用。与此相反,长期卧床则会使跟腱力量下降,不利于跟腱功能的恢复[34]。跟腱组织,尤其是跟腱中段缺乏血液供应,代谢缓慢,因此愈合周期较为漫长[36]。对于跟腱断裂患者,使跟腱长期处于静止状态会导致跟腱在愈合后期没有应力负荷,粘弹性和抗拉能力降低,吸收弹性能量的能力下降,增加再次断裂的概率[11,37]。同时,跟腱愈合期间对踝关节进行长期固定可能引起小腿附近肌肉、软骨萎缩等并发症的发生。研究认为,相比于长期踝关节固定,在术后早期进行康复训练有利于跟腱功能的快速恢复,对跟腱断裂患者的恢复极其关键[38-39]。Brumann等[38]对跟腱急性断裂后的康复研究进行了系统分析。该研究认为,在术后早期使跟腱进行承重训练的康复效果效果优于无承重训练;跟腱术后早期放弃踝关节固定的康复效果优于踝关节固定[38]。在术后早期放弃踝关节固定,并结合跟腱的承重训练是最佳康复方案,能够显著缩短患者重新正常工作、运动的时间,并且能够减少术后并发症的出现[38]。Holm等[39]对所纳入7篇文献进行分析后认为:如今对于运动性跟腱断裂的治疗,手术与非手术的选择可能已并非最重要的问题,两种不同治疗方法间的效果差异已经变得越来越小。相较而言,术后早期的康复过程则变得愈加重要,术后康复甚至已经成为治疗跟腱断裂中最为关键的一环[39]。可见,在传统方案中,术后进行6周石膏固定后再进行康复训练的效果可能并不理想,在跟腱愈合早期就应该开展康复训练的观点被越来越多的研究所认可。
然而,过早的应力负荷可能会破坏跟腱的愈合。在跟腱愈合早期,Ⅲ型胶原蛋白含量较高,跟腱较软,很容易被拉长,且瘢痕组织并未完全愈合,激进的康复训练容易导致跟腱再次断裂。因此,康复训练中的运动方式和运动强度要保证既能使跟腱承受一定的应力负荷,又不会将缝合处拉开导致跟腱再次断裂,这就使术后康复训练开展时间和训练强度的确定变得十分关键。然而,目前此方面的研究并没有一致的结论。部分研究认为术后在石膏固定下踝关节可立即进行适当负重训练,也有研究支持术后几天甚至几周才能开始康复训练[40]。关于跟腱断裂术后康复的方式,研究发现,离心收缩的效果优于向心收缩、牵拉等,但因为难以准确判断体内跟腱的愈合进程,怎样确定合适的收缩强度尚不明 确[41-42]。可见,术后如何评估体内跟腱的力学特性、判断其愈合程度,以指导康复训练方案的制定,应为此后跟腱断裂治疗领域的重要研究方向。
此外,近期研究发现,由多种细胞因子调控的内源性愈合对跟腱术后康复能够发挥重要作用[43-45]。胶原蛋白纤维决定跟腱力量,胶原蛋白含量和其交联是影响跟腱结构和功能的主要因素[46]。胶原蛋白在人体内的合成途径十分复杂,所有种类的胶原蛋白在产生之初都以原骨胶原的形式存在[46]。Kashiwagi等[43]以大鼠为研究对象,将其跟腱切断后立即进行修复,再将两种不同剂量的转化生长因子溶入磷酸盐缓冲盐水中,注射到修复位置,结果显示Ⅰ型和Ⅲ型原骨胶原蛋白mRNA表达的增加呈现剂量性依赖。该结果表明,转化生长因子β1浓度的提升有利于大鼠断裂跟腱的修复。究其原因,胶原蛋白纤维交连的形成过程由赖氨酰氧化酶催化,而转化生长因子β1能显著提高赖氨酰氧化酶mRNA和赖氨酰氧化酶的含量[44,46]。Hou等[45]研究进一步验证了此结论:相比于普通受伤跟腱,将转染转化生长因子β1基因的骨髓间充质干细胞通过手术移植到受伤的跟腱中能够提高Ⅰ型胶原蛋白含量和基质重塑速度,促进胶原蛋白交联的形成,提高跟腱力量。综合前人研究结果可见,在跟腱受伤后,转化生长因子β1有助于恢复跟腱力量和性能,可以作为跟腱治疗和康复的又一条新途径,具有很高的临床应用价值。对于包括血管内皮生长因子、胰岛素生长因子等其他细胞因子在跟腱康复中的作用,目前尚未得到广泛认可,需更多的研究结果加以验证。
.jpg) 文题释义:
跟腱:是人体最粗大最强壮的肌腱。跟腱长约15 cm,由小腿三头肌(比目鱼肌、腓肠肌内、外头)的肌腱融合形成。在此过程中,跟腱的腱纤维有90°的扭转。跟腱的主要功能是屈小腿和跖屈踝关节,是小腿肌肉力量传导至足部的最主要的解剖结构。人能够直立、站稳,能跑、能跳,靠的都是它。如果单侧跟腱断裂,就会出现跛行,如果双侧跟腱均断裂,则不能行走。
跟腱断裂:是跟腱组织的断裂。临床上常见的跟腱自发性断裂一般发生在单侧肢体。这种断裂可以在跟腱-跟骨连接部,也可以在跟腱-肌腹连接处或是跟腱组织本身。70%以上的自发性断裂在运动时发生,由于伤后的肿胀掩盖了跟腱断裂导致的凹陷,跖肌腱和足母长屈肌腱的存在使踝关节跖屈肌力部分得以代偿从而还可以行走,X射线片检查也没有骨折。据统计,有高达25%的跟腱断裂可以在初次就诊时被漏诊。
文题释义:
跟腱:是人体最粗大最强壮的肌腱。跟腱长约15 cm,由小腿三头肌(比目鱼肌、腓肠肌内、外头)的肌腱融合形成。在此过程中,跟腱的腱纤维有90°的扭转。跟腱的主要功能是屈小腿和跖屈踝关节,是小腿肌肉力量传导至足部的最主要的解剖结构。人能够直立、站稳,能跑、能跳,靠的都是它。如果单侧跟腱断裂,就会出现跛行,如果双侧跟腱均断裂,则不能行走。
跟腱断裂:是跟腱组织的断裂。临床上常见的跟腱自发性断裂一般发生在单侧肢体。这种断裂可以在跟腱-跟骨连接部,也可以在跟腱-肌腹连接处或是跟腱组织本身。70%以上的自发性断裂在运动时发生,由于伤后的肿胀掩盖了跟腱断裂导致的凹陷,跖肌腱和足母长屈肌腱的存在使踝关节跖屈肌力部分得以代偿从而还可以行走,X射线片检查也没有骨折。据统计,有高达25%的跟腱断裂可以在初次就诊时被漏诊。.jpg) 文题释义:
跟腱:是人体最粗大最强壮的肌腱。跟腱长约15 cm,由小腿三头肌(比目鱼肌、腓肠肌内、外头)的肌腱融合形成。在此过程中,跟腱的腱纤维有90°的扭转。跟腱的主要功能是屈小腿和跖屈踝关节,是小腿肌肉力量传导至足部的最主要的解剖结构。人能够直立、站稳,能跑、能跳,靠的都是它。如果单侧跟腱断裂,就会出现跛行,如果双侧跟腱均断裂,则不能行走。
跟腱断裂:是跟腱组织的断裂。临床上常见的跟腱自发性断裂一般发生在单侧肢体。这种断裂可以在跟腱-跟骨连接部,也可以在跟腱-肌腹连接处或是跟腱组织本身。70%以上的自发性断裂在运动时发生,由于伤后的肿胀掩盖了跟腱断裂导致的凹陷,跖肌腱和足母长屈肌腱的存在使踝关节跖屈肌力部分得以代偿从而还可以行走,X射线片检查也没有骨折。据统计,有高达25%的跟腱断裂可以在初次就诊时被漏诊。
文题释义:
跟腱:是人体最粗大最强壮的肌腱。跟腱长约15 cm,由小腿三头肌(比目鱼肌、腓肠肌内、外头)的肌腱融合形成。在此过程中,跟腱的腱纤维有90°的扭转。跟腱的主要功能是屈小腿和跖屈踝关节,是小腿肌肉力量传导至足部的最主要的解剖结构。人能够直立、站稳,能跑、能跳,靠的都是它。如果单侧跟腱断裂,就会出现跛行,如果双侧跟腱均断裂,则不能行走。
跟腱断裂:是跟腱组织的断裂。临床上常见的跟腱自发性断裂一般发生在单侧肢体。这种断裂可以在跟腱-跟骨连接部,也可以在跟腱-肌腹连接处或是跟腱组织本身。70%以上的自发性断裂在运动时发生,由于伤后的肿胀掩盖了跟腱断裂导致的凹陷,跖肌腱和足母长屈肌腱的存在使踝关节跖屈肌力部分得以代偿从而还可以行走,X射线片检查也没有骨折。据统计,有高达25%的跟腱断裂可以在初次就诊时被漏诊。

.jpg) 文题释义:
跟腱:是人体最粗大最强壮的肌腱。跟腱长约15 cm,由小腿三头肌(比目鱼肌、腓肠肌内、外头)的肌腱融合形成。在此过程中,跟腱的腱纤维有90°的扭转。跟腱的主要功能是屈小腿和跖屈踝关节,是小腿肌肉力量传导至足部的最主要的解剖结构。人能够直立、站稳,能跑、能跳,靠的都是它。如果单侧跟腱断裂,就会出现跛行,如果双侧跟腱均断裂,则不能行走。
跟腱断裂:是跟腱组织的断裂。临床上常见的跟腱自发性断裂一般发生在单侧肢体。这种断裂可以在跟腱-跟骨连接部,也可以在跟腱-肌腹连接处或是跟腱组织本身。70%以上的自发性断裂在运动时发生,由于伤后的肿胀掩盖了跟腱断裂导致的凹陷,跖肌腱和足母长屈肌腱的存在使踝关节跖屈肌力部分得以代偿从而还可以行走,X射线片检查也没有骨折。据统计,有高达25%的跟腱断裂可以在初次就诊时被漏诊。
文题释义:
跟腱:是人体最粗大最强壮的肌腱。跟腱长约15 cm,由小腿三头肌(比目鱼肌、腓肠肌内、外头)的肌腱融合形成。在此过程中,跟腱的腱纤维有90°的扭转。跟腱的主要功能是屈小腿和跖屈踝关节,是小腿肌肉力量传导至足部的最主要的解剖结构。人能够直立、站稳,能跑、能跳,靠的都是它。如果单侧跟腱断裂,就会出现跛行,如果双侧跟腱均断裂,则不能行走。
跟腱断裂:是跟腱组织的断裂。临床上常见的跟腱自发性断裂一般发生在单侧肢体。这种断裂可以在跟腱-跟骨连接部,也可以在跟腱-肌腹连接处或是跟腱组织本身。70%以上的自发性断裂在运动时发生,由于伤后的肿胀掩盖了跟腱断裂导致的凹陷,跖肌腱和足母长屈肌腱的存在使踝关节跖屈肌力部分得以代偿从而还可以行走,X射线片检查也没有骨折。据统计,有高达25%的跟腱断裂可以在初次就诊时被漏诊。