中国组织工程研究 ›› 2024, Vol. 28 ›› Issue (4): 499-504.doi: 10.12307/2024.323
• 软骨组织构建 cartilage tissue construction • 上一篇 下一篇
敲低环状RNA WD重复含蛋白1抑制膝骨关节炎软骨细胞增殖并诱导凋亡
申飞燕1,姚吉祥2,苏珊珊2,赵忠民2,唐巍东3
- 1长春中医药大学中西医结合学院,吉林省长春市 130000;2泰州市人民医院疼痛科,江苏省泰州市 225300;3江苏省钟山康复医院,江苏省南京市 210014
Knockdown of circRNA WD repeat containing protein 1 inhibits proliferation and induces apoptosis of chondrocytes in knee osteoarthritis
Shen Feiyan1, Yao Jixiang2, Su Shanshan2, Zhao Zhongmin2, Tang Weidong3
- 1College of Integrated Chinese and Western Medicine, Changchun University of Chinese Medicine, Changchun 130000, Jilin Province, China; 2Department of Pain, Taizhou People’s Hospital, Taizhou 225300, Jiangsu Province, China; 3Jiangsu Zhongshan Rehabilitation Hospital, Nanjing 210014, Jiangsu Province, China
摘要:

文题释义:
环状RNA (circRNA):是一类特殊的非编码RNA分子,也是近年非编码RNA领域研究的热点和重点;其在真核生物内广泛表达,circRNA环状共价闭合结构,没有5′帽子结构和3′polyA尾巴,是反向间接形成,不受RNA外切酶影响,稳定性良好,且大多数circRNA位于细胞质。miRNA:是一种内源性非编码RNA分子,由22-25个核苷酸组成的小分子RNA,circRNA可与miRNA竞争结合,并充当miRNA海绵,进而解除miRNA下游靶基因mRNA表达抑制作用,针对以上作用机制称为竞争性内源RNA机制。近年研究已证实,circRNA/miRNA/mRNA轴在多种疾病、恶性肿瘤中发挥着重要调控作用。
背景:环状RNA(circular RNA,circRNA)在多种疾病或肿瘤中发挥着重要作用,近年研究结果发现,膝骨关节炎中circRNA失常表达,并可通过调控微小RNA(miRNA)/mRNA参与疾病进展。
目的:探究circ-BRWD1/miR-488-3p/DNMT3A对膝骨关节炎软骨细胞增殖和凋亡的影响。方法:实时荧光定量PCR检测膝骨关节炎软骨细胞miR-488-3p、circ-BRWD1、DNMT3A表达。将细胞分为si-NC组、si-circ-BRWD1组、si-circ-BRWD1+anti-miR-NC组、si-circ-BRWD1+anti-miR-488-3p组、vector组、circ-BRWD1组、miR-NC组、miR-488-3p组、miR-488-3p+vector组、miR-488-3p+DNMT3A组、anti-miR-NC组、anti-miR-488-3p组;实时荧光定量PCR检测circ-BRWD1、miR-488-3p、DNMT3A表达,MTT、流式细胞术检测增殖和凋亡,Western blot检测DNMT3A、增殖、凋亡相关蛋白表达;双荧光素酶报告实验检测circ-BRWD1与miR-488-3p、miR-488-3p与DNMT3A的靶向关系。
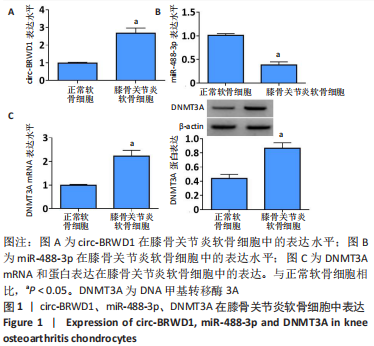
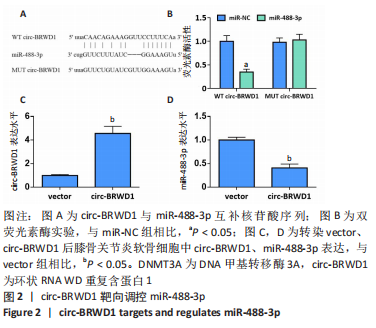
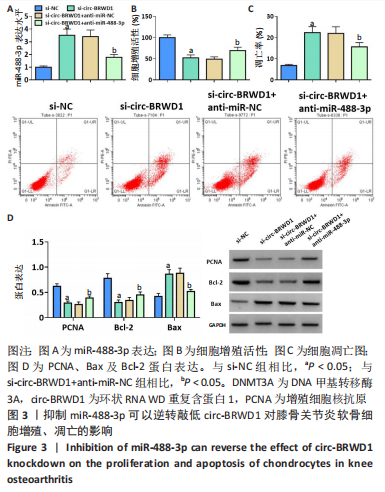
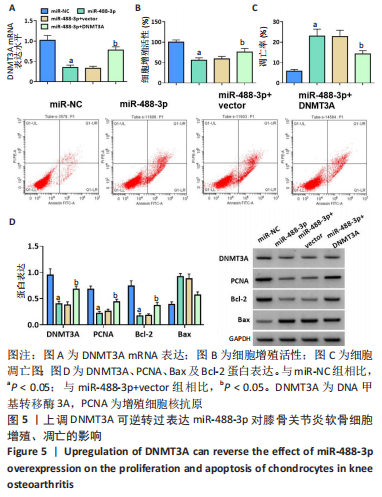
结果与结论:①与正常软骨细胞相比,circ-BRWD1、DNMT3A在膝骨关节炎软骨细胞中高表达,miR-488-3p低表达;②敲低circ-BRWD1或过表达miR-488-3p可抑制膝骨关节炎软骨细胞增殖并诱导凋亡;③circ-BRWD1靶向负调控miR-488-3p,抑制miR-488-3p可逆转敲低
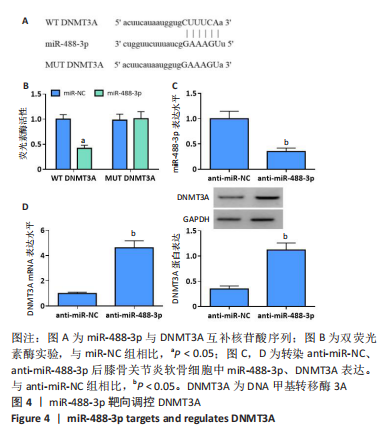
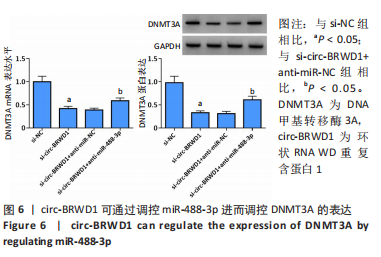
circ-BRWD1对膝骨关节炎软骨细胞增殖、凋亡的影响;④miR-488-3p靶向负调控DNMT3A,上调DNMT3A可逆转过表达miR-488-3p对膝骨关节炎软骨细胞增殖、凋亡的影响;⑤circ-BRWD1可通过调控miR-488-3p进而调控DNMT3A的表达;⑥结果表明,敲低circ-BRWD1可抑制膝骨关节炎软骨细胞增殖并诱导凋亡,其作用机制可能与调控miR-488-3p/DNMT3A轴有关。
https://orcid.org/0009-0006-9400-859X(申飞燕)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号: