1.1 设计 随机对照动物实验,组间比较采用两独立样本t检验。
1.2 时间及地点 实验于2022年1月至2023年2月在遵义医科大学基础药理教育部重点实验室完成。
1.3 材料
1.3.1 实验动物 雌性C57BL/6J小鼠60只,6周龄,体质量(18.36±3.65) g,购于斯贝福生物技术有限公司(北京),许可证号:SCXK(京)2019-0010。该研究获得遵义医科大学伦理委员会批准,审批号为伦审〔2020〕2-473号,实验结果报道遵从ARRIVE (the Animal Research: Reporting of in vivo Experiments guidelines)动物实验报道指南。
1.3.2 实验仪器及试剂 超净工作台(苏净安泰,中国);CO2恒温培养箱(Thermo Scientific,美国);高压灭菌锅(HIRAYAMA,日本);倒置相差显微镜(Olympus,日本);低速离心机(中佳科学仪器有限公司,中国);高速离心机(Beckman Coulter,美国);超纯水机(Millipore,法国);流式细胞仪(Beckmen,美国);实时荧光定量 PCR 仪(BIO-RAD,美国);PCR反转录仪(BIO-RAD,美国);移液枪(Eppendorf,德国);细胞培养瓶(Nest,美国);α-MEM(Gibco,美国);胎牛血清(Gibco,澳大利亚);磷酸盐缓冲液(Solarbio,中国);0.25%胰蛋白酶(Solarbio,中国);青霉素链霉素混合液(Solarbio,中国);β-甘油磷酸钠(Solarbio,中国);二甲基亚砜(Solarbio,中国);吲哚美辛(Solarbio,中国);维生素C(Sigma,中国);IBMX(Solarbio,中国);油红O染液(Solarbio,中国);茜素红染液(Solarbio,中国);Trizol(TAKARA,日本);RNA反转录试剂盒(生工生物,中国);荧光定量试剂盒(生工生物,中国);相关引物(生工生物,中国);BCA蛋白试剂盒(Solarbio,中国)。
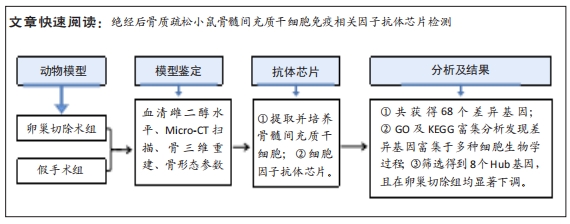
1.4 实验方法 实验技术路线图如图1所示。
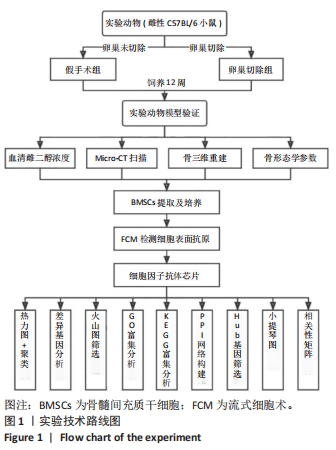
1.4.1 POP小鼠模型的建立 选取雌性C57BL /6小鼠30只,使用1%戊巴比妥钠溶液以50 mg/kg剂量麻醉小鼠后剃除其背部毛发完成备皮,用碘伏消毒备皮部位的皮肤,随后剪开背部皮肤,分层剥离皮下、脂肪及腹腔层。随机抽取其中15只小鼠找到脏层的双侧卵巢,结扎和剪弃,建立POP小鼠模型,作为卵巢切除组;剩余15只小鼠仅剪去卵巢周围组织作为假手术组。两组小鼠在室内温度20-26 ℃,相对湿度40%-70%的条件下饲养12周。
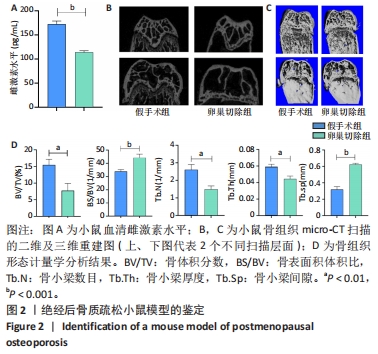
1.4.2 POP小鼠模型的验证 建模后12周,取假手术组和卵巢切除组小鼠各3只,注射1%戊巴比妥钠溶液麻醉,固定并剪去小鼠胡须。用乙醇轻轻擦拭眼周皮肤待其自然干燥,轻轻按压待取血部位的眼部皮肤使眼球充血突出。将小鼠头部朝下,用弯头镊摘取眼球,同时用指腹按压小鼠心脏部位加快滴血速度。将取出的血液收集于无菌无酶的PE管中,静置2-4 h后可见血液分层,吸取100 μL上层血清转移至新的无菌无酶的PE管中,采用ELISA试剂盒检测血清中雌二醇水平。取血完成后采用颈椎脱臼法处死小鼠,取出小鼠长骨,去净骨上附着的软组织,以40 g/L多聚甲醛溶液浸泡,送至重庆医科大学附属口腔医院进行Micro-CT 扫描及分析,以10.44 μm分辨率扫描小鼠长骨(电流500 mA、电压160 kV),通过计算机软件进行骨形态分析和三维重建。
1.4.3 BMSCs的提取与培养 每组选取6只小鼠,注射1%戊巴比妥钠溶液麻醉小鼠后采用颈椎脱臼法处死,用体积分数75%乙醇浸泡5 min,取出小鼠置于超净工作台内,组织剪分离小鼠长骨,用无菌纱布去净骨上附着的软组织,灭菌PBS冲洗1 min,置于含体积分数15%胎牛血清、1%青霉素-链霉素混合液的α-MEM完全培养基中,剪去胫骨以及股骨两端,将其浸泡于完全培养基中,用吸取完全培养基的1 mL注射器反复冲洗骨髓腔,将混合液转移至25 cm2的透气培养瓶中,轻轻振荡培养瓶,静置于37 ℃、体积分数5% CO2 细胞孵育箱中培养。观察细胞的生长状态,每2 d更换1次完全培养基,待贴壁细胞生长融合达到85%后,用0.25%胰蛋白酶消化1 min,镜下观察贴壁细胞脱落后用5%完全培养基终止消化,以1∶2进行传代,BMSCs传代至第2代后用于以下实验。
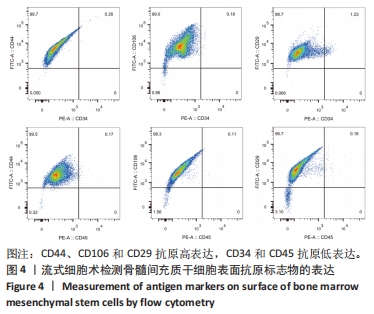
1.4.4 流式细胞仪检测细胞表面分子标志 将培养好的第2代BMSCs用0.25%胰蛋白酶消化,以300×g低速离心5 min,弃上清,用完全培养基重悬,计数,取1.0×109 L-1细胞(1 mL)于新的1.5 mL PE管中,300×g低速离心5 min,弃上清,用100 μL完全培养基重悬,按说明书分别加入相应抗体及同型对照(PE 及 FITC 荧光标记的 CD106、CD44、CD29、CD34、CD45抗小鼠抗体),避光孵育20 min,加入1.5 mL灭菌PBS 洗掉多余的流式抗体,1 400 r/min低速离心5 min,弃上清,用200 μL完全培养基重悬,200目尼龙网过滤,装入流式管中,上机检测。
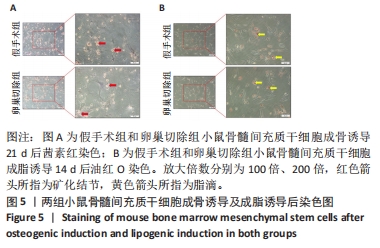
1.4.5 茜素红染色及油红O染色 将培养至第3代的BMSCs,按1.0×107 L-1细胞浓度加至6孔板内,每孔2 mL,置于37 ℃、体积分数5%CO2细胞孵育箱内培养。待细胞密度达底板85%时,弃去完全培养基,分别加入成骨和成脂诱导培养基并诱导培养21 d及14 d后,弃去诱导培养基,加入2 mL 40 g/L多聚甲醛溶液固定20 min,PBS轻缓冲洗去除多聚甲醛溶液,向成骨诱导组每孔中加入1.2 mL茜素红染液静置染色10 min,成脂诱导组每孔中加入1.5 mL油红O染液静置染色30 min,PBS轻缓冲洗去除残留染液,于光学显微镜下观察染色结果并拍照。
1.4.6 BMSCs的细胞因子抗体芯片检测 将培养好的第2代BMSCs用0.25%胰蛋白酶消化,以1 000 r/min低速离心5 min,重悬后计数使细胞浓度为3×109 L-1,将细胞悬液转移至1.5 mL冻存管中,以800 r/min低速离心5 min,弃上清液,转移至-80 ℃超低温冰箱中存储。假手术组和卵巢切除组均重复3个样本。采用BCA蛋白试剂盒按说明书操作提取样本中的总蛋白制备蛋白样本。利用细胞因子抗体芯片阵列对样品中的蛋白质初始氨基基团进行生物素化,封闭载玻片阵列,此过程类似于蛋白免疫印迹法,将生物素标记的样品添加到预先印有捕获抗体的载玻片上,载玻片孵育后将与靶蛋白结合,加入链霉亲和素偶联荧光染料(Cy3等效物),待载玻片干燥后使用激光荧光扫描获取可视化信号。
1.4.7 细胞因子抗体芯片数据分析
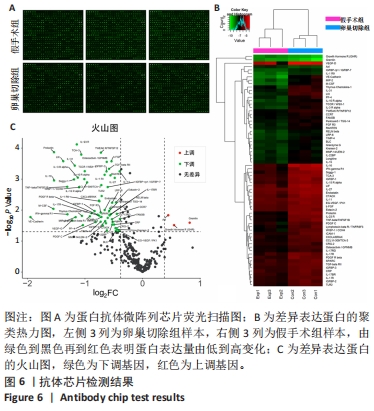
(1)聚类热力图及差异表达基因的分析:荧光检测后获得芯片扫描图,对扫描图结果进行计算机分析后得到荧光值,以荧光值作为原始值,通过原始值去除背景信号值获得修正值,以标准化方法通过阳参点做数据校正,得到标准值并以此结果的log2来绘制聚类热力图。蛋白聚类分析是根据样品蛋白表达谱的相近程度将蛋白进行聚类,直观展示蛋白在不同样品中的差异表达情况。其中横坐标为样本,纵坐标为差异蛋白,不同颜色表示不同的蛋白表达水平,颜色由绿色经黑色至红色表示表达量从低到高。
通过计算卵巢切除组与假手术组表达量标准值的比值获得差异倍数(fold change,FC)。FC反映样本之间同一个蛋白表达量的变化倍数,使用两独立样本t检验对两组之间的差异进行比较。依据FC值以及t检验的显著性水平,可将每一个基因分为以下3类:①上调基因:需满足FC≥1.3且 P < 0.05;②下调基因:需满足FC≤0.667且P < 0.05;③无差异基因:1/1.5 < FC < 1.5或P≥0.05。绘制火山图描述差异表达蛋白的整体分布情况。以 log2FC为横坐标,代表蛋白在两组样本中差异表达倍数的对数;-log10(P值)为纵坐标,代表蛋白表达量变化差异的统计学显著性。
(2)差异表达基因的GO及KEGG富集分析:通过芯片检测结果并查找NCBI数据库进行搜索分析得到样本蛋白对应的mRNA。借助R语言安装包“ChIPseeker”对富集峰进行注释;特定基因组区域的热图由deepTools绘制。通过GO富集分析找到差异mRNAs主要参与的功能途径及信号传导途径。mRNAs对应的GO注释分为3类:生物过程(biological process,BP)、细胞成分(cellar component,CC)和分子功能(molecular function,MF)。根据富集结果采用R语言绘制GO富集性饼图、柱状图以及气泡图。KEGG路径分析是将基因映射到KEGG途径的功能分析。通过KEGG数据库系统分析基因产物在细胞中的代谢途径以及这些基因产物的功能,采用的基本方法是超几何分布。KEGG富集性气泡图横轴表示富集因子,纵轴表示路径;气泡的面积越大,则富集的基因数越多;Rich Factor 表示位于该通路的差异基因数与位于该通路的总基因数的比值,其比值越大,则富集的程度越大。P值表示与条件相关途径的重要性,P值越小,则置信程度越高,说明该途径越有意义。矫正后的P值 < 0.05被认为差异有显著性意义。
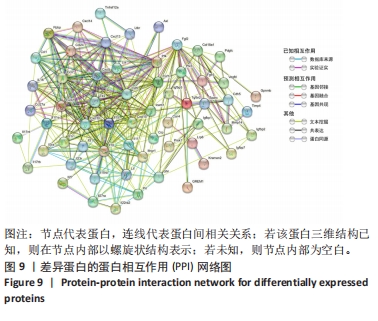
(3) PPI 网络的构建:通过String数据库(https://cn.string-db.org/)分析编码差异蛋白的mRNAs之间的相互作用,构建PPI网络。
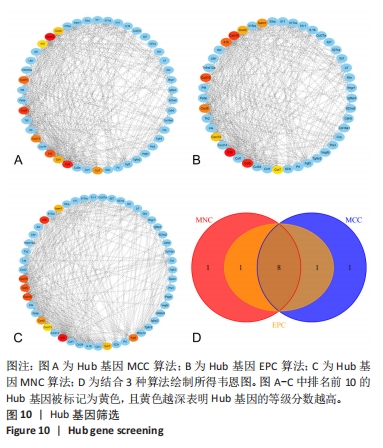
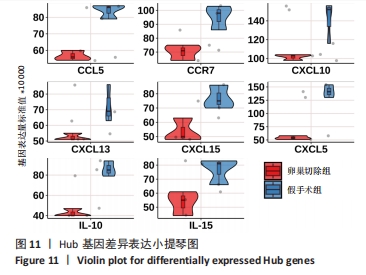
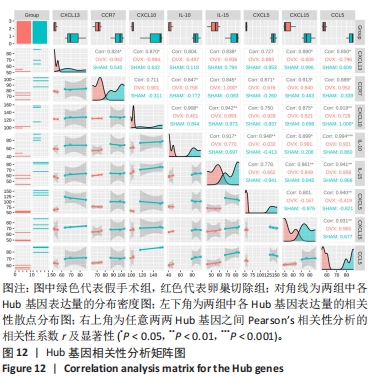
(4)关键Hub基因获取:通过cytoHubba(版本0.1)将PPI网络图所得数据进行Hub基因筛选,运用边缘渗透分量(edge permeability component,EPC)、最大邻域分量(maximum neighborhood component,MNC)及最大集团中心性(maximal clique centrality,MCC)分析算法得到各自排名前10的Hub基因,绘制韦恩图筛选出3种算法所得的共同Hub基因。对以上共同Hub基因绘制蛋白表达的小提琴图及相关性矩阵。
1.4.8 RT-qPCR检测关键因子的表达 第2代假手术组和卵巢切除组小鼠BMSCs样本用于检测GREM1 mRNA 的表达。根据Trizol说明书从样品中提取RNA,用RNA反转录试剂盒对样品RNA进行反转录为cDNA。将目的基因的引物序列(GREM1:5’-ATG AGA CGA AGT GGG GAG CT-3’: 3’-TTA CAG TGG GCA GGA GGA GT-5’;β-actin:5’-CTG GCA CCA CAC CTT CTA CA-3’: 3’-GGT ACG ACC AGA GGC ATA CA-5’)用qRT-PCR进行扩增反应,配置扩增反应体系,上qRT-PCR仪,设置条件:第1阶段(预变性):95 ℃ 5 min;第2阶段(变性):95 ℃ 10 s;第3阶段(退火):60 ℃,20 s;第4阶段(延伸):70 ℃,1-10 s;第2-4阶段反复循环40次。用2-ΔΔCt法计算基因表达的相对倍数。
1.5 主要观察指标 ①卵巢切除组与假手术组之间差异表达的基因筛选;②差异表达基因的GO及KEGG富集分析;③PPI蛋白互作网络分析及Hub基因筛选。
1.6 统计学分析 使用GraphPad Prism 8.0及R语言对数据进行统计分析,组间比较采用两独立样本t检验,以双尾 P < 0.05为差异有显著性意义;相关性矩阵采用Pearson’s相关性系数,以双尾P < 0.05为两组数据之间具有显著相关性,r取值介于-1至1之间,其绝对值越接近1表明相关性越强,当r取值为正时表明两组之间呈现正相关关系,当r取值为负时表明两组之间呈现负相关关系。数据均采用x±s形式进行描述。该文统计学方法已经通过遵义医科大学统计学专家审核。