1.1 设计 体外细胞观察对比性实验,两样本均数间的比较采用t检验;多个样本间的比较采用单因素方差分析(One-way ANOVA)。
1.2 时间及地点 实验于2020年9月至2021年12月在广西中医药大学科学实验中心分子生物学实验室完成。
1.3 材料
1.3.1 细胞株 HepG2细胞株购自上海赛百慷生物技术股份有限公司,货号为iCell-h092。
1.3.2 实验试剂 DMEM/F12培养基(上海源培生物,货号L310KJ);胎牛血清(美国Gemini公司,货号9001-108);流式抗体:CD133(美国BD公司,货号566593);干细胞消化液(美国Invitrogen公司,货号E129610);B27、N2、乳铁传递蛋白(美国Gibco公司,货号分别为17504-044、17502-048、
PHC9484);成纤维细胞生长因子、表皮生长因子(美国PEPROTECH公司,货号分别为AF-100-18B、AF-100-15B);反转录试剂盒(加拿大Fermentas公司,货号K1622);四甲基乙二胺、ECL发光液(上海赛默飞公司,货号分别为17919、OH188466A);GAPDH、NANOG、SOX2、OCT4一抗、鼠二抗、兔二抗(美国CST公司,货号分别为AF7021、4903s、3579s、2750s、8480s、4249);Polybrene(英国Abcam公司,货号40804ES76)。
1.3.3 实验仪器 HF-90型二氧化碳培养箱(中国香港Heal Force公司);超微量核酸测定仪、PCR仪、酶标仪(美国Thermo公司);3120000.216型微量移液器(德国Eppendrof公司);NU-C200R-E型离心机(中国香港天美公司);BD C6型流式仪器(美国BD FASAria Cell Sorter公司);DMi8型荧光显微镜(德国Leica公司);人CD133微磁珠试剂盒(德国Miltenyi Biotec公司);Trizol Reagent(美国Ambion公司);实时定量PCR仪(美国伯乐公司);4200型全自动化学发光图像分析系统、凝胶成像系统(上海Tanon科技)。
1.4 实验方法
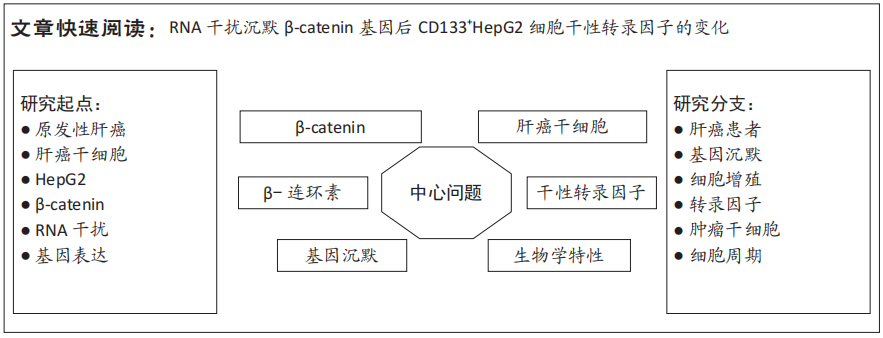
1.4.1 HepG2细胞的培养 将HepG2细胞接种于高糖DMEM培养液,置于37 ℃,体积分数为5% CO2培养箱中培养,隔日换液,观察细胞状态,待细胞贴壁比例大于80%,用0.25%胰蛋白酶消化细胞2 min,滴加DMEM培养液终止消化,于4 ℃、1 000 r/min低温离心机中离心5 min,弃上清,加入适量10%DMEM培养液,1∶3传代后继续培养。
1.4.2 磁珠分选 取培养至第3代对数生长期的HepG2细胞,用胰蛋白酶消化2 min,4 ℃、1 000 r/min低温离心5 min后收集细胞沉淀,用300 μL缓冲液制成细胞浓度为1×1011 L-1的细胞悬液,加入100 μL CD133磁珠,混匀后于2-8 ℃孵育30 min,4 ℃、1 000 r/min低温离心10 min,去除上清液,然后过柱分离得到CD133+HepG2细胞;最后用缓冲液进行洗脱,并分离柱上吸附的CD133+HepG2细胞,每日观察细胞状态并记录,培养3代后进行诱导。
1.4.3 CD133+HepG2细胞诱导 预配干细胞培养液:DMEM/F12+表皮生长因子(20 μg/L)+成纤维细胞生长因子(20 μg/L)+乳铁传递蛋白(10 μg/L)+ B27(1X)+ N2(1X);取足量对数生长期、分选后的CD133+HepG2细胞,换液,4 ℃、1 000 r/min低温离心5 min,用DMEM/F12培养液重悬,取10 μL细胞悬液滴于细胞计数板进行细胞总数测定,将细胞悬液浓度稀释至3×107 L-1,取100 μL接种于6孔培养板中(3 000个细胞/孔),每孔加入2 mL干细胞培养液,置于培养箱中继续培养,培养至细胞数达到108个进行流式鉴定。
1.4.4 流式鉴定 将筛选、诱导后的CD133+HepG2细胞用干细胞消化液(1 mL 0.25%胰酶+0.02%EDTA)消化2 min,1 000 r/min、4 ℃低温条件离心5 min后收集细胞,计数,制成细胞浓度为1×109 L-1细胞悬液;用预冷的PBS洗涤细胞2次,1 000 r/min、4 ℃低温条件离心5 min后弃上清,收集细胞沉淀,将500 μL 40 g/L多聚甲醛固定液加入Ep管中,吹打混匀并固定20 min,1 000 r/min、4 ℃低温条件离心5 min后收集细胞;继续PBS洗涤细胞1次,重复离心后弃上清,收集细胞沉淀,将500 μL 0.5% Triton X-100加入Ep管中破膜15 min,离心后收集细胞;再次PBS洗涤细胞1次,用100 μL含1%牛血清白蛋白的PBS重悬细胞,随后加入3 μL预冷的CD133流式抗体,混匀,4 ℃避光孵育30 min,PBS清洗2遍,上机鉴定。
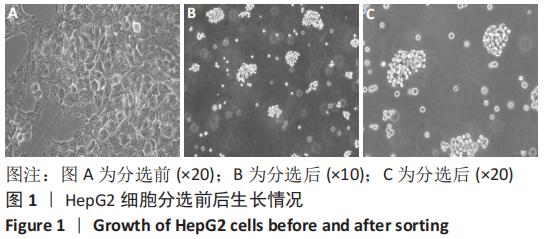
1.4.5 慢病毒包装、转染 借鉴杨丽兰[12]的实验方法,按照 RNA 干扰序列设计原则,由上海研集生物科技有限公司合成3条含干扰序列的双链DNA(β-catenin-RNAi-a:5’-GGT TAA TAA GGC TGC AGT TAT TTC AAG AGA ATA ACT GCA GCC TTA TTA ACC TTT TTT-3’;β-catenin-RNAi-b:5’-GCA TAA CCT TTC CCA TCA TTT CAA GAG AAT GAT GGG AAA GGT TAT GCT TTT TT-3’;β-catenin-RNAi-c:5’-GCT GAT CTT GGA CTT GAT ATT CAA GAG ATA TCA AGT CCA AGA TCA GCT TTT TT-3’),并连接在酶切后的RNA干扰载体上。将连接好的产物进行转化,对长出的克隆进行PCR鉴定,正确的克隆即为构建成功的目的基因RNA干扰慢病毒载体。严格按照慢病毒感染步骤,用DMEM完全培养基培养CD133+HepG2细胞至对数生长期,重悬于DMEM/F12培养基,细胞浓度为1×109 L-1,放入培养箱培养24 h,加入 60 μL聚凝胺,再加入50 μL慢病毒或者慢病毒空载体,继续培养72 h,荧光显微镜下观察绿色荧光蛋白的表达,以评估感染效率,并选取干扰能力最佳病毒备用。
1.4.6 细胞分组、干预 实验设置设空白对照组,病毒空载组,病毒干扰组。将CD133+HepG2细胞接种于6孔板中,每孔细胞数为1×106个,培养72 h后,空白对照组不做处理,病毒空载组稳定感染入shRNA慢病毒空载质粒,病毒干扰组稳定感染入β-catenin-shRNA慢病毒质粒。培养72 h显微镜下观察,感染效率评估达80%后,收集细胞沉淀,进行后续检测。
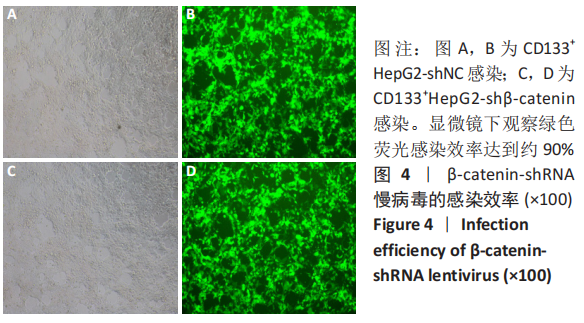
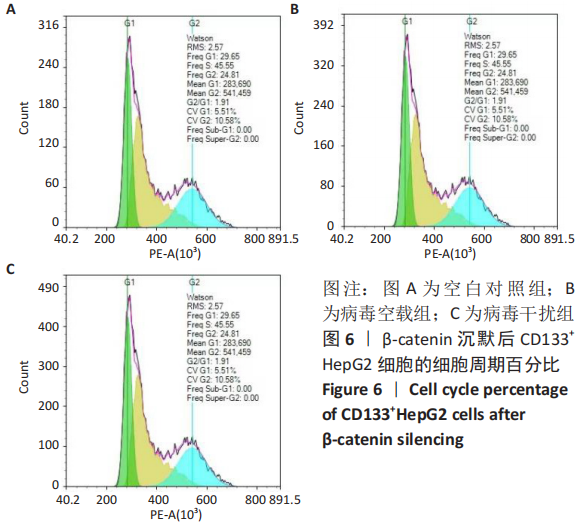
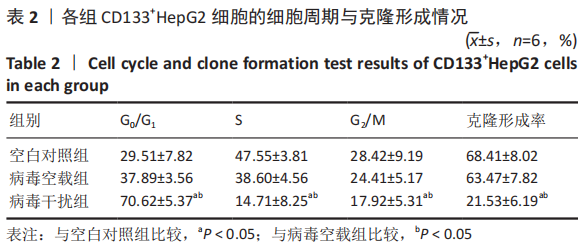
1.4.7 β-catenin沉默后CD133+HepG2细胞的增殖、细胞周期 将各组CD133+HepG2细胞接种于直径6 cm的培养皿中,每皿接种200个细胞,并加入5 mL DMEM/F12培养基充分混匀,置37 ℃,体积分数为5% CO2及饱和湿度的细胞培养箱中培养14 d,当培养皿中出现肉眼可见的克隆时,吸弃培养液,用PBS小心浸洗2次,加40 g/L多聚甲醛固定15 min,用流水缓慢洗去染色液,空气干燥,拍照记录。取各组处于对数生长期CD133+HepG2细胞,计数,制成细胞浓度为1×109 L-1的细胞悬液,收集于离心管中,400×g离心5 min,弃去培养液,加入1 mL PBS洗涤1次,400×g离心5 min,用DMEM/F12培养基重悬细胞,加入约1 mL无水乙醇固定细胞;加入100 μL的RNase A充分悬浮细胞,37 ℃水浴30 min,加入400 μL PI溶液充分混匀,4 ℃避光孵育30 min,上机检测。
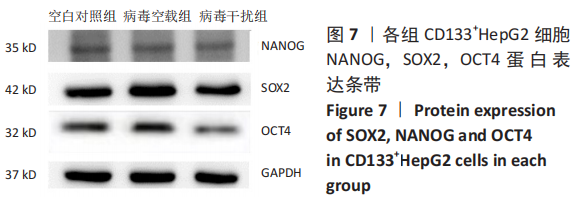
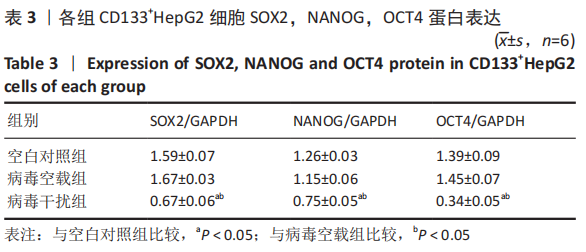
1.4.8 Western blot检测SOX2,NANOG,OCT4的蛋白表达 在各组细胞沉淀中加入RIPA裂解液(RIPA∶PMPF=100∶1),静置5 min,反复吹打,于4 ℃摇床上温和摇振15 min,收集蛋白,BCA法测蛋白浓度,酶标仪测定波长为562 nm的吸光度值,根据相应的标准曲线,计算待测样品的浓度及所需稀释的对应量;加入相应量的SDS-PAGE蛋白上样缓冲液,缓冲液∶蛋白体积=1∶4,混匀后于100 ℃变性8 min,取出后分装备用,制胶后以恒压80 V,30 min之后恒压120 V,60 min进行蛋白电泳,电泳结束后将PAGE胶从玻板上卸下,装配转膜三明治,恒流,350 mA转60 min,将蛋白转移到PVDF膜上;用封闭液(含5%脱脂奶粉的TBST溶液)室温封闭膜1 h;加入OCT4、NANOG、SOX2、GAPDH一抗(1∶1 000)室温孵育2 h,PBS洗涤3次,每次5 min;加入对应鼠二抗(1∶5 000)、兔二抗(1∶5 000)孵育,按1∶1比例混合显影液A液和B液,将混合液均匀滴加于PVDF膜上,反应60 s,放入化学发光成像仪中,曝光,并拍照记录。以GAPDH为参照,用Quantity One软件测量各蛋白条带平均吸光度值,计算SOX2,NANOG,OCT4的蛋白表达。
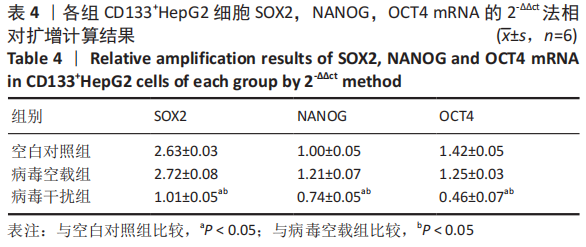
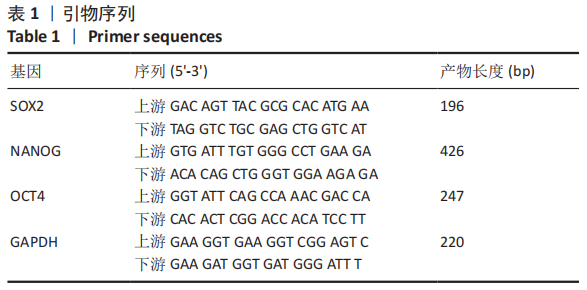
1.4.9 qRT-PCR检测SOX2,NANOG,OCT4的mRNA表达 Triol法提取各组细胞总RNA,使用miRcute Puls miRNA First-Strand cDNA Synthesis Kit试剂盒,将提取的RNA反转录为cDNA,应用qRT-PCR检测SOX2,NANOG,OCT4的mRNA表达。PCR扩增条件(反应体系为20 µL)为95 ℃反应5 min预变性,95 ℃反应10 s,60 ℃反应30 s,重复40次循环,采用2-ΔΔCt法计算mRNA的相对表达水平。引物序列具体信息见表1。
1.5 主要观察指标 ①CD133+HepG2细胞阳性率;②β-catenin-shRNA 慢病毒的封闭效果和感染效率;③β-catenin沉默后CD133+HepG2细胞的增殖情况、细胞周期以及SOX2,NANOG,OCT4的蛋白和mRNA表达水平。
1.6 统计学分析 利用SPSS 20.0软件进行统计学分析,利用Excel软件进行绘图。计量资料以x±s表示,两样本均数间的比较采用t检验;多个样本间的比较采用单因素方差分析(One-way ANOVA)。检验水准设定为α=0.05,当P < 0.05 时,差异有显著性意义。