1.1 设计 体外观察性实验。
1.2 时间及地点 实验于2019年3月至2020年3月在滨州医学院附属医院实验室完成。
1.3 材料 淫羊藿苷(上海如吉生物);聚己内酯(sigma,美国);扫描电镜(EVOLS15,Zeiss,德国);激光共聚焦显微镜(OLYMPUS,日本);CO2细胞培养箱(SANYO公司,日本);酶标仪(SpectraMax M2,MolecuLar Devices,美国);紫外-可见光分光光度计(NanoDrop2000,Thermo Fisher Scientific,美国);荧光实时定量 PCR 仪(Rotor-Gene 3000,Corbett,澳大利亚);α-MEM 培养液(Hyclone);CCK-8 检测试剂盒(碧云天);碱性磷酸酶检测试剂盒(碧云天);N,N-二甲基甲酰胺(国药试剂);三氯甲烷(国药试剂);反转录试剂盒(PrimeScriptTM RT reagent Kit with gDNA Eraser);PCR试剂盒(SYBR Premix ExTaqTM,Takara,日本)。
1.4 实验方法
1.4.1 细胞培养 向MC3T3-E1细胞(四川大学赠送)添加α-MEM 培养基(含体积分数10%胎牛血清、100 mg/L青霉素、100 mg/L链霉素),置于37 ℃、体积分数5%CO2 培养箱中培养,24 h冲洗换液,传代3次后备用。
1.4.2 静电纺丝纳米纤维膜的制备 使用移液枪在避光条件下吸取300 µL二甲基亚砜滴入无菌玻璃瓶内,加入淫羊藿苷粉末20 mg,吹打振荡使药物完全溶解;吸取10 µL上述溶液,使用α-MEM 培养基将淫羊藿苷稀释至10-5 mol/L, 4 ℃冰箱避光保存备用。
使用移液枪准确吸取7.5 mL三氯甲烷和2.5 mL N,N-二甲基甲酰胺滴入到无菌玻璃瓶内,加入聚己内酯2.4 g,置于常温磁力搅拌机搅拌24 h至聚己内酯全部溶解,直至溶液干净透亮,静置半小时。使用2个10 mL的注射器分别吸取10 mL淫羊藿苷溶液及10 mL聚己内酯溶液并将其固定在微量注射泵上,连接高压静电装置,通过聚氯乙烯管与9号针头(内径为 0.6 mm)相连,针头尖端直流高压电正极,平整锡箔纸固定于接收板上与高压电的负极相连同时将导线接地,设定参数:流速为 3 mL/h,高压电压为(25.0±0.5) kV,接收距离为 15 cm,在室温和相对湿度60%湿度条件下制备淫羊藿苷/聚己内酯纳米纤维膜。同样的环境下制备单纯聚己内酯纳米纤维膜。完成后将锡箔纸置于真空干燥箱内 24 h,小心取下即获得静电纺丝纳米纤维薄膜。
1.4.3 纳米纤维膜微观形貌 将淫羊藿苷/聚己内酯纳米纤维膜裁剪成10 mm×10 mm样本,用导电胶将其固定在观测台上,喷金60 s后扫描电镜观察孔径并计算统计纤维平均直径。
1.4.4 淫羊藿苷/聚己内酯纳米纤维膜体外释药实验 避光下称取淫羊藿苷10 mg,添加150 µL DMSO彻底溶解,用无菌PBS稀释至100 mL。使用移液器分别取0.2,0.4,0.8,1.0,2.0,3.0 mL淫羊藿苷溶液放置在6个试管中,PBS定容到20 mL,作为标准浓度,使用紫外分光光度计测定标准吸光度值A270 nm。
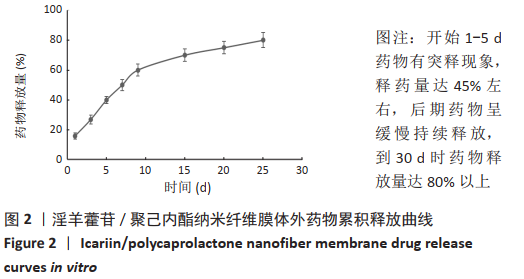
将淫羊藿苷/聚己内酯纳米纤维膜紫外线照射消毒1 h,置入含40 mL无菌PBS的密闭容器中,37 ℃恒温水浴箱振荡(100 r/min)。在第1,3,5,7,9,15,20,25,30天的同一时间点分别取出5 mL纤维膜释放液于离心管中,4 ℃恒温保存备用,同时向原溶液中注入5 mL PBS以保证原容积不变。紫外分光光度计分别测试释放液吸光度值A270 nm,测算其药物释放浓度。每组样本重复3次,取平均值作为最终药物释放量,绘制累积药物释放曲线。
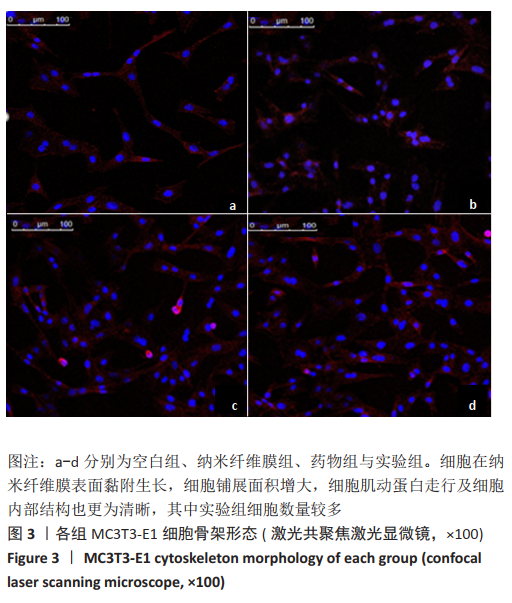
1.4.5 激光共聚焦显微镜观察细胞形态 将淫羊藿苷/聚己内酯纳米纤维膜紫外线照射消毒1 h,置于24孔板中,接种细胞浓度为5×107 L-1的细胞爬片,每孔加入1 mL细胞悬液,分4组:空白组常规培养细胞,纳米纤维膜组加入聚己内酯纳米纤维膜,药物组加入含10-5 mol/L淫羊藿苷的培养基,实验组加入淫羊藿苷/聚己内酯纳米纤维膜。恒温箱静置培育 24 h,吸净培养液,使用37 ℃预热PBS清洗3次,40 g/L多聚甲醛固定10 min,PBS复洗3次,每次10 min。取100 nmol/L的罗丹明-鬼笔环肽 200 μL覆盖爬片上的细胞,室温避光孵育30 min,PBS冲洗3次,每次5 min,抗荧光猝灭封固,激光扫描共聚焦显微镜观察细胞三维骨架形态。
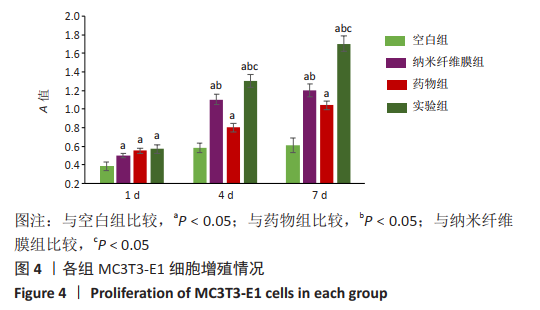
1.4.6 细胞增殖检测 将淫羊藿苷/聚己内酯纤维膜紫外线照射消毒1 h,置于96孔板中备用。选取处于对数生长期的MC3T3-E1细胞,以5×107 L-1的细胞浓度接种于96孔板内,每孔100 μL,按照1.4.5分组处理,每组设置5个复孔。培养 1,4,7 d 时,每孔加入10 μL CCK-8 混合液孵育1 h,用酶标仪于450 nm 波长测定吸光度值。
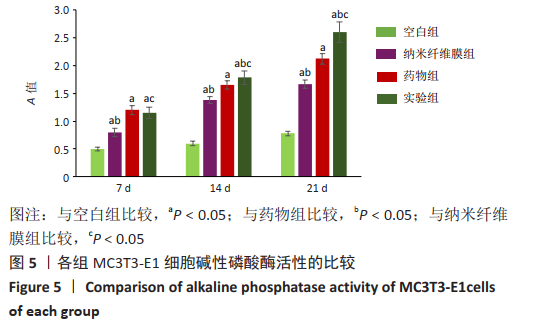
1.4.7 碱性磷酸酶活性检测 将淫羊藿苷/聚己内酯纳米纤维膜紫外照射消毒,置于6孔板中备用。将MC3T3-E1细胞以5×107 L-1的细胞浓度接种于6孔板内,每孔1 mL,按照1.4.5分组处理,每组设置3个复孔。培养24 h细胞贴壁后,空白组、纳米纤维膜组、实验组更换为成骨诱导液(含a-MEM培养液、1.0 mmol/L β-甘油磷酸钠、0.05 mmol/L维生素C和100 mmol/L地塞米松),单纯药物组更换为含10-5 mol/L淫羊藿苷的成骨诱导液。诱导培养 7,14,21 d后弃原培养液,每孔加入200 μL细胞裂解液,充分裂解后收集细胞,离心后取上清,按碱性磷酸酶试剂盒说明书进行操作,酶标仪测定 405 nm处的吸光度值。
1.4.8 RT-qPCR 检测细胞骨钙素mRNA表达 将MC3T3-E1细胞以3×107 L-1的细胞浓度接种于6孔板内,每孔2 mL,按照1.4.5分组处理,每组设置3个平行复孔。培养24 h细胞贴壁后,空白组、纳米纤维膜组、实验组更换为成骨诱导液(含a-MEM培养液、1.0 mmol/L β-甘油磷酸钠、0.05 mmol/L维生素C和100 mmol/L地塞米松),单纯药物组更换为含10-5 mol/L淫羊藿苷的成骨诱导液。诱导7 d后提取各组细胞总RNA,分光光度计检测总RNA纯度,结果显示各组A260 nm/A280 nm值均在1.7-2.1之间,说明其纯度较高,参照反转录说明书合成 cDNA。内参GADPH及骨钙素引物的合成,见表1。

RT-qPCR 反应采用荧光染料法(参照 SYBR Premix Ex Taq说明),反应条件为:95 ℃预变性30 s,1个循环;95 ℃变性
5 s,60 ℃退火30 s,45个循环。选择20 μL 体系:SYBRⅡ
10 μL,上游引物、下游引物各 0.8 μL,RT反应液1.6 μL,DEPC水6.8 μL。收集荧光信号进行分析,使用荧光阈值表示RT-qPCR 结果,定义空白组基因表达量为 1,根据公式(2-∆∆Ct)计算目的基因表达量,获得每组基因的相对表达量。
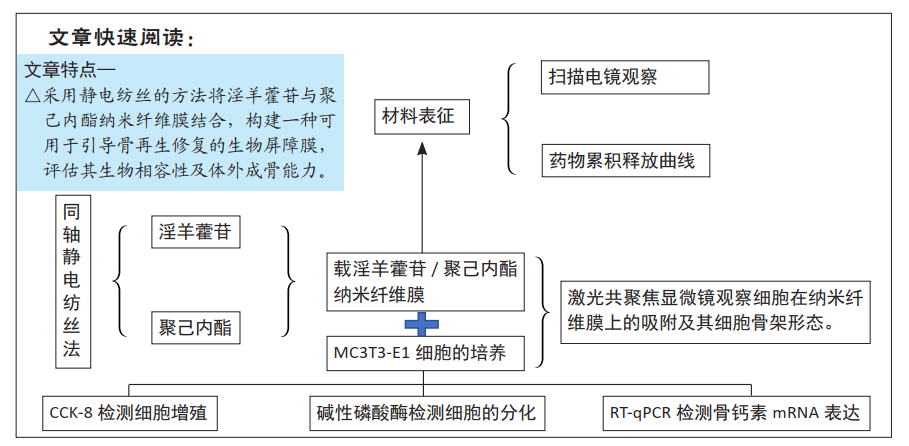
1.5 主要观察指标 淫羊藿苷/聚己内酯纳米纤维膜的微观形貌、药物累积释放曲线,以及对MC3T3-E1细胞增殖与分化的影响。
1.6 统计学分析 采用 SPSS 21.0 软件进行统计学分析,数据采用x±s 表示。组间差异比较采用单因素方差分析,实验组组间两两比较采用 t 检验,以 P < 0.05 为差异有显著性意义。