中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (29): 4619-4625.doi: 10.12307/2021.159
• 肌肉肌腱韧带组织构建 tissue construction of the muscle, tendon and ligament • 上一篇 下一篇
高强度跳跃肌腱损伤即刻冷水浸没干预模型兔髌腱组织内的炎症反应和胶原重塑
王 博1,白胜超2,李文博3,王 琳4
- 1北京体育大学,北京市 100084;2南京理工大学体育部,江苏省南京市 210014;3河北北方学院,河北省张家口市 075000;4北京体育大学运动医学教研室,北京市 100084
A rabbit model of high-intensity jumping-induced tendon injury followed by post-exercise cold water immersion: inflammations and collagen remodeling in the patellar tendon
Wang Bo1, Bai Shengchao2, Li Wenbo3, Wang Lin4
- 1Beijing Sport University, Beijing 100084, China; 2Department of Sports, Nanjing University of Science and Technology, Nanjing 210014, Jiangsu Province, China; 3Hebei North University, Zhangjiakou 075000, Hebei Province, China; 4Department of Sports Medicine, Beijing Sport University, Beijing 100084, China
Wang Bo, PhD, Lecturer, Beijing Sport University, Beijing 100084, China
摘要:
文题释义:
髌腱退行性病变:为一种常见的运动损伤,常见于田径以及篮排球运动员等,主要的损伤表现为跑步跳跃疼痛、膝关节水肿等症状,其中炎症反应以及组织修复是导致损伤的主要原因。
冷水浸没:是常用的运动后疲劳放松方法,通过对局部或者全身进行冷水浸没达到缓解运动疲劳、消除炎症反应的目的。
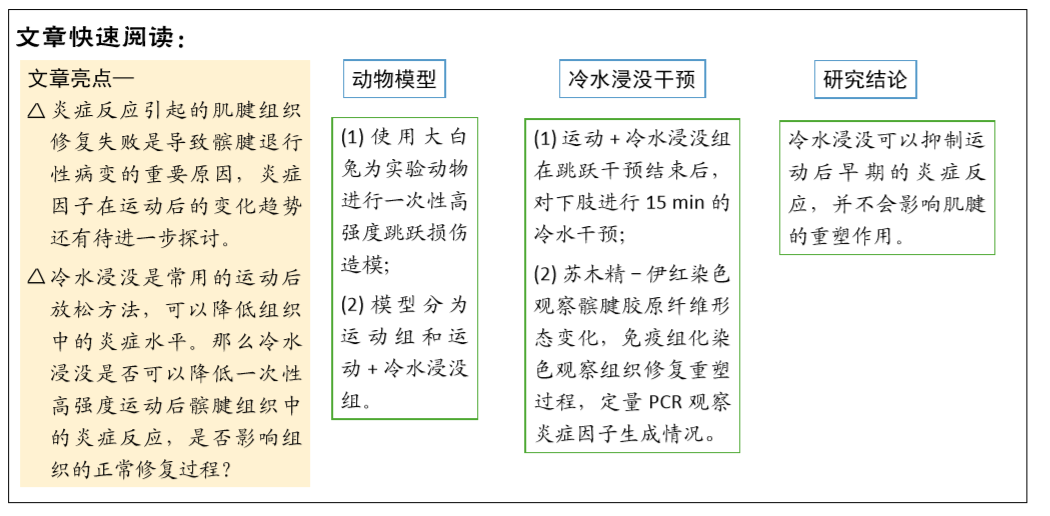
背景:髌腱退行性病变是常见的运动损伤,长期跑步和跳跃运动是导致损伤的重要因素。冷水浸没是一种常见的处理运动后炎症反应的方法,可以减慢局部血流速度,减慢局部代谢反应,从而减轻炎症反应。
目的:观察冷水浸没干预对大强度跳跃运动后髌腱中炎症和重塑修复的影响。
方法:选择30只雌性成年兔,体质量3.0 kg,其中安静对照组6只;其余24只兔右腿定为运动组,左腿定为运动+冷水浸没组,并在冷水浸没后0,6,24,48 h每个时间点挑出6只兔进行实验。兔需要一次性完成150次跳跃,每次80-120 N,跳跃10次间隔2 min,跳跃50次间隔10 min,随后立即在4 ℃冷水中进行15 min的冷水浸没干预,并按照分组在冷水浸没后0,6,24,48 h对肌腱和股直肌进行取材。采用相对定量PCR测定白细胞介素1β、肿瘤坏死因子α、环氧化酶2、基质金属蛋白酶1 mRNA在肌腱组织中的表达,以免疫组化染色测定肌腱中Ⅰ/Ⅲ型胶原蛋白、转化生长因子β蛋白的表达水平,采用苏木精-伊红染色观察肌腱中胶原纤维的变化。
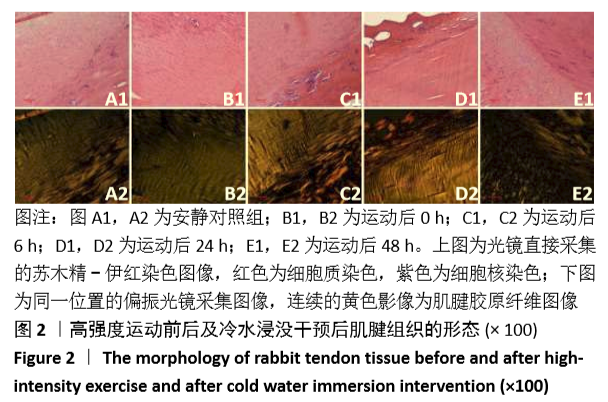
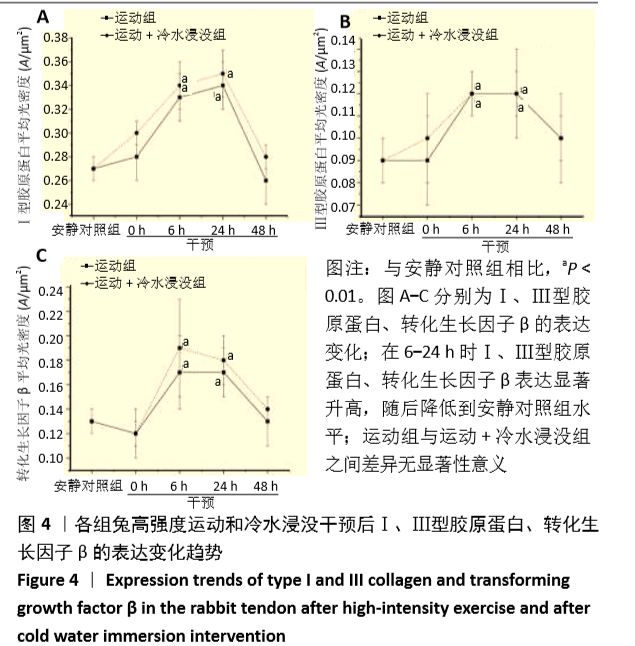
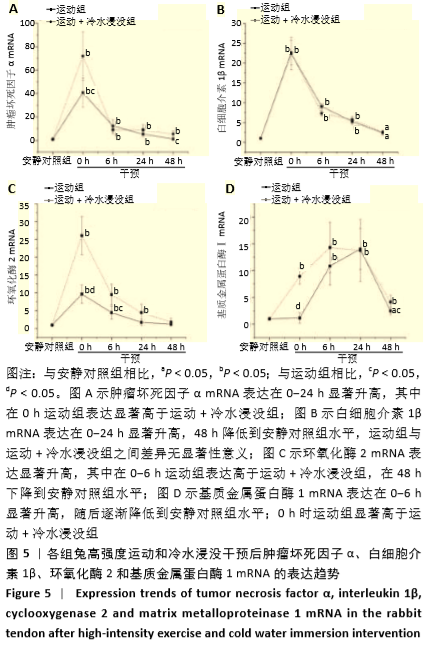
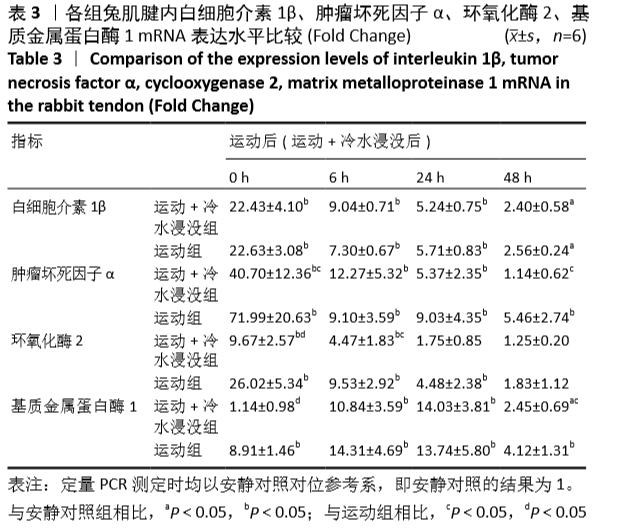
结果与结论:①白细胞介素1β的mRNA表达水平在0-24 h出现显著升高,运动+冷水浸没和运动组之间没有区别;②肿瘤坏死因子α mRNA表达水平显著升高,0 h运动组的mRNA表达水平高于运动+冷水浸没组(P < 0.05);③环氧化酶2 mRNA表达水平在0-24 h显著升高,运动组在0-6 h的表达水平高于运动+冷水浸没组(P < 0.05);④基质金属蛋白酶1 mRNA表达水平显著升高,0 h运动组的mRNA表达水平高于运动+冷水浸没组(P < 0.05);⑤ Ⅰ/Ⅲ型胶原蛋白、转化生长因子β在6-24 h表达显著升高,运动组与运动+冷水浸没组之间差异无显著性意义;⑥苏木精-伊红染色结果显示,运动后0-24 h肌腱胶原纤维排列出现紊乱,胶原纤维排列在运动后48 h基本恢复到运动前状态;运动组和运动+冷水浸没组在组织形态上无明显差异;⑦提示冷水浸没可以抑制运动后早期的炎症反应,并不会影响肌腱的重塑作用。
https://orcid.org/0000-0003-1299-0382 (王博)
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
中图分类号: