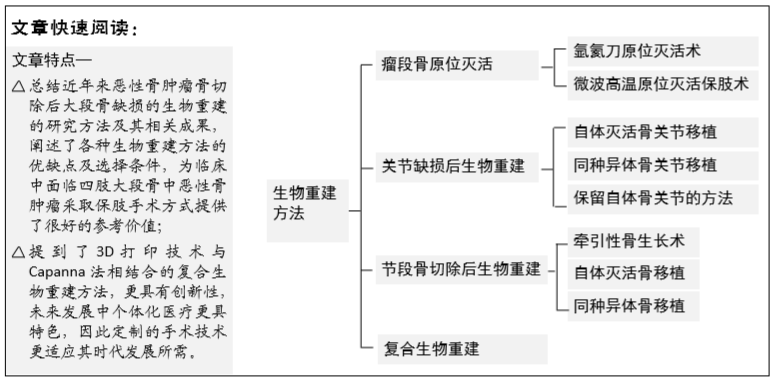
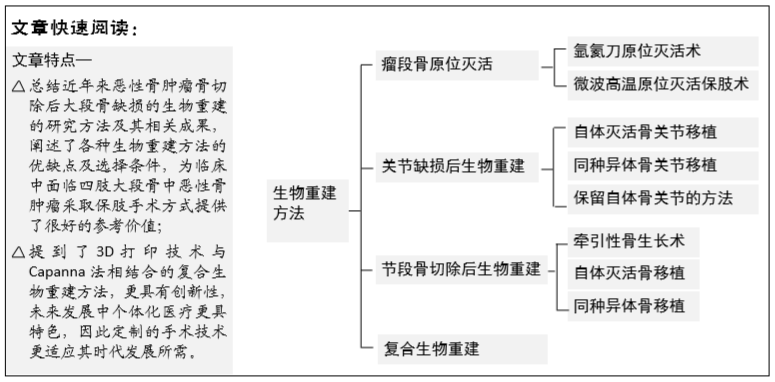
2.1 瘤段骨原位灭活 主要采取以下2种方法,瘤段骨性原位灭活后,再次以内固定方式将骨段植入缺损部位。
2.1.1 氩氦刀原位灭活术 氩氦刀原位灭活术是冷冻外科治疗骨肿瘤的新型方法,是以氩气-氦气为媒介的冷冻外科手术设备为基础,对无法进行手术切除的晚期肿瘤进行原位治疗。作用机制为:①氩氦刀在肿瘤细胞内外迅速形成冰晶,引起其结构破坏,导致细胞死亡,并在靶区微小血管内形成冰晶及微血栓,对周围病灶有治疗作用[6];②因热池效应,氩氦刀不会损伤大血管[7];③具有抗肿瘤免疫作用,肿瘤细胞坏死后所分泌的免疫抑制因子减少,坏死的原位肿瘤细胞可成为肿瘤抗原,可增强免疫[8]。
2.1.2 微波高温原位灭活保肢术 1992年范靖宇等[9]开展了微波高温原位灭活法治疗骨肿瘤,经多年随访数据,该方法无论在肿瘤学结果或是功能学结果方面都有明显优点。
具体方法[9]:①首先将瘤段骨与周围正常组织分离,瘤体表面留一薄层正常组织,以保证肿瘤手术特有的安全界限,同时保留临近关节的完整连续性;②瘤段骨中均匀插入微波天线阵列,同时严密保护正常组织并注意严格的无瘤操作防止肿瘤血液污染正常组织;③将研制的频率为2 450 MHz的微波治疗机输入肿瘤组织使瘤段骨组织升温,其表面温度达50 ℃,中心温度最高可达108 ℃,至少持续30 min,同时使用循环降温系统保证周围正常组织不受高温影响;④刮除微波灭活的肿瘤组织及周围坏死组织;⑤根据骨质的坚固程度分别采用自体骨、同种异体骨、同种异体骨基质粒复合骨水泥或吻合血管的自体骨移植加固灭活后的瘤段骨结构;⑥适当的软组织覆盖。
瘤段骨原位灭活治疗的优点:①氩氦刀有减轻肿瘤负荷、减少肿瘤产生的肿瘤免疫抑制因子,术后应激反应轻、机体免疫抑制小和坏死原位肿瘤抗原释放后可刺激机体免疫功能等外科手术治疗所不具备的优点;②微波原位灭活只做肿瘤的原位分离(包括重要的血管神经束和未被侵犯的肌肉),而不破坏骨关节内外结构,可最大限度保留邻近关节功能,无松动及高度退行性变等远期并发症。在范靖宇等[9]的研究中,经此方法治疗的309例患者,3年以上存活率为60.2%,多数患者肢体功能得以保留。
瘤段骨原位灭活治疗的缺点:①若肿瘤对骨破坏严重,瘤段骨原位治疗有明显手术指征限制;②原位灭活有可能残余存活的肿瘤组织,有复发风险;③受侵袭的瘤段骨生物力学强度不足,易发生骨折等并发症。
2.2 关节缺损后生物重建 恶性骨肿瘤侵袭关节所导致的关节缺损生物重建,通常采取以下3种方法:
2.2.1 自体灭活骨关节移植 对于自体侵蚀程度不高的骨关节可行自体灭活骨关节移植。将瘤段骨与周围组织按照肿瘤手术安全界限与周围软组织进行分离后,将肿瘤行刮除术,将肿瘤组织去除后,再用放射线、液氮等方法对其进行灭活后,植入原位。
自体灭活骨关节移植的优点:关节为自体关节,解剖位置对位及瘤段骨力线正确,可以为周围软组织提供正确的韧带与肌腱附丽点,术后愈合更牢固,日后更有利于患者的肢体功能康复。
自体灭活骨关节移植的缺点:①恶性骨肉瘤对关节侵蚀范围大,若破骨范围太大,失去骨关节必须存在的支撑点及附着面,再行瘤段骨灭活后,关节强度降低,此为该方法的明显的手术指征限制;②放射线灭活处理之后,自体骨关节生物力学及力学强度不够,远期易出现关节面的塌陷、韧带及肌腱附着点正常关系破坏,患侧关节将会失去功能[10]。
2.2.2 同种异体骨关节移植 1908年LEXER最早实施肿瘤切除后的异体骨关节移植术[11]。20世纪60年代,OTTOLENGHI、PARRISH、VOLKOV等报道了大块异体骨关节移植的临床结果,手术效果良好。同种异体骨关节移植的适应证基本与保肢手术所要求的Enneking分期一致,同种异体骨关节的来源主要是死亡供体,其次为活体供骨。经过深冻、冻干、脱钙、脱脂、灭菌等处理后,采取深低温冷冻法储存供骨。杨克强等[12]的试验证明,深低温冷冻法储存供体骨,皮质骨的生物力学特性受储存时间长短影响不显著。主要方法为:取骨库超低温冷存的同种同侧同名异体骨关节,快速复温后,截取与瘤段骨等长的一段移植到缺损部位。为使同种异体骨关节移植成功,需完全去除骨干的软组织,尤其是半关节置换,在靠近关节缺损部位的骨外膜留为袖状,关节囊适当留宽,便于植入时与相应结构吻合,使重建关节尽可能稳定。
同种异体骨移植关节的优点:①形状符合,可提供肌肉、韧带和关节囊附丽点[13];②由于常使用冷冻储存,复温后可维持原有生物力学特性,产生骨诱导作用。有研究表明,异体骨复合自体干细胞、人重组骨形态发生蛋白2可促进移植骨与宿主之间的融合[14],在骨端获得牢靠的生物愈合,因而软组织更易得到可靠的生物力学要求,与人工假体相比,其远期功能较好。
同种异体骨移植关节的缺点:①因关节面各附着点需良好匹配,而同种异体骨关节会存在匹配不佳情况,且需要医院配有数字化骨库或有大量异体骨来源方可匹配正确的关节面;②如果肌肉、韧带附丽点不好,远期可导致关节不稳,软组织及肌肉强度不佳,关节活动度及肢体功能锻炼明显受限;③骨库一般储存为成人骨,儿童同种异体骨关节来源十分受限。④同种异体骨关节通过处理后,也会出现移植骨-宿主愈合不良、切口感染、骨不连等并发症。
2.2.3 保留自体骨关节的方法 近期LI等[15]率先进行了保留自体骨关节的方法,该方法结合以氩氦刀为基础的冷冻消融术与异体骨复合生物重建,报道中12例近关节骨肉瘤患者在术前均进行了新辅助化疗。具体方法为:借助氩氦刀设备,将2-4根探针按照肿瘤边界深入关节面1.5-3.0 cm不等,依靠高压循环氩气产生超低温-150 ℃,冷冻持续10 min,之后通过相同的管道缓慢循环氦气,产生35 ℃温度进行消融,整个冷冻消融共进行3个循环。冷冻消融后对瘤段骨进行完整切除,保留骺端1.1-1.5 cm,使用与之相配的同种异体骨与自体带血管蒂游离腓骨进行复合重建。
该方法的优点:①保留关节与所属关节韧带,有很好的功能支持。在LI等[15]的研究中,术后对关节进行功能评分,整体美国骨骼肌肉肿瘤协会功能评分为92.7%;②使用的带血管蒂游离腓骨瓣,既提供了成骨性组织结构,从而促进了同种异体骨与宿主骨之间的愈合,报道中的12例均实现了骨愈合,又可以对保留的骺端产生机械性支持,促进骺端血供重建,此外,该报道中没有因骨坏死所导致的骨折。
该方法的缺点[15]:①组织学证据不足以证明保留部分是否残余肿瘤组织;②若过度冷冻消融,会导致保留的骺端局部缺血坏死。因此,术后随访很重要,以确定适合患者的方法,尽可能保留更多具有功能的正常骨与关节。
2.3 节段骨切除后生物重建 对于四肢节段骨的恶性骨肿瘤,肿瘤切除后导致大段骨缺损,通常采用以下几种方法进行骨肿瘤切除后的生物重建。
2.3.1 牵引性骨生长术 TSUCHIYA等[16]根据Ilizarov张力-应力原则,利用外固定架进行缓慢牵拉可增加局部组织的代谢活跃度,刺激延长区的细胞增殖和生物合成功能,进而在延长区域出现生长带、骨小梁,并促进延长区与周围的血液循环,使周围软组织、肌腱及皮肤等组织均呈现增长的改变,从而肢体一定程度上得到延长。牵引性骨生长的手术方法,在近关节处骨肿瘤切除后的节段骨重建中有广泛应用[17]。
各种因素影响下,牵引性骨生长术有不同方法,根据手术方法分为牵引性骨生长技术(包括骨搬移术和骨延长术)和加髓内钉的改良型方法;根据肿瘤所侵袭部位不同分为骨干重建、干骺端重建、骺部重建、关节下重建和关节固定术。术者应按需选择不同方法。
在TSUCHIYA等[16]的报道中,作者对19例患者行牵引性骨生长术,包括10例患者行骨搬移术,其中5例骨肉瘤,5例骨巨细胞瘤;3例行骨牵引术,其中2例骨肉瘤,1例Ewing’s肉瘤;6例行加髓内钉改良方法术,其中3例骨肉瘤,2例软骨肉瘤,1例未分化多形性肉瘤。平均切除长度为8.4 cm,骨搬移术组平均外固定器参数为39.5 d/cm(d/cm 代表延长1 cm平均需要多少天),骨牵引术组为34.1 d/cm,加髓内钉改良组为24.0 d/cm;术后12例患者功能评估为很好,5例为良好,2例为中等。
牵引性骨生长的优点:①虽然牵引性骨生长治疗恶性骨肿瘤会发生不同类型并发症,患者可能经历手术较多,时间较长,但患者通过牵引性骨生长能获得生物愈合。TSUCHIYA等[16]研究显示,对符合牵引性骨生长术手术标准的患者,这种方法可以有效提供持久的生物力学功能,并可有效治疗骨肿瘤及手术所导致的双腿长度不等的并发症,对发育中的儿童更有利。②无假体置换术后松动等机械性并发症,患者远期预后较好。当然,在治疗中需严格把握其适应证:对化疗敏感,且肿瘤切除后可留有足够长度牢固固定外固定架。
牵引性骨生长的缺点:①因需要使用外固定架辅助牵引伸长缺损部位,牵引两端固定钢针,容易出现针道感染,影响愈合,因而在术后日常护理中应每天使用酒精擦拭针眼处,保证其干燥,无渗出液附着[18];②行骨搬移过程中,存在出现骨缺损两端轴性偏移风险,因此需确保外固定架的稳定性,其连杆应平行于长骨的解剖纵轴,螺钉需于长骨的纵轴垂直、且需平行关节面;③牵引时间长,且在牵拉过程中引起局部软组织张力增大,造成患肢剧烈疼痛,患者较为痛苦;④可能并发骨不愈合,导致骨生物力学强度不足,影响患肢功能。
2.3.2 自体灭活骨移植 瘤段骨切除后,由于骨库不健全、传染病和地方宗教信仰等问题存在,同种异体骨在一些亚洲国家很难获取[19],因此结构尚好的自体骨被广泛再利用。在自体灭活骨移植中,首先行肿瘤与软组织整体切除,采用刮除术对瘤段骨进行处理。之后采取以下几种方法进行自体骨灭活处理。
(1)液氮法:TSUCHIYA等 [20]报道了使用液氮灭活自体骨再移植。瘤段骨置于-196 ℃液氮中冷冻20 min后,监测瘤段骨表面和髓腔温度达到-60 ℃,如未达到此温度,延长浸泡至30 min,置于室温复温15 min,再于蒸馏水中复温10 min后,将瘤段骨重新归位,采取髓内钉或钢板固定,必要时可以用骨水泥固定。国内外学者普遍认为液氮冻融的温度差对肿瘤细胞的杀伤力很强,研究显示,冷冻的杀伤深度可达3 cm[21]。冷冻消融后,瘤段骨彻底变成死骨,其复发率较低。液氮灭活,另一优势在于具有冷冻免疫效果,可以抑制肿瘤生长因子。YAMAMOTO等[22]将瘤段骨置于液氮中20 min后,取肿瘤组织,将其植入无胸腺小鼠体内,并没有肿瘤再生长现象。
(2)无水酒精法:将截除瘤段骨贯通髓腔,预先制备拟固定方式的螺钉孔道,以 99%酒精灭活 30 min,将骨水泥加压注入灭活骨内,安装内固定,并与关节面固定[23]。内固定方式可选择髓内钉或钢板,必须在放置骨水泥之前预制螺钉孔道。无水酒精杀灭肿瘤的病理生理机制研究证实,酒精灭活后仅骨表面和髓腔内薄层组织变性坏死,蛋白凝固,瘤段骨的肿瘤细胞在这一隔绝状态下4 d内死亡,而新生血管的生成需要7 d以上的时间[24]。
(3)巴氏法:应用巴氏法灭活瘤段骨最早于1991年由INOKUCHI等[25]报道,具体操作是将灭活骨置于65 ℃,保持30 min。有学者指出可将温度提高,时间缩短,以保留更多骨内蛋白的活性。北京大学人民医院使用改良的巴氏法,即将瘤段骨置于65 ℃的10%-20%的高渗盐水中浸泡30 min,与常规巴氏法相比,高渗盐水的渗透压使肿瘤杀伤率进一步提高,局部复发率随之降低。高渗盐水对骨内活性蛋白结构存在一定保护作用,更能促进骨愈合,骨强度恢复快[26-27]。
(4)高压蒸汽法:瘤段骨高压蒸汽130 ℃中处理8 min,样本在抗生素与生理盐水的混合液中浸泡5 min,再植入宿主内,并用钢板固定[28]。高压蒸汽灭活对骨活性蛋白的损伤很大,导致术后骨折、断端不愈合等并发症的发生率很高,现较少使用。高压蒸汽灭活骨再植后肿瘤的复发率为5%-20%,不愈合率为5%-30%,机械并发症发生率为5.3%-20.0%[29]。
(5)放射法:瘤段骨浸透在万古霉素液中处理后,用纱布包裹置于无菌袋,放入聚甲基丙烯酸酯的盒子后开始放射处理,对于放疗敏感的(例如尤文氏瘤)用70 Gy照射,对于放射不敏感的(例如骨肉瘤、梭形细胞瘤等)则用90 Gy,持续30 min[30]。根据CASEY等[28]关于MSKCC(凯特琳癌症中心)109例成人尤文氏瘤的治疗显示,现代化放射设备治疗对于肿瘤患者中位生存期有所提高,并不局限于成人,对儿童同样有作用。
自体灭活骨移植的优点:①自体瘤段骨灭活再植在免疫学及解剖结构上与宿主骨十分匹配,保留了肌腱和韧带及其正常的附着点,符合正常的解剖关系,较假体置换价格低廉,同时这种生物固定技术的远期并发症远低于现有的假体置换术。在没有大型异体骨骨库、假体又相对昂贵的时候,植入灭活骨是一种适合中国国情的重要重建方式[26]。②组织相容性好,保留了骨内活性蛋白及骨诱导因子,具有骨诱导和骨传导的作用,可促进灭活端骨折愈合,其愈合后缺损部位生物力学强度好,感染较少。
自体灭活骨移植的缺点:①伤口愈合延迟和感染是灭活后再植最常见的早期并发症,主要由于其手术时间的加长,术中存在诸多不可控环节,如浸泡、照射及高压锅处理等;②肿瘤复发:由于处理时间并非适合所有患者、所有肿瘤,存在将部分肿瘤组织残留于肿瘤周围软组织、血管神经及瘤段骨中,导致复发;③机械并发症和关节退变:处理时间过长,会使相应软骨软化,导致临近关节出现关节松弛[31];并会破坏正常骨组织,损伤正常骨组织强度,导致出现其机械并发症(即内固定和灭活骨发生折断、松动等情况);④愈合延迟和不愈合:随着肿瘤杀伤强度增加,不愈合也将明显增加,因而适当把握灭活过程的时间及各项指标。⑤如上文所述,节段骨缺损中,自体灭活骨会出现瘤段骨原位治疗中的问题。
2.3.3 同种异体骨移植 自体骨灭活骨移植有其优势,但由于一些条件限制,需采取异体骨移植。处理异体骨,一般采用冷冻法。异体骨由骨库制备,置于-80 ℃深低温冰箱保存。切除瘤段骨后,将术前选好的异体骨放入50-60 ℃温水中复温15-20 min,尽量刮除髓腔脂肪,用体积分数75%乙醇浸泡30 min脱脂后,用生理盐水反复冲洗,修剪多余软组织,保留用于重建肌肉、韧带的附丽点[32]。
灭活处理后,根据缺损部位长度、大小等截取移植骨,植入缺损部位。一般采取钢板和髓内钉固定,必要时用骨水泥辅助固定。
同种异体骨移植的优点:①规范化数字化骨库建立下,通过一定选配方法,可挑选匹配良好的植骨材料[13];②异体骨可提供存活组织的再生骨架、正常形态附着面,允许肌肉、肌腱及韧带等再连接,维持组织的结构完整;③对于儿童的保肢手术,因患儿生长需求,可行保留骨骺的保肢手术,采用大段同种异体骨移植修复肿瘤切除后的大块骨缺损,临床随访结果显示可使患儿获得较好的肢体功能。
同种异体骨移植的缺点:①人类HLA染色体复合物决定组织相容性,相容性较差会出现严重排异;②骨折是重要并发症,主要取决于肿瘤性质、肿瘤部位、手术操作、化疗影响因素和异体骨再血管化等因素;③异体骨与宿主骨愈合缓慢,出现一系列并发症,ORTIZ-CRUZ等[33]的报道中,共108例患者用大段异体骨移植治疗,30%患者出现骨不愈合;即使并发症在术后可控制,但患者需承受很长时间的功能障碍及各种并发症,将严重影响患者生活质量[34];④感染,由于移植物没有血管,感染很难根除,大部分患者需取出移植物,大块的骨盆移植物感染的发生率更高。因此在骨盆肿瘤的手术治疗中,可借鉴范靖宇等[35]等推广的“原位分离+高温灭活”的保肢技术方法。
2.3.4 复合生物重建 1988年CAPANNA等[36]考虑到带血管蒂游离腓骨在骨不愈合与骨吸收所引起的大段骨缺损保肢手术中的良好作用,结合异体骨移植,首次用对侧带血管蒂游离腓骨与大段异体骨移植相结合的方法,进行复合生物重建。1996年WUISMAN等[37]报道了同侧腓骨与异体骨的复合重建,此方法即可减少手术创面,也可缩短手术时间。随着技术与实验研究的发展,现可用不同方法灭活自体骨,再与自体带血管蒂游离腓骨复合重建,取得成效。带血管蒂的腓骨瓣的应用,术后感染率明显下降[38]。
(1)操作方法:术前使用辅助技术(CT或MRI)确定肿瘤界限,将肿瘤行广泛切除,使用的移植骨应与骨缺损部位匹配。清理移植骨髓腔,在后中侧切约1 cm宽的槽,便于带血管蒂游离腓骨可顺利插入。带血管蒂游离腓骨,应较缺损部位长4.0-5.0 cm,以保证腓骨两端至少各有2 cm骨段插入吻合端。移植骨与缺损部位接合后,用接骨板进行固定,重建体的固定只需用单皮质固定灭活瘤段骨,勿将螺钉固定于腓骨,以防影响腓骨血循坏。之后进行血管缝合[39],受区血管蒂和腓骨瓣血管蒂之间如长度不足,可采用大隐静脉做桥接移植,见图2,3[39-40]。
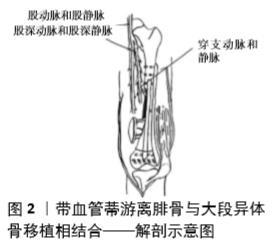

(2)移植骨的处理:复合生物重建中,移植骨同样有两个来源,自体骨与异体骨。处理方法上文已阐述,不再赘述。
(3)复合生物重建的优点:①采取带血管蒂游离腓骨移植,进行血管吻合,可为缺损部位提供血供,从而减少血运相关的并发症。②构建皮质异体骨支架可机械支持带血管蒂游离腓骨,增加生物力学强度,从而降低骨折的风险[41]。③手术中出现的增生肥大,可逐渐吸收,并且骨吸收现象较少见。SUGIURA等[42]的研究中,采用巴氏灭活骨与带血管蒂游离腓骨移植复合,通过临床数据分析可得:巴氏灭活骨结合带血管蒂游离腓骨,可减少移植骨不愈合(从83%减少到19%)和骨吸收情况(从67%减少到0%)。④移植骨中纵向切开的槽,暴露移植骨内表面,利于骨爬行。通过对骨形成蛋白和组织学检测可知,具有骨传导和骨诱导作用,利于移植骨的血管再生与内部修复[43],可促进灭活瘤段骨-宿主骨结合部的骨性愈合。⑤由于手术往往在皮下进行,所以皮肤并发症(创面破溃感染、切口不愈合等)常发生,尤其是胫骨前侧,采用游离皮瓣可减少相关问题。⑥用高压蒸汽灭活自体骨与带血管蒂游离腓骨的复合重建。UMER等[19]的临床数据显示,40例儿科患者经复合重建后,至少18个月时间里,31例患者康复,没有任何并发症;38例患者移植骨与自体骨牢固相接;3例患者出现术后感染,但成功进行清创,并用皮瓣修复缺损处;2例患者出现原位复发与骨不愈合;整体美国骨骼肌肉肿瘤协会功能评分为22分。⑦用放射灭活法自体瘤段骨与带血管蒂游离腓骨复合。在MOTTARD等[30]的研究中,15例患者整体生存率为93%,保肢率为93%,3年后美国骨骼肌肉肿瘤协会功能评分为27.4分。以上临床病例及数据均提示了带血运的腓骨对灭活瘤段骨骨愈合有促进作用,是复合生物重建获得良好功能结果的基础。
当然,复合重建也有常见并发症,如感染、骨折、骨不愈合和骨吸收等,但与单独同种或异体骨移植相比,因采用带血管蒂的游离腓骨移植,其并发症的发生率有所降低。