中国组织工程研究 ›› 2014, Vol. 18 ›› Issue (38): 6079-6084.doi: 10.3969/j.issn.2095-4344.2014.38.003
• 口腔组织构建 oral tissue construction • 上一篇 下一篇
富血小板血浆复合Bio-Oss/Bio-Gide修复兔牙槽骨临界骨缺损
梁恒燕,焦 鑫,王 洋,葛振林
- 兰州大学口腔医院正畸科,甘肃省兰州市 730000
Application of platelet-rich plasma composited Bio-Oss/Bio-Gide to repair a critical-size alveolar defect in rabbits
Liang Heng-yan, Jiao Xin, Wang Yang, Ge Zhen-lin
- Department of Orthodontics, Stomatological Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China
摘要:
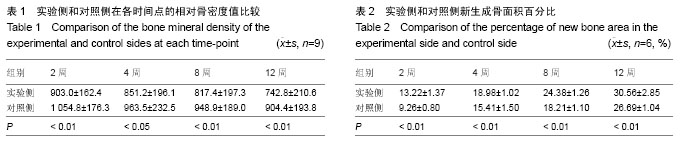
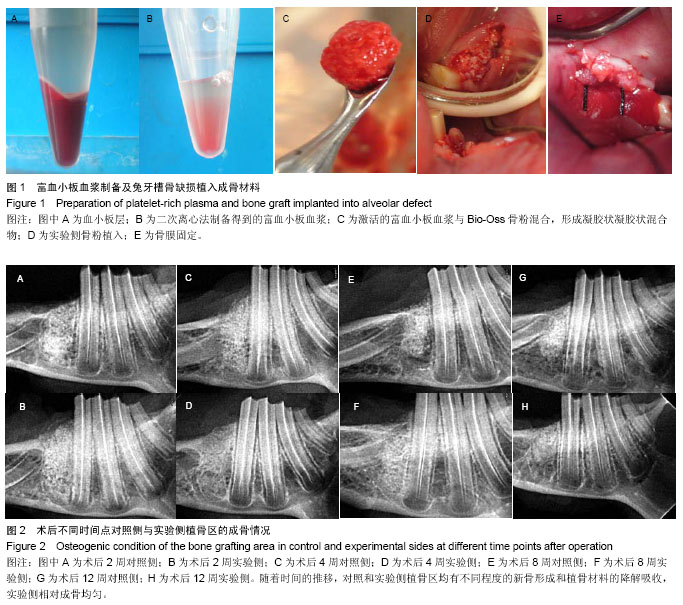
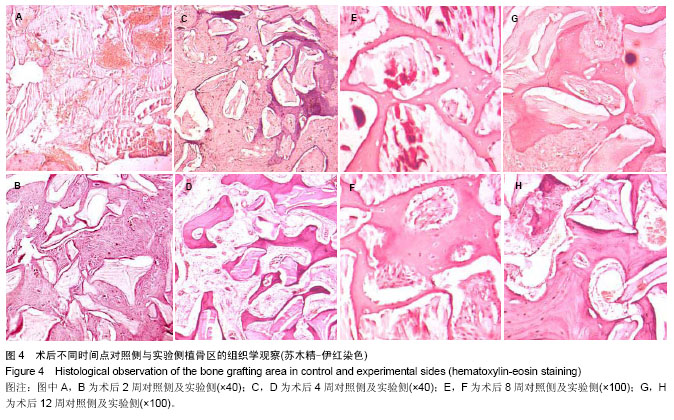
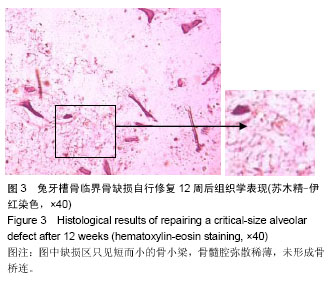
背景:有研究发现,富血小板血浆可促进骨、软组织损伤修复,但在骨愈合过程中的作用仍存在争议,目前尚无定论。 目的:对比观察富血小板血浆复合Bio-Oss/Bio-Gide在兔牙槽骨缺损修复过程中的成骨效果,以探讨富血小板血浆在骨损伤愈合中的作用。 方法:选择新西兰大白兔16只,手术建立兔下颌牙槽骨临界骨缺损模型,采取自身对照,随机选择一侧下颌骨以富血小板血浆/Bio-Oss/Bio-Gide修复骨缺损(实验侧);另外一侧以Bio-Oss/Bio-Gide修复骨缺损(对照侧)。分别于术后2,4,8,12周时各处死4只,通过大体观察、X射线观察、CBCT骨密度测定、组织学切片观察以及新生骨占缺损面积百分比的测定,定性及定量分析牙槽骨缺损区的成骨效果。 结果与结论:术后2-12周的X射线、CBCT及组织学切片观察显示,实验侧和对照侧均有不同程度的新骨形成以及植骨材料的降解吸收;12周时,实验侧缺损表面可见连续的皮质骨形成,植骨区新骨形成并趋于成熟,植骨材料降解吸收明显,对照侧修复效果次之。在术后2,4,8,12周各时间点,实验侧骨密度值均低于对照侧(P < 0.05),实验侧新生骨占面积百分比均大于对照侧(P < 0.05)。说明在兔下颌牙槽骨缺损修复中,富血小板血浆/Bio-Oss/Bio-Gide比Bio-Oss/Bio-Gide具有更好的成骨效果,表明富血小板血浆可促进新骨的形成以及Bio-Oss骨粉的降解吸收。
中图分类号: